Infectieziekten Bulletin
April 2018 | jaargang 29, nummer 4
https://magazines.rivm.nl/2018/04/infectieziekten-bulletin
Gesignaleerd
Overzicht van bijzondere meldingen, clusters en epidemieën van infectieziekten in binnen- en buitenland tot en met 2 april 2018.
Gesignaleerd
Binnenlandse signalen
Beloop griepepidemie in Nederland (vervolg)
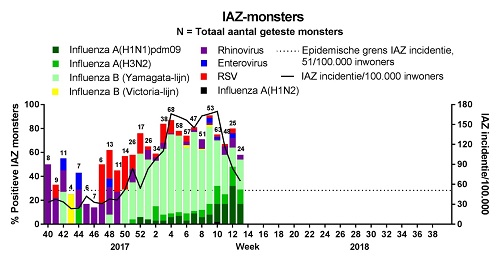
Deze winter is er in Nederland sprake van een langdurige griepepidemie. Het aantal patiënten met een griepachtig ziektebeeld (IAZ, influenza-achtig ziektebeeld) daalde in week 13 naar 65 per 100.000 inwoners. In week 10 waren er nog 166 patiënten per 100.000 inwoners. Week 13 was de zestiende week dat de incidentie van IAZ boven de epidemische grens van 51 per 100.000 ingeschreven patiënten lag. Hoewel influenzavirustype B (Yamagatalijn) tijdens het grootste deel van de epidemie dominant was, nam het aandeel influenzavirustype A gaandeweg het seizoen toe (Figuur 1). Ook in de influenzaviruspositieve monsters die naar het ErasmusMC waren opgestuurd en in de meldingen van de virologische weekstaten, was een verschuiving richting influenzavirustype A zichtbaar. De prevalentie van pneumonie, gemeld door de NIVEL-huisartsen, was hoog vergeleken met voorgaande jaren en het hoogst onder mensen ouder dan 65 jaar. De totale sterfte was hoog, voornamelijk onder patiënten in de leeftijdsgroep van 65 jaar en ouder. Verschillende media berichtten over grote drukte in de ziekenhuizen veroorzaakt door veel patiënten met griep en een tekort aan personeel waardoor operaties moesten worden uitgesteld. (Bronnen: RIVM, Nivel Zorgregistraties eerstelijn peilstations, Virologische weekstaten, CBS, ErasmusMC, Medisch contact, RIVM-sterftecijfers)
Figuur 1. Incidentie van IAZ en laboratoriumuitslagen van monsters van patiënten met IAZ, Nederland, week 40 2017 – week 13 2018
Uitbraken met een panresistente Acinetobacter baumannii
Bij het Signaleringsoverleg Ziekenhuisinfecties en Antimicrobiële resistentie (SO-ZI/AMR) zijn 2 gerelateerde uitbraken gemeld veroorzaakt door een Acinetobacter baumannii, die resistent is tegen alle beschikbare antibiotica (panresistent), waaronder carbapenem en colistine. In juli werd een patiënt met brandwonden na repatriëring uit een conflictgebied in Afrika, in strikte isolatie opgenomen op de intensivecare-afdeling van een ziekenhuis in Nederland. Deze indexpatiënt bleek drager te zijn van een panresistente NDM-positieve Acinetobacter baumannii. Vanaf november 2017, toen de patiënt weer uit bed mocht zijn 3 andere patiënten na elkaar - in november, december en januari - besmet geraakt. De contactonderzoeken wezen uit dat er geen andere patiënten besmet zijn geraakt. Eén van de 3 besmette patiënten werd naar een ander ziekenhuis overgeplaatst. Hoewel dit ziekenhuis ingelicht was en de patiënt in strikte isolatie werd verpleegd, werden tenminste 6 andere patiënten besmet. Het ziekenhuis heeft daarop voor de afdelingen intensive care en medium care een opname- en uitplaatsingsstop ingesteld om de transmissie te stoppen.
Acinetobacter baumannii is vaak multiresistent en dus ongevoelig voor meerdere klassen antibiotica, waaronder carbapenems en veroorzaakt infecties bij mensen met een verminderde afweer. Ook veroorzaakt hij vaak ziekenhuisinfecties, met name op intensivecare-afdelingen. De laatste jaren wordt in een aantal Zuid- en Oost-Europese landen een sterke toename gezien van invasieve infecties door multiresistente Acinetobacter baumannii. Ook worden in >75% van de landen in de Europese Unie (EU) uitbraken, (inter-)regionale verspreidingen of zelfs endemische aanwezigheid in gezondheidszorginstellingen, gemeld. (Bronnen; SO-ZI/AMR, ECDC, CAESAR)
Aantal tuberculosepatiënten gedaald
In 2017 daalde het aantal tuberculosepatiënten in Nederland voor het eerst sinds de eerste registratie in 1950, onder de 800; 787 patiënten ten opzichte van 887 in 2016. De incidentie in 2017 was 4,6 per 100.000 inwoners. Van de 787 patiënten hadden 463 patiënten (59%) longtuberculose, waarvan 203 patiënten sputumpositieve longtuberculose, de meest besmettelijke vorm (open tuberculose). De overige 324 patiënten (41%) hadden extrapulmonale tuberculose. Net als voorgaande jaren was bijna driekwart van het aantal patiënten geboren in het buitenland. De meesten kwamen uit Eritrea (94), gevolgd door patiënten uit Marokko (73) en Somalië (58). Bij 11 patiënten was sprake van een ernstige vorm van resistentie tegen antibiotica (10 patiënten met een isoniazide- en rifampicineresistente bacterie en 1 patiënt met een rifampicineresistente bacterie). In 2017 werden 1.773 patiënten gemeld met latente tuberculose. (Bronnen: RIVM, KNCV Tuberculosefonds)
Psittacose onder bezoekers van een grote vogelbeurs
In Osiris zijn in maart 7 patiënten met psittacose gemeld door 6 GGD’en waarbij, naast het houden van vogels als hobby, een bezoek aan een grote vogelbeurs als mogelijke bron wordt genoemd. Op de beurs, die in februari gehouden werd, waren naar schatting 10.000 vogels en 7400 bezoekers en medewerkers. Er waren ook bezoekers uit o.a. België, Duitsland, Italië, Engeland, Frankrijk, Denemarken, Polen en Hongarije. De patiënten waren binnen 1-4 weken na de beurs ziek geworden. Dit is de incubatietijd van psittacose. 6 patiënten zijn in het ziekenhuis opgenomen. Bij alle 7 patiënten werd de diagnose gesteld met behulp van PCR. Van 5 patiënten is er een genotyperingsuitslag bekend: allen hadden genotype A. Alle 7 patiënten houden thuis vogels. De vogels van de 6 patiënten die de Nederlandse Voedsel- en Warenautoriteit (NVWA) kon testen, waren negatief voor C. psittaci. De GGD en de NVWA gaan samen de organisatoren van de beurs benaderen om een inschatting te verkrijgen van de mogelijkheden voor preventieve maatregelen ter voorkoming zoönotische transmissie van C. psittaci, vooral ook voor een volgende vogelbeurs. (Bronnen: Osiris, NVWA, GGD)
Legionella pneumophila in tweede biologische afvalwaterzuivering
In het zuiden van Nederland is Legionella pneumophila serogroep 1 aangetoond in een biologische afvalwaterzuivering op een bedrijfsterrein. De traditionele biologische afvalwaterzuivering bij dit bedrijf werd in 2012 verbouwd naar een duurzame installatie met productie van biogas. In de beluchtingsvijver werden concentraties tot 80 miljoen KVE/L gevonden. Ook werd Legionella aangetoond in gezuiverd afvalwater dat via een lokaal stroompje op het oppervlaktewater wordt geloosd. De waterzuiveringsinstallatie werd om een de volgende redenen bemonsterd:
- uit de omgeving kwamen sinds 2013 meer meldingen van Legionella dan verwacht. In de periode van 2013 tot maart 2018 ging het om 56 patiënten, terwijl dit in de 5 voorgaande jaren (2008-2012) maar 11 patiënten waren. De stijging is groter dan de landelijk toename;
- in de periode 2013-2017 werd bij 7 van 17 patiënten, een identiek ST-type aangetoond (ST1646). Ook in 2018 is een patiënt gezien waarbij de typering op een ST1646 duidt. Het ST-type werd in 2016-2017 ook gevonden bij een cluster patiënten uit een nabijgelegen gemeente. Hier was een biologische waterzuiveringsinstallatie waarschijnlijk de besmettingsbron. Omdat de typering van de Legionella uit de waterisolaten van de waterzuivering overeenkomt met ST1646 , wordt deze waterzuivering beschouwd als waarschijnlijke besmettingsbron voor een deel van de patiënten in de regio.
Sommige patiënten met ST1646 wonen op enkele kilometers afstand van de installatie. Als de waterinstallatie inderdaad de bron van infectie is voor deze patiënten, duidt dit op een transmissie over een grotere afstand dan tot nog toe is beschreven in de literatuur. Als voorlopige maatregel heeft het bedrijf de beluchtingsbak afgedekt. De concentratie van Legionella in het oppervlaktewater zal nog nader worden onderzocht. De link tussen de 2 waterzuiveringen is nog niet duidelijk. Er is ook onderzoek ingezet naar andere biologische afvalwaterzuiveringsinstallaties als mogelijke bron voor legionelloseclusters in Nederland. (Bronnen: GGD, RIVM)
Buitenlandse signalen
Dengue-uitbraak op La Réunion
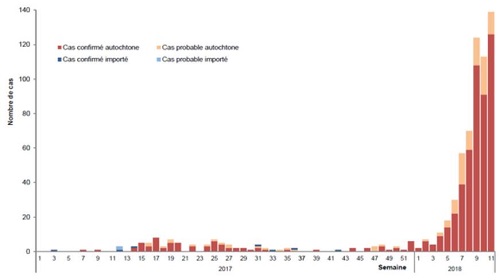
De Franse gezondheidsautoriteiten hebben een dengue-uitbraak op La Réunion gemeld, een eiland met 800.000 inwoners in de Indische Oceaan. Tussen begin januari en eind maart zijn 588 patiënten gemeld die de besmetting ter plaatse hadden opgelopen (Figuur 2). De meeste infecties zijn veroorzaakt door denguevirusserotype 2 (DENV-2), dat ook in 2016 op het eiland circuleerde. Het aantal patiënten in deze tijd van het jaar is voor het zuidelijk halfrond ongebruikelijk hoog en zorgelijk omdat het ‘muggenseizoen’ nog moet beginnen. Er worden maatregelen genomen waaronder intensievere surveillance en muggenbestrijding. De bevolking is verzocht om potentiële broedplaatsen, zoals oude autobanden, blikken, bloempotten en emmers waar water in kan blijven staan, op te ruimen. Het Landelijk Coördinatiecentrum Reizersadvisering (LCR) adviseert alle reizigers naar La Réunion om beschermende middelen te gebruiken tegen muggensteken. (Bron: ECDC).
Figuur 2. Aantal gemelde denguepatiënten, La Réunion, 2017 – 2018 (Bron: Santé Publique France)
Mazelen in Portugal en Frankrijk
De Portugese gezondheidsautoriteiten hebben een uitbraak van mazelen gemeld. Het gaat om 62 patiënten bij wie de diagnose door laboratoriumonderzoek werd bevestigd. 36 van hen werken in een ziekenhuis in Porto. Eén van de patiënten is epidemiologisch gerelateerd aan een mazelenuitbraak die momenteel gaande is in Zuidwest-Frankrijk. Ook door andere EU-landen worden mazelenpatiënten gemeld. In januari 2018 werden 1073 patiënten gemeld, waarvan de meeste uit Griekenland (431), Frankrijk (231), Italië (168) en Roemenië (100). In regio’s grenzend aan de EU - de Balkan en Oekraïne - zijn sinds januari 2018 respectievelijk 3442 en 6484 patiënten gemeld. Hiervan zijn 16 overleden. (Bronnen: ECDC, DGS, SPF)
Zeer resistente Neisseria gonorrhoeae in Groot-Brittannië
De Britse gezondheidsautoriteiten meldden 1 patiënt met een infectie veroorzaakt door Neisseria gonorrhoeae. Deze bacterie is zeer resistent tegen azitromycine (high-level resistance) en resistent tegen ceftriaxon. Azitromycine en ceftriaxon zijn in veel Europese landen belangrijke eerstelijnsantibiotica bij de behandeling van gonorroe. De patiënt meldde zich bij de sexual health service en had waarschijnlijk een maand eerder de infectie opgelopen via heteroseksueel contact in Zuidoost-Azië. De patiënt werd aanvankelijk behandeld met 1g ceftriaxon. Het N. gonorrhoeae-isolaat had een ceftriaxon MIC van 0.5 en een azitromycine MIC van >256 mg/L. De andere antibioticumgevoeligheidsbepalingen lieten alleen gevoeligheid zien voor spectinomycine zien. De patiënt werd hiermee in tweede instantie behandeld. Controle op curatie met behulp van NAAT op urine was negatief, maar de keelswab bleef positief. Herinfectie werd uitgesloten en de patiënt werd vervolgens op geleide van een gevoeligheidsbepaling (MIC 0.032 mg/L) met ertapenem behandeld. Contactonderzoek rond de patiënt werd ingezet maar heeft geen verdere verspreiding aangetoond.
In Nederland is ceftriaxon de eerste keuze voor behandeling van gonorroe. Tot nu toe is in Nederland geen ceftriaxonresistentie gerapporteerd. Wel laat de surveillance van de Centra voor Seksuele Gezondheid zien dat van alle N. gonorrhoeae waarbij in 2017 gevoeligheidsbepalingen werden uitgevoerd, 15% resistent was tegen azitromycine, waarvan 0,2% zeer resistent (MIC >256 mg/L). In 2012 was slechts 6% resistent tegen azitromycine. Dit signaal benadrukt de noodzaak voor het afnemen van kweken voor antibioticumgevoeligheidsbepalingen bij patiënten met gonorroe. (Bronnen: ECDC, PHE, GRAS)
Acute encefalitis door bornavirusinfectie na orgaantransplantatie in Duitsland
De Duitse gezondheidsautoriteiten hebben in de periode 2011-2013 4 patiënten gemeld met acute encefalitis, veroorzaakt door het bornavirustype 1 (BoDV-1); 3 van hen zijn overleden. 3 van de 4 patiënten werden ziek toen zij behandeld werden met immunosuppressiva nadat bij hen organen, afkomstig van 1 donor, waren getransplanteerd. Deze donor had geen neurologische klachten bij overlijden. Alhoewel de bron van infectie van de vierde patiënt niet is gevonden, was het wel duidelijk dat deze besmetting niet gerelateerd was aan de andere 3. Het BoDV-1-genoom en antigeen in de 3 patiënten werd aangetoond met een specifieke RT-qPCR, nieuwegeneratiesequencing, immunohistochemie en met in situ hybridisatie.
Het zoönotisch potentieel van bornavirustype 1 is sinds jaren onderwerp van discussie en onderzoek. Het is nu de eerste keer dat is vastgesteld dat dit bornavirustype ernstige ziekte bij mensen kan veroorzaken. Eerder werd wel beschreven hoe Variegated Squirrel Bornavirustype 1 (VSBV-1) in eekhoorns, encephalitis veroorzaakte bij eekhoornfokkers in Duitsland. Bornavirus heeft in het verleden vooral bij paarden en schapen tot ziekte geleid. Vooral in Zuid-Duitsland en Centraal-Europa is de incidentie van BoDV-1 onder dieren verhoogd. De veldspitsmuis (Crocidura leucodon) wordt verondersteld het natuurlijk reservoir van BoDV-1 te zijn. Alhoewel deze muis voorkomt in Oost- en Zuid-Nederland is het voorkomen van BoDV-1 in dier en mens in Nederland vooralsnog onbekend. Diagnostiek op experimentele basis kan voor zowel BoDV-1 als VSBV-1 worden aangevraagd bij de afdeling Virologie van het ErasmusMC. (Bronnen: RKI, ECDC).
Auteur
T. Leenstra, Centrum Infectieziektebestrijding, RIVM
Correspondentie
Humane leptospirose via een puppy
Een dierenarts krijgt leptospirose (ziekte van Weil) na contact met een zieke pup van een hondenfokker. Met inspanning en geluk wordt een zeer waarschijnlijke match vastgesteld. Het gaat om het Leptospira interrogans s.s. Wat is in zo’n situatie het volksgezondheidsrisico? Het is belangrijk dat zowel mensenartsen als dierenartsen de risico’s van zoönosen onderkennen. Hygiënemaatregelen en preventie, door het vaccineren van honden, kunnen het risico op overdracht beperken. One-health-projecten of projecten over zoönosen en huisdieren kunnen hieraan bijdragen.
Humane leptospirose via een puppy
De casus
In augustus 2016 werd een van de dierenartsen van een dierenkliniek in het ziekenhuis opgenomen met een leptospirose. Op basis van de meldingsplicht pakte GGD IJsselland de bronopsporing op. Een week eerder was de dierenarts bij een hondenfokker geweest om een icterische teckelpup van 8 weken oud, uit een nest van 6, te onderzoeken. De pup (A) overleed 2 uur later. Een dag nadat de dierenarts ziek was geworden kwam de eigenaar met de andere 5 pups uit het nest, naar een collega van de zieke dierenarts voor de tweede vaccinatieserie tegen parvovirus en (de eerste vaccinatie) tegen leptospirose. Eén pup (B) was te ziek om te vaccineren en 2 dagen later kwam de eigenaar terug met deze pup B die inmiddels icterisch was geworden. Uit bloedonderzoek bleek een verstoorde lever- en nierfunctie met een leukocytose. De pup B werd geëuthanaseerd. Dit was 10 dagen na de dood van de eerste pup A. Het ziektebeeld paste mogelijk bij leptospirose, maar bij een pup wordt daar niet zo snel aan gedacht. Het brononderzoek bij de dierenarts leverde geen andere risicovolle activiteiten op. Hij was niet in het buitenland geweest. Zijn eigen (gevaccineerde) honden zwemmen wel regelmatig in natuurwater maar waren niet recent ziek geweest.De vraag is of de puppy’s inderdaad leptospirose hadden en de dierenarts de besmetting opgelopen kan hebben via pup A. Daartoe moet worden aangetoond dat beiden door hetzelfde leptospiratype ziek zijn geworden.
Kan een hond de bron zijn van humane leptospirose?
Leptospirose wordt veroorzaakt door leptospiren, die in de nieren van hun natuurlijke gastheren leven en worden uitgescheiden met de urine. In principe kan bijna elk zoogdier een infectiebron of reservoir vormen, maar het zijn vooral knaagdieren en insecteneters die leptospiren bij zich dragen. De meningen onder professionals over honden als bron van besmetting, zijn verdeeld. Bewijs hiervoor wordt zelden geleverd. Het was dan ook een uitdaging voor de GGD om het leptospiratype in pup B vast te stellen.
Diagnostiek
Naast de beschikbare serologie, PCR-test (polymerase chain reaction) en het kweekonderzoek bij de dierenarts (op stolbloed en EDTA-volbloed) in het laboratorium, bewaarde de dierenkliniek nog bloedmonsters van pup B. Deze bloedmonsters werden naar het Nationaal Referentielaboratorium voor Leptospirosen/Academisch Medisch Centrum Amsterdam in het AMC (NRL) gestuurd voor verder onderzoek. Er werd geen obductie gedaan op de puppy’s.
In het NRL werd het bloed van de dierenarts en van pup B onderzocht. Op de zesde ziektedag van de dierenarts was de PCR positief voor leptospiren en uit het serumonderzoek op ziektedag 19 leek een serovar uit serogroep Icterohaemorrhagiae de meest waarschijnlijke verwekker. De uitslag van het kweekonderzoek was negatief.
Pup B had ook een positieve PCR voor leptospiren. De smeltcurves van beide PCR-producten gaven leptospiren species interrogans aan. De serovars uit serogroep Icterohaemorrhagiae die in Nederland voorkomen behoren tot L. interrogans. Verdere typering met MLST (Multilocus sequence typing) liet zien dat ook pup B geïnfecteerd was met een serovar uit serogroep Icterohaemorrhagiae.
Op basis van de PCR, MLST en serologieresultaten bleek dat zowel de dierenarts als pup B besmet waren met een serovar uit de serogroep Icterohaemorrhagiae met als species interrogans s.s. Het was zeer waarschijnlijk dat de dierenarts de leptospirosebesmetting van pup A had opgelopen.
Bron- en contactopsporing
In overleg met de GGD ging de Nederlandse Voedsel- en Warenautoriteit (NVWA) langs bij de eigenaar/hondenfokker die op een boerderij woonde. De pups A en B kwamen uit een nest van 6 teckelpups. De moederhond was het laatste jaar niet gevaccineerd tegen leptospirose. Zij heeft geen maternale antistoffen via de melk aan haar pups kunnen doorgeven. De teckels en poezen op de boerderij vingen regelmatig ratten die ze de schuur mee in namen. Het nest met de pups was in een schuur en daar kwamen ook ratten. Pas op de leeftijd van 9 weken krijgen de pups hun eerste leptospirosevaccinatie. De NVWA besprak hygiënemaatregelen en manieren om ratten uit de schuur te houden.
Twee andere pups uit het nest waren ondertussen naar nieuwe eigenaren gegaan die wel gewaarschuwd werden voor leptospirose. Een van deze pups kwam in een gezin in de omgeving, werd matig ziek en werd in de dierenkliniek uit deze casus direct behandeld voor leptospirose. In het gezin waren ook kinderen die dus een risico hadden gelopen op leptospirose. De andere pup verhuisde naar een ander deel van het land en werd daar preventief door een dierenarts behandeld.
Aanbevelingen/overwegingen
voor de GGD
- Maak een inschatting van de hoogte van het risico voor de volksgezondheid en bepaal aan de hand daarvan in hoeverre het zinvol is om besmetting van dier naar mens te bewijzen. In deze casus heeft meegewogen dat er een hondenfokkerij bij betrokken was. Echter, ook in geval van een klein risico voor de volksgezondheid, is het soms goed om vervolgonderzoek te doen, ook om de eigen kennis te voeden. Ondanks de extra inzet die dit vergt, zien wij dit ook als een van de taken van een GGD.
- Het is over het algemeen niet altijd makkelijk om van patiënten die inmiddels beter zijn, instemming te krijgen om opnieuw een monster af te nemen voor vervolgonderzoek. Dit vergt soms overredingskracht van de GGD. Van een patiënt met leptospirose is gedurende de eerste 10 ziektedagen EDTA-bloed en heparinebloed nodig voor PCR en kweekonderzoek en stolbloed voor |(bij voorkeur 2-punt) serologie. Pas 1 tot 2 weken na de eerste ziektedag zijn de titers hoog genoeg om een stijging aan te tonen.
- Bij honden die vermoedelijk leptospirose hebben wordt meestal geen specifieke diagnostiek ingezet en worden er zeker geen bloedmonsters bewaard. De GGD zal zich dan ook actief moeten inzetten om, in gevallen zoals deze casus, tot een match te komen tussen mens en dier. Door de incubatietijd van maximaal 30 dagen is het achteraf inzetten van bloedonderzoek bij een mogelijk bron nu nog zeer beperkt mogelijk.
- Bepaal de rol van de NVWA in een casus als deze: toezichthouder dierwelzijn of adviseur voor dierwelzijn en volksgezondheid? Welke rol kan de GGD hierbij spelen?
- Leptospirose bij huisdieren is niet meldingsplichtig. Bij wie ligt de rol om diagnostiek te organiseren voor brononderzoek aan de veterinaire kant? En hoe is de financiering en diagnostiek geregeld? Omdat leptospirose een risico voor de volksgezondheid kan betekenen, kan de GGD de regie nemen in het beantwoorden van deze vragen. Het gebruik van het budget van de openbare gezondheidszorg (OGZ) van de GGD zal per casus beoordeeld moeten worden. In deze casus heeft het NRL op verzoek van/in opdracht van de GGD diagnostiek verricht ten behoeve van brononderzoek.
voor de dierenarts
- Vaccineren van een moederhond tegen leptospirose wordt sterk geadviseerd.
- Bij een zieke pup wordt niet snel aan leptospirose gedacht. Wel bij jachthonden en oudere honden. Iedere hond die met buitenwater in contact komt, loopt echter een risico. Dit kan door zwemmen en spelen in modderplassen, maar mogelijk ook door drinken uit waterplassen.
- De dierenarts heeft een vertrouwensrelatie met degene die met zijn huisdier langskomt. Dit kan van invloed zijn als er diergegevens worden opgevraagd in een situatie waarbij een risico is ontstaan voor de volksgezondheid
- In hoeverre krijgen hondeneigenaren informatie van de dierenarts over de risico’s van leptospirose? Jaarlijkse vaccinatie (na een dubbele initiële vaccinatie) in het voorjaar beschermt de hond en indirect de eigenaar tegen leptospirose. 10% van de humane besmettingen verloopt zeer ernstig en 3% van deze patiënten overlijdt. De ernst van zoönosen bij huisdieren zou vaker onderwerp moeten zijn van bijscholingsprojecten voor dierenartsen en One-health-projecten.
- Is iedere medewerker in een dierenkliniek zich bewust van het risico dat hij zelf loopt om besmet te worden? En in hoeverre hij een rol kan spelen bij het besmetten van andere dieren? Weten medewerkers hoe belangrijk en wat de juiste hygiënemaatregelen zijn?
- Leptospirose kan bij alle honden voorkomen, ook bij pups.
- Hondeneigenaren en medewerkers van een dierenkliniek lopen risico op leptospirose als ze niet de juiste hygiëne betrachten.
- Samenwerking tussen artsen, dierenartsen en de sector publieke gezondheid is van belang voor vroege signalering van leptospirose en het nemen van preventie/bestrijdingsmaatregelen. GGD’en zouden aan kunnen sluiten bij regionale One-Health-projecten waar ook dierenartsen voor gezelschapsdieren aan meedoen.
Conclusie en aanbeveling
Het is belangrijk dat de GGD een bijdrage levert aan zoönoseonderzoek. In deze casus werd dit bemoeilijkt door de lange incubatietijd en diagnostische mogelijkheden voor typering van leptospirose. Alhoewel in de literatuur bewezen overdracht van leptospirose van hond naar mens nog niet is beschreven, heeft deze casus laten zien dat het wel mogelijk. Het is dan ook belangrijk om dit verder te onderzoeken. De ernst van het ziektebeeld leptospirose bij zowel mens als dier verantwoordt de extra inspanning van alle partijen. De meldingsplicht voor artsen en voor dierenartsen verschilt van elkaar en dit beperkt de mogelijkheid om snel te reageren bij infecties bij huisdieren. Een laatste aspect dat een het afhandelen van deze casus bemoeilijkte was de onduidelijk financiering voor de diagnostiek.
Deze casus werd gekenmerkt door goede samenwerking tussen de GDD, NVWA en de patiënt. Ook bij toekomstige zoönosen blijft extra inspanning en samenwerking belangrijk. Misschien dat voor volksgezondheidsrisico’s door huisdieren ook landelijke afspraken gemaakt kunnen worden voor diagnostische mogelijkheden, financiële middelen en over meldingen van infecties bij huisdieren.
Met dank aan Marga Goris, NRL, Harry Rozendaal en Jörg Zenker, NVWA, patiënt/dierenarts
Auteurs
S. de Jong, M.J. Vossebelt, GGD IJsselland
Correspondentie
sandra.de.jong@ggdijsselland.nl
Infectieziekten Bulletin, jaargang 29, nummer 4, april 2018
Hepatitis A-uitbraak op een zorgboerderij
In juni 2017 was er in Limburg een uitbraak van hepatitis A onder cliënten met een verstandelijke beperking van een zorgboerderij. De uitbraak speelde in 2 GGD-regio’s op het moment dat er een landelijk tekort was aan hepatitis A-vaccin en laat zien hoe complex uitbraakbestrijding in een kwetsbare populatie kan worden. Ook wordt duidelijk hoe belangrijk het is om bestrijdingsmaatregelen onderling af te stemmen.
Hepatitis A-uitbraak op een zorgboerderij
De uitbraak
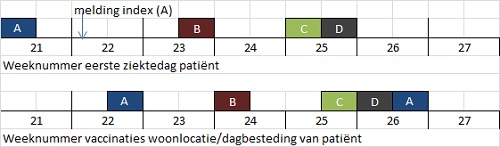
Op 30 mei 2017 kwam bij de GGD Limburg Noord een melding binnen van een patiënt met een hepatitis A. Het bleek te gaan om een man met een verstandelijke beperking (patiënt A, index). Hij was op 23 mei icterisch geworden (Figuur 1). Patiënt A woonde samen met andere mensen met een verstandelijke beperking. Als dagbesteding werkte hij op een zorgboerderij in Zuid-Limburg. Een groep mensen uit zijn nabije omgeving werd geïmmuniseerd: 33 medewerkers en 21 medecliënten op de zorgboerderij, 13 medebewoners en de begeleiders, vrijwilligers, schoonmaakpersoneel en het technisch personeel op de woonlocatie. Vanwege het landelijk tekort aan hepatitis A-vaccin ten tijde van de melding werd besloten om ook contactpersonen jonger dan 40 jaar passieve immunisatie met gammaglobulines aan te bieden. (1, 2) GGD Limburg Noord bepaalde het schoonmaak- en desinfectiebeleid in overleg met de medische dienst van de woonlocatie. GGD Zuid-Limburg werd op de hoogte gesteld, vanwege de locatie van de zorgboerderij en omdat de medewerkers en medecliënten van patiënt A verspreid over Limburg woonden.
Figuur 1 Tijdspad van de uitbraak. De letters in de figuur verwijzen naar de betreffende patiënt in de tekst. Bovenste tijdsbalk verwijst naar de eerste ziektedag per patiënt; de onderste tijdsbalk naar het tijdstip van de vaccinatie per patiënt. Door het verloop van de uitbraak met de uiteindelijke sterke verdenking dat de bron op de zorgboerderij lag, is op een later tijdstip de eerste vaccinatie-actie (A, week 22) geëvalueerd en besloten die uit te breiden naar een groep medewerkers van de ‘buitenploeg’ van de zorgboerderij (vaccinatie-actie A, week 26).
Op 10 juni, 2 weken na de eerste melding, kreeg de GGD Zuid Limburg een melding van acute hepatitis A bij een cliënt (patiënt B) die ook werkzaam was op de zorgboerderij waar patiënt A werkte. Ook hij woonde samen met andere mensen met een verstandelijke beperking. Patiënt B was een week eerder, op 2 juni, geïmmuniseerd met gammaglobulines. Diezelfde dag waren door de medische dienst van zijn woonlocatie ook zijn medebewoners (n=16) en het verzorgend personeel geïmmuniseerd met gammaglobulines.
Nadat bijna 2 weken later, op 20 juni, opnieuw een acute hepatitis A bij een cliënt van wederom dezelfde zorgboerderij (patiënt C) was gemeld bij de GGD Zuid Limburg, werd besloten een afstemmingsoverleg te houden tussen de 2 betrokken GGD’en en de instelling voor gehandicaptenzorg waartoe de woonlocaties van de patiënten behoorden. Ook patiënt C had op 2 juni gammaglobulines toegediend gekregen. Na de melding van patiënt C werden door de GGD Zuid Limburg 22 medebewoners en 23 medewerkers van de woonlocatie geïmmuniseerd met hepatitis A-vaccin of gammaglobulines. Andere medewerkers die niet aanwezig waren, werden later via het reizigersvaccinatiebureau geïmmuniseerd.
Op 23 juni volgde nog een vierde melding, ditmaal van een medewerker (patiënt D) van de zorgboerderij. Ook hij had tijdens de eerste vaccinatieactie op de zorgboerderij gammaglobulines gekregen. Zijn (gezins)contacten werden conform de richtlijn van de Landelijke Coördinatie Infectieziektebestrijding (LCI) van het RIVM geïmmuniseerd.
Verloop
Bij alle patiënten was er een duidelijk klinisch beeld (icterus) passend bij acute hepatitis A. Conform de LCI-richtlijn is overwogen om patiënten met mogelijk asymptomatische hepatitis A op te sporen met PCR. (3) Toch is besloten om niet aan dergelijke actieve case-finding te doen: gezien de leeftijd van de betrokkenen was het aannemelijk dat nieuwe besmettingen met hepatitis A-virus (HAV) symptomatisch zouden verlopen.
De betrokken instelling werd geadviseerd om voor een periode van tweemaal de maximale incubatietijd (in totaal 14 weken) na de melding van patiënt D, alert te zijn op nieuwe besmettingen onder personeel of bewoners. Er zijn uiteindelijk geen nieuwe patiënten meer gemeld die gerelateerd waren aan de zorgboerderij of een woonlocatie van de instelling.
Patiënten B, C en D waren op 2 juni geïmmuniseerd met gammaglobuline, binnen 2 weken na de eerste ziektedag van patiënt A. De te verwachten beschermingsgraad van gammaglobuline als post-expositieprofylaxe is 80-90% wanneer die binnen 2 weken na blootstelling is gegeven. (4) Het feit dat de vaccinatie-actie tijdig is gestart met de korte tijdsperiode tussen de eerste ziektedagen van de patiënten B-D, maakt het waarschijnlijk dat alle patiënten aan dezelfde besmettingsbron waren blootgesteld. Vanwege de sterke verdenking dat de bron op de zorgboerderij lag, is op een later tijdstip de eerste vaccinatie-actie geëvalueerd en besloten die uit te breiden naar een groep medewerkers van de buitenploeg van de zorgboerderij.
Tegelijk met deze uitbraak was er ook een landelijke verheffing van hepatitis A onder mannen die seks hebben met mannen (MSM). (1) Een van de HAV-stammen die gevonden werden bij deze uitbraken was 1A Europride/Taiwan (RIVM-HAV16–069); de stam wordt ook gevonden in niet-MSM.(5) De stam werd ook gevonden bij alle patiënten in de uitbraak op de zorgboerderij. Verder was er een landelijk hepatitis A-uitbraak die gerelateerd was aan voedsel. (1) Bij alle patiënten zijn daarom ook de Osiris-vragenlijst en de voedselconsumptievragenlijst afgenomen. Er waren (anamnestisch) bij deze uitbraak geen aanwijzingen voor seksuele transmissie. Het is helaas niet gelukt om de bron van de uitbraak te achterhalen.
Conclusie
Deze uitbraak toont aan dat een hepatitis A-uitbraak op een speciale locatie waar mensen met een verstandelijke beperking werken, de potentie heeft om zeer groot te worden. Gelukkig is dat binnen deze casus niet gebeurd, al werden er wel meer dan 100 mensen geïmmuniseerd. De beperkte beschikbaarheid van hepatitis A-vaccin heeft geen rol gespeeld in het verloop van deze uitbraak. Vanuit het RIVM waren de GGD’en geadviseerd om tijdens deze vaccinschaarste voldoende vaccin voorradig te hebben voor onder andere gezinscontacten van patiënten. Het aantal vaccinaties dat tijdens deze uitbraak nodig was, was echter beduidend meer dan in voorraad was. Vanwege de schaarste werd daarom in eerste instantie gekozen voor passieve immunisatie als postexpositieprofylaxe. Passieve immunisatie levert een snelle, adequate bescherming tegen hepatitis A op. (3) Later in de uitbraak heeft het reizigersvaccinatiebureau Ease Travel & Health Clinic bijgedragen aan de levering van vaccin aan de GGD Zuid Limburg.
Een discussiepunt is of we als GGD’en niet pro-actiever aan case-finding en brondetectie hadden moeten doen. Diagnostiek bij patiënten met asymptomatische klachten met behulp van PCR was kostbaar geweest en een grote logistieke operatie. Serologische diagnostiek inzetten had als nadeel dat besmettingen in een vroeg stadium mogelijk gemist zouden worden. Ook had diagnostiek ons niet geholpen in onderscheid tussen besmettingsbron en contacten. Bij verdere verspreiding was inzet van diagnostiek het heroverwegen waard geweest.
In het begin verliep de onderlinge afstemming tussen beide GGD’en niet gemakkelijk: belangrijke details kwamen soms pas later in beeld. Inzage in elkaars notities was niet mogelijk, ondanks gebruik van dezelfde software (HPZone). Het bestrijden van deze uitbraak was makkelijker verlopen wanneer het bijvoorbeeld mogelijk was geweest real-time dossiers te delen toen hier aanleiding toe was. Het is belangrijk om bij een regio-overschrijdend probleem direct afspraken te maken over coördinatie en inhoudelijke afstemming. De lijnen van communicatie, vooral met externe partijen zoals het LCI en de instelling(en), moeten onderling besproken worden. Het overleg met alle partijen tijdens deze uitbraak hebben wij als een prettige manier van afstemming ervaren. Een aanbeveling die hieruit voortkomt, is om bij het oefenen van een grootschalige uitbraak ook het oefenen met naburige GGD’en niet te schuwen.
Met dank aan de betrokken medewerkers van de GGD Limburg Noord en GGD Zuid Limburg, Ease Travel & Health Clinic.
Auteurs
A. Verhaegh-Haasnoot1, M. Bongartz2, C.D.J. den Heijer1
- Afdeling Seksuele Gezondheid, Infectieziekten en Milieu, GGD Zuid Limburg, Heerlen
- Afdeling Infectieziektebestrijding, GGD Limburg-Noord, Venlo
Correspondentie
Literatuur
- European Centre for Disease Prevention and Control. Hepatitis A outbreak in the EU/EEA mostly affecting men who have sex with men – third update, 28 June 2017. Stockholm: ECDC; 2017.
- Bantjes S, Meiberg A, Sonder G, Petrignani M, Isken L, Ruijs H, et al. Inf@ct: Hepatitis A- en hepatitis B-vaccins beide beperkt beschikbaar 26-4-17 ed. Bilthoven: RIVM; 2017.
- LCI-richtlijn Hepatitis A. Laatste revisie juli 2013 ed: RIVM.
- Winokur PL, Stapleton JT. Immunoglobulin prophylaxis for hepatitis A. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America. 1992;14(2):580-6.
- Communicable disease threats report: Week 1, 31 December 2017-6 January 2018. Stockholm, Sweden: European Centre for Disease Prevention and Control 2018 06-01-2018.
Infectieziekten Bulletin, jaargang 29, nummer 4, april 2018
De hygiënebuddy: de coach bij het handenwassen
In 2016 won GGD Zeeland de GGD-innovatieprijs met het idee van de Hygiënebuddy: een innovatief handhygiëne-feedbackcomputerprogramma voor gebruik in verpleeghuizen. Het programma dat ingebouwd is in een wastafel ‘herkent’ zorgmedewerkers en ‘coacht’ hen bij het toepassen van de juiste handhygiëne. De hygiënebuddy kan bijdragen aan het inperken van de verspreiding van resistente bacteriën. Als zorgmedewerkers de aanwijzingen van de hygiënebuddy goed opvolgen, zijn hun handen voldoende schoon. GGD Zeeland en studenten van de HZ University of Applied Sciences hebben een voorlopig prototype van de hygiënebuddy gebouwd.
De hygiënebuddy: de coach bij het handenwassen
Wat is de hygiënebuddy?
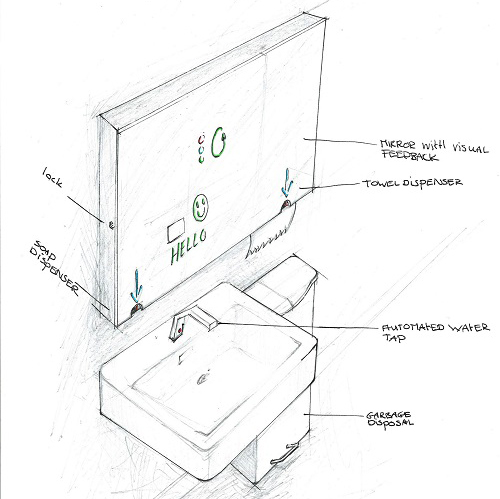
De hygiënebuddy ziet eruit als een wastafelmeubel en heeft een ingebouwd computerprogramma om zorgmedewerkers te ondersteunen bij het correct uitvoeren van handhygiëne. Het wastafelmeubel heeft een spiegel en een wasbak met kraan, stromend water, een zeeppompje en een houder voor papieren handdoekjes gemonteerd onderaan de spiegel (Figuur 1). Het programma start met het identificeren van de gebruiker/zorgmedewerker. Hierna verschijnen op de spiegel visuele instructies over welke handhygiëne uitgevoerd moet worden. De spiegel registreert via een wifiverbinding het aantal handenwasmomenten van de gebruikers in een database. Op basis van de registraties kunnen de zorgteams de effectiviteit van de toegepaste handhygiëne bespreken en de juiste handhygiëne stimuleren.De hygiënebuddy kan ook ‘gewoon’ worden gebruikt zonder dat er instructies op de spiegel verschijnen.
Figuur 1. Ontwerp hygiënebuddy
Hoe is dit idee ontstaan?
GGD Zeeland voert in een aantal zorginstellingen jaarlijks hygiëne-audits uit. Uit de audits blijkt dat de handhygiëne niet altijd correct worden uitgevoerd. De handen worden niet ingezeept volgens de hygiënestandaard How to handwash van de World Health Organization (WHO, 2016). Er zijn niet altijd papieren handdoekjes en men gebruikt dan textiele handdoeken. Ook is het opvallend dat er nauwelijks feedback wordt gegeven door leidinggevenden over de manier waarop de handhygiëne al dan niet correct wordt uitgevoerd. Tijdens een brainstormsessie over deze constateringen is het idee over een hygiënebuddy ontstaan.
In 2016 werden GGD’en opgeroepen door het Centrum Infectieziektebestrijding (CIb) van het RIVM om ideeën in te sturen voor de GGD-Innovatieprijs 2016. GGD Zeeland presenteerde het idee van de hygiënebuddy. De GGD-Innovatieprijs is wordt uitgereikt voor innovaties in producten, diensten, methoden of processen op het terrein van infectieziektebestrijding. Het uitreiken van deze prijs wordt beschouwd als voorronde voor de RIVM-Innovatieprijs. In het jurycommentaar stond het volgende vermeld over de hygiënebuddy: “Het idee om het handen wassen te nudgen, spreekt de jury erg aan! We zijn benieuwd wat er allemaal mogelijk is op korte termijn met een klein budget en in samenwerking met innovatieve partijen in het land.”
Hoe is het prototype gebouwd?
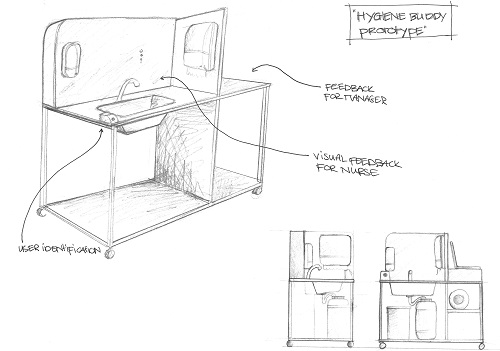
Een team van studenten Engineering, minor mechatronics aan de HZ University of Applied Sciences heeft een voorlopig prototype van de hygiënebuddy gebouwd (Figuur 2). Het team was opgedeeld in subteams die zich bezighielden met identificatie, gegevensopslag, productdesign of het handenwasproces. De beslissingen die voor elk onderdeel gemaakt moesten worden, werden genomen op basis van literatuuronderzoek en de input van experts en zorgmedewerkers van een verpleeghuis.
- Het programma start met de identificatie van de gebruiker/zorgmedewerker aan de hand van een persoonsgebonden tag. Hiermee wordt voorkomen dat de handhygiënegegevens van ‘gewone’ gebruikers (bijvoorbeeld bezoekers) worden meegeteld.
- De database waarin wordt geregistreerd hoe vaak gebruikers/zorgmedewerkers hun handen wassen, is eenvoudig toegankelijk voor leidinggevenden en medewerkers. Dit biedt mogelijkheden om het onderwerp handhygiëne te bespreken tijdens teamoverleggen.
- Voor het productdesign waren de eisen dat de onderdelen glad en afwasbaar moeten zijn. Ook moet er voldoende ruimte zijn tussen de kraan en de onderkant van de wasbak. Je hebt ruimte nodig om je handen goed in te zepen en af te spoelen.
- Het ‘traject’ van het op de goede manier wassen van de handen is in stukken geknipt en ‘vertaald’ naar pictogrammen die elk een volgende stap uitbeelden. De stappen zijn bepaald zoals omschreven in de hygiënestandaard How to handwash. De pictogrammen worden volgens een tijdschema geprojecteerd op de spiegel. Uiteraard kan men langer over de procedure doen maar niet korter. De tijd die het kost om bij het handenwassen de hygiënebuddy te gebruiken is nauwelijks meer dan de tijd die goed handenwassen kost zonder hulp van de hygiënebuddy.
Door de input van het zorgpersoneel konden de bouwers het gebruik van de hygiënebuddy zo goed mogelijk naar hun wensen afstemmen. Een van hun verzoeken was bijvoorbeeld om het ook voor mensen in een rolstoel mogelijk te maken om de buddy te gebruiken. En ook wordt met opzet niet gebruik gemaakt van gesproken instructies, omdat die overstemd zouden kunnen worden door omgevingsgeluiden.
Figuur 2. Prototype hygiënebuddy
Hoe verloopt dit traject verder?
In het eerste kwartaal van 2018 is het voorlopige prototype van de hygiënebuddy door de studenten opgeleverd. Hierna zullen zij in een gezamenlijk project, een geavanceerder prototype bouwen. Ter voorbereiding gaat een groep HBO-studenten Verpleegkunde met het voorlopige prototype een onderzoek doen bij een verpleeghuis waarbij ze de stelling ‘Handen worden vaker gewassen met behulp van de hygiënebuddy’ zullen toetsen. Voorafgaand aan het onderzoek wordt een nulmeting uitgevoerd op basis van observatieonderzoek en na afloop zal de situatie opnieuw gemeten worden. Daarnaast wordt met behulp van een enquête onderzocht wat zorgmedewerkers vinden van de instructiepictogrammen op de spiegel. Op basis van de bevindingen van dit onderzoek zullen de studenten aanbevelingen ter verbetering opstellen.
Waar kan de hygiënebuddy nog meer worden ingezet?
Er zijn meerdere ideeën om de hygiënebuddy uit te bouwen. Bijvoorbeeld met pictogrammen van beschermende maatregelen, richtlijnen en afvinklijsten. Tevens is een wens om de kwaliteit van de handhygiëne te kunnen meten en een handdesinfectiemodule in te bouwen. Verder kan de hygiënebuddy ook worden ingezet in andere sectoren zoals in de horeca of in kinderdagverblijven of tijdens festivals.
Het traject van idee naar prototype is een leertraject voor de GGD. Het is een voorbeeld van hoe techniek en zorg samen komen om een bepaald doel te bereiken, in dit geval zo veel mogelijk verspreiding van resistente bacteriën voorkomen.
Auteur
C.L. Verdonk, GGD Zeeland
Correspondentie
Caroline.verdonk@ggdzeeland.nl
Infectieziekten Bulletin, jaargang 29, nummer 4, april 2018
Zwangerschap en de ziekte van Chagas
Een verloskundige had in mei 2017 een cliënt van Braziliaanse afkomst in de praktijk, die sinds een paar maanden in Nederland woonde. De zwangere vrouw gaf aan dat in Brazilië, vrouwen tijdens de zwangerschap routinematig wordt gescreend op de ziekte van Chagas. Zij wilde dit ook in Nederland laten doen. De verloskundige wilde van de GGD weten of dit noodzakelijk is, wat deze screening inhoudt en waar die wordt uitgevoerd. Een LCI-richtlijn (Landelijke Coördinatie Infectieziektebestrijding) over dit onderwerp ontbreekt en daarom beschrijven we hieronder wat de ziekte van Chagas is en wat screening naar de ziekte bij zwangere vrouwen inhoudt.
Zwangerschap en de ziekte van Chagas
Ziekte van Chagas
Kliniek
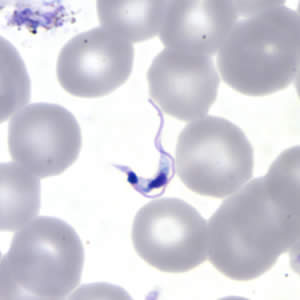
De ziekte van Chagas is een ziekte die wordt veroorzaakt door de parasiet Trypanosoma cruzi (Afbeelding 1). Hij kan worden overgedragen via roofwantsen, gecontamineerd sap of via bloed van geïnfecteerde personen. De klinische presentatie van de ziekte van Chagas is onder te verdelen in 2 fasen:
- De acute fase verloopt bij de meeste patiënten asymptomatisch en duurt 4 – 8 weken. (1) Deze fase kenmerkt zich door een hoge parasitaemie. Symptomen in de acute fase zijn koorts, een lokale ontstekingsreactie bij een beet van een roofwants (een rode zwelling rondom het oog en op het ooglid wordt ‘het teken van Romaña’ genoemd), lymfadenopathie en hepatosplenomegalie. In zeldzame gevallen verloopt een acute infectie ernstig met cardiale en neurologische symptomen. (2) Na circa 90 dagen daalt het aantal parasieten in het perifere bloed en blijft de parasiet voornamelijk intracellulair aanwezig in glad spierweefsel, hartweefsel en gastro-intestinaalweefsel aanwezig. (1)
- Als patiënten niet behandeld worden, komen ze hierna in de chronische fase, waarbij op termijn met name cardiale en gastro-intestinale complicaties kunnen ontstaan. (3) Cardiale afwijkingen worden hierbij het meest gezien. Orgaanschade met bijbehorende klachten ontstaat bij 30 tot 40% van de geïnfecteerde patiënten, 10 tot 30 jaar na het moment van de acute infectie. (1) Re-activatie van de infectie in de chronische fase door immunosuppressie is mogelijk. Schade in de weefsels wordt waarschijnlijk veroorzaakt door de parasiet zelf en de ontstekingsreactie van het lichaam op de parasiet. (1)
Afbeelding 1. Trypanosoma Cruzi op dikkedruppelpreparaat gekleurd met Giemsakleuring (Bron: CDC)
Een congenitale T. cruzi-infectie bij een pasgeboren baby verloopt vaak asymptomatisch. Als er wel symptomen zijn, dan zijn deze vaak aspecifiek. Myocarditis of meningo-encephalitis zijn ernstige complicaties van een congenitale infectie, maar worden slechts zelden gezien.(4) De complicaties van congenitale infectie - met name cardiale en/of gastro-intestinale afwijkingen - worden meestal pas later in het leven als zodanig herkend en zijn dan over het algemeen onomkeerbaar
Transmissieroutes
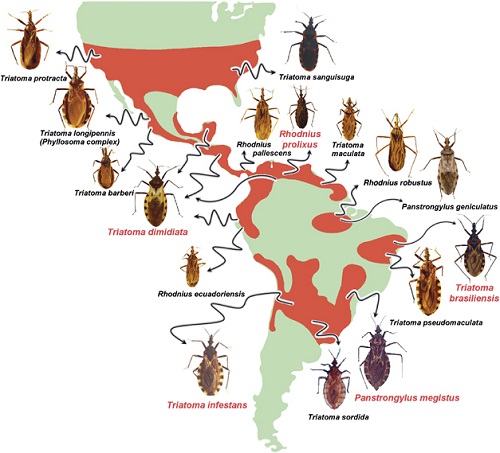
Trypanosoma cruzi wordt overgedragen via roofwantsen (triatomine) ook kissing bugs genoemd, die in Latijns-Amerika voorkomen (Figuur 2). (5) Deze roofwantsen voeden zich onder andere met bloed van ratten, gordeldieren, andere kleine zoogdieren en mensen. Zij kunnen allemaal een reservoir zijn voor de T. cruzi-parasiet. De roofwantsen bijten voornamelijk ’s nachts.(6) Ze zuigen bloed op en tegelijkertijd lozen ze met T.cruzi besmette ontlasting. De ontlasting van de wants komt zo in de buurt van de bijtplek op de huid. Als men hierna over de jeukende plek wrijft, kan de besmette ontlasting tot een infectie leiden. De besmette ontlasting kan, indien vermengd met voedsel of vruchtensap en andere dranken, gastro-intestinale infecties bij mensen veroorzaken. Deze infecties kunnen een ernstig beloop hebben. (1)
Figuur 2. Verspreiding van roofwantsen in Latijns-Amerika. (Bron: Gourbière et al. Genetics and evolution of triatomines: From phylogeny to vector control. Heredity (Edinb). 2012 Mar;108(3):190-202)
Andere belangrijke transmissieroutes zonder betrokkenheid van vectoren, zijn via bloedtransfusies en orgaantransplantaties en het doorgeven van T. cruzi van een moeder aan haar ongeboren kind. Dit laatste kan een congenitale infectie van T. cruzi bij het kind tot gevolg hebben. Bij zwangere vrouwen die geïnfecteerd zijn met T. cruzi vindt bij ongeveer 4,7% (range 3,9-5,6%) transmissie naar het kind plaats, waarbij de transmissie in endemische landen mogelijk hoger ligt dan in niet-endemische landen (5% versus 2,7%). Dit heeft waarschijnlijk te maken met de aanwezigheid van meerdere subtypen van de parasiet in endemische landen. Sommige subtypen zijn makkelijker verticaal over te dragen. (1)
Na infectie vermenigvuldigt de parasiet zich intracellulair in het menselijk lichaam. Na het volwassen worden van de parasieten, barsten de geïnfecteerde cellen open en komen de parasieten in de bloedcirculatie terecht. Roofwantsen nemen met een volgend bloedmaal bij een geïnfecteerd persoon de parasieten op en kunnen weer nieuwe personen infecteren. (1)
Epidemiologie
De ziekte van Chagas is endemisch in 21 Latijns-Amerikaanse landen, van het zuiden van de Verenigde Staten tot het noorden van Argentinië en Chili. Naar schatting zijn wereldwijd 8 miljoen mensen geïnfecteerd met T. cruzi (en hebben dus de ziekte van Chagas), waarvan naar schatting 2 miljoen vrouwen in de vruchtbare leeftijd. Het vóórkomen van de ziekte van Chagas varieert sterk per land en per regio. De hoogste prevalentie wordt gevonden in de armste gebieden van Bolivia, Argentinië en Mexico. (7) In Brazilië is het aantal patiënten echter ook niet onaanzienlijk met in 2015, naar schatting, 119.000 vrouwen met de ziekte van Chagas in de leeftijdsgroep van 15 tot 44 jaar. De seroprevalentie in Brazilië is gemiddeld 0,03% met sterke verschillen tussen de regio’s (8).
Het vóórkomen van de ziekte van Chagas is sterk verbonden aan de aanwezigheid van vectoren voor de infectie en contact van deze vectoren met de mens. Van oudsher vonden de meeste infecties plaats op het platteland waar de roofwantsen veel voorkwamen in slecht onderhouden of slecht geïsoleerde huizen, met spleten of gaten in de daken en muren, en met palmbladen als dakbedekking.
De afgelopen jaren hebben er grote verschuivingen plaatsgevonden in de epidemiologie van de ziekte, met name door een afname van het aantal met T. cruzi geïnfecteerde mensen. Dit is het effect van langlopende beheersprogramma’s in meerdere Zuid-Amerikaanse landen, die gericht zijn op bestrijding van de roofwantsen op het platteland, betere huisvesting en het systematisch screenen van bloeddonoren op een infectie met T. cruzi. Echter, de migratie van patiënten die geïnfecteerd zijn met T. cruzi uit Latijns-Amerikaanse landen naar andere, niet-endemische gebieden, heeft ertoe geleid dat de ziekte van Chagas nu ook in andere landen bij grotere groepen mensen gezien wordt. In de Verenigde Staten verblijven naar schatting 300.000 en in Europa 80.000 – 120.000 migranten uit Latijns-Amerika met de ziekte van Chagas. (7) De prevalentie van de ziekte van Chagas onder Latijns-Amerikaanse migranten in Europa is naar schatting 4,2% (95% CI 2,2-5,6), met de hoogste prevalenties bij migranten uit Bolivia (18,1%) en Paraguay (5,5%). (1) In Europa zijn in Spanje de meeste immigranten met de ziekte van Chagas, naar schatting 42.000, waarvan 25.000 vrouwen in de vruchtbare leeftijd. (9)
In Nederland is de grootste migrantengroep afkomstig uit Latijns-Amerika van Surinaamse afkomst. Het is onbekend wat de prevalentie van de ziekte van Chagas onder de Surinaamse bevolking is. In een publicatie van de Pan American Health Organization (PAHO) uit 2006 wordt de prevalentie in Suriname op 1,3% geschat (10) maar waarschijnlijk is de werkelijke prevalentie lager. (2) De prevalentie in de binnenlanden wordt op 0,7% geschat, en langs de kust van Suriname op nagenoeg 0%.Het totaal aantal seropositieve mensen in Nederland, gebaseerd op het aantal migranten uit Latijns-Amerika, werd in 2011 geschat op 726. In het Amsterdam Medisch Centrum wordt jaarlijks ongeveer 1 nieuwe patiënt met de ziekte van Chagas gediagnosticeerd. (2, 11)
In tegenstelling tot Latijns-Amerikaanse landen is er in Europa geen natuurlijke vector voor transmissie van T. cruzi naar de mens, de roofwants komt hier namelijk niet voor, de ziekte kan dan ook niet endemisch worden.
Diagnostiek
In de acute fase van de infectie is de parasitaemie hoog. Met microscopisch onderzoek kan de parasiet in het bloed aangetoond worden. Het DNA van de parasiet kan worden aangetoond met een PCR-test (polymerase chain reaction). In de hierop volgende chronische fase van de ziekte is de parasitaemie zeer laag. De sensitiviteit van microscopie is dan ontoereikend. De PCR kan positief zijn, maar is regelmatig ook negatief. De hoeksteen van de diagnostiek voor de chronische fase van de ziekte van Chagas is het gebruik van serologie, waarbij specifieke IgG-antistoffen tegen T. cruzi aangetoond worden. Een positieve uitslag wordt gebaseerd op IgG tegen verschillende T.cruzi-antigenen, aangetoond met tenminste 2 serologische testen met verschillende antigenen. (1) De duur totdat serologie negatief wordt na infectie is proportioneel aan de duur van infectie. Bij een chronische infectie van tientallen jaren, kan het dus tientallen jaren duren voordat serologie negatief wordt na behandeling. (12)
Therapie
Voor de therapie van de ziekte van Chagas zijn 2 geneesmiddelen in gebruik: benznidazol en nifortimox. Beide antiparasitaire middelen zijn in Nederland niet geregistreerd en alleen verkrijgbaar via de WHO of de Braziliaanse overheid. (2) In de acute fase van de infectie en bij pasgeboren congenitaal geïnfecteerde kinderen (zie onder) heeft deze therapie een effectiviteit tot 100%. Medicamenteuze behandeling van patiënten met chronische Chagas is minder effectief met een effectiviteit variërend van 60% – 93% bij kinderen jonger dan 14 jaar, tot 2 – 40% bij volwassenen. (1)
Onderzoek naar de ziekte van Chagas bij zwangere vrouwen en pasgeboren baby’s
De belangrijkste reden voor het uitvoeren van screening op Chagas bij zwangere vrouwen in landen waar de ziekte endemisch is, is het voorkómen van een chronische infectie bij het kind. De onomkeerbare cardiale en/of gastro-intestinale afwijkingen op latere leeftijd geven veel ziektelast over een lange periode. Daarnaast is behandeling effectiever naarmate de leeftijd op het moment van infectie, lager is. (1) Ook geeft behandeling op lagere leeftijd minder bijwerkingen dan behandeling op hogere leeftijd. (4) Als een zwangere vrouw gediagnosticeerd wordt met de ziekte van Chagas, is het advies om onderzoek te doen bij eventuele andere kinderen in het gezin, waardoor ook voor hen vroegtijdige en veelal effectieve behandeling mogelijk wordt.
Wanneer bij een zwangere vrouw serologisch wordt vastgesteld dat zij de ziekte van Chagas heeft, moet bij het kind na de geboorte onderzocht worden of er verticale transmissie van de parasiet heeft plaatsgevonden. Een recent voorstel voor diagnostische follow-up na de geboorte (4) bestaat uit het testen van het bloed van het kind 1 maand na de geboorte met microscopie en PCR op T. cruzi. Na 9 en eventueel 12 maanden, wordt serologisch onderzoek op Chagas uitgevoerd. Als na 9 en/of 12 maanden geen antistoffen tegen T. cruzi meer gevonden worden, heeft het kind zeker geen congenitale Chagas. In het eerste levensjaar kunnen nog maternale antistoffen in het bloed aanwezig zijn. Als microscopie, PCR en/of serologisch onderzoek positief zijn, is er sprake van een congenitale infectie. In dit geval wordt dan ook meteen gestart met behandeling. In sommige gevallen is dit dus na 12 maanden, als zeker is dat maternale antistoffen verdwenen zijn.
Screeningsprogramma’s naar de ziekte van Chagas bij zwangere vrouwen in Latijns-Amerika en Europa
In Latijns-Amerikaanse landen waar de ziekte endemisch voorkomt, wordt door de overheid screening naar de ziekte van Chagas aangeboden aan alle zwangere vrouwen.In sommige Europese landen, zoals Italië, Spanje en Zwitserland waar veel immigranten uit Latijns-Amerika komen, zijn sinds de jaren ’90 van de vorige eeuw voor zwangere vrouwen uit risicogebieden ook screeningsprogramma’s naar de ziekte van Chagas gestart. (4, 7) In Spanje werden in screeningsprogramma’s bij zwangere vrouwen van Latijns-Amerikaanse origine, seroprevalenties voor de ziekte van Chagas gevonden variërend van 3% tot 16% (3), en een verticale transmissie naar het kind van 7%. (4) De hoogste prevalenties werden gevonden bij zwangere vrouwen van Boliviaanse origine. (7) In de Europese landen waar screening plaats vindt, is het programma vaak niet landelijk dekkend en wordt het uitgevoerd in enkele grote centra.
Antwoord op de vraag van de verloskundige
De verloskundige is door de GGD geadviseerd om het bloed van de zwangere vrouw serologisch te laten testen op T. cruzi-antistoffen. In Brazilië is de seroprevalentie gemiddeld 0,03% (8), maar in sommige delen van het land, en afhankelijk van leeftijd is dit hoger. Aangezien de kans op transmissie naar het kind bij seropositiviteit van de moeder ongeveer 5% is, is de kans op besmetting in dit geval klein. Gezien het potentiële gevaar voor het kind adviseerde de GGD desondanks aan de verloskundige om de moeder te laten testen op specifieke antistoffen voor de ziekte van Chagas. De zwangere vrouw was negatief voor T.Cruzi-antistoffen.
De diagnostische interventie is relatief eenvoudig, goedkoop, schept meer duidelijkheid (en geruststelling) naar de zwangere vrouw en er is een handelingsperspectief bij dragerschap. Verloskundigen worden daarom geadviseerd om bij zwangere vrouwen die geboren en/of meerdere jaren gewoond hebben in Latijns Amerika, de ziekte van Chagas te benoemen. Mogelijk heeft de zwangere vrouw zelf al ervan gehoord of vragen erover. De GGD is bereikbaar voor advies. Afhankelijk van het land van herkomst of het specifieke gebied en ongerustheid bij de zwangere vrouw, kan het advies zijn om screening voor de ziekte van Chagas in te zetten.
Een LCI-richtlijn (Landelijke Coördinatie Infectieziektebestrijding/RIVM) over deze ziekte bestaat vooralsnog niet. Gezien de grotere migratiestromen in Europa vanuit Latijns-Amerika in de afgelopen decennia, wordt kennis over dit ziektebeeld wel relevanter en zijn voornamelijk heldere criteria over screeningsbeleid bij zwangere vrouwen, wenselijk.
In Nederland is het Academisch Medisch Centrum in Amsterdam gespecialiseerd in de diagnostiek en behandeling van patiënten met de ziekte van Chagas. Voor diagnostiek wordt naar dit laboratorium verwezen.
Auteurs
A.D. Hintaran1, J. Pattipeilohy1, E.Fanoy1,4, T. Kortbeek2, T. van Gool3
- GGD regio Utrecht
- Rijksinstituut voor Volksgezondheid en Milieu, Bilthoven
- Academisch Medisch Centrum, Amsterdam
- GGD Rotterdam-Rijnmond
Correspondentie
Literatuur
- Perez-Molina JA, Molina I. Chagas disease. Lancet (London, England). 2017.
- Bart A, Hodiamont CJ, Grobusch MP, van den Brink RB, Smout AJ, van Gool T. [Chagas disease in the Netherlands: an estimate of the number of patients]. Ned Tijdschr Geneeskd. 2011;155:A3170.
- Antinori S, Galimberti L, Bianco R, Grande R, Galli M, Corbellino M. Chagas disease in Europe: A review for the internist in the globalized world. European journal of internal medicine. 2017.
- Abras A, Munoz C, Ballart C, Berenguer P, Llovet T, Herrero M, et al. Towards a New Strategy for Diagnosis of Congenital Trypanosoma cruzi Infection. Journal of clinical microbiology. 2017;55(5):1396-407.
- Gourbiere S, Dorn P, Tripet F, Dumonteil E. Genetics and evolution of triatomines: from phylogeny to vector control. Heredity. 2012;108(3):190-202.
- Rozendaal JA. Chapter 3 Triatomine bugs. Vector control: methods for use by individuals and communities: WHO Library Cataloguing in Publication Data; 1997.
- Soriano-Arandes A, Angheben A, Serre-Delcor N, Trevino-Maruri B, Gomez IPJ, Jackson Y. Control and management of congenital Chagas disease in Europe and other non-endemic countries: current policies and practices. Tropical medicine & international health : TM & IH. 2016;21(5):590-6.
- Chagas disease in Latin America: an epidemiological update based on 2010 estimates. Releve epidemiologique hebdomadaire. 2015;90(6):33-43.
- Perez-Molina JA, Perez AM, Norman FF, Monge-Maillo B, Lopez-Velez R. Old and new challenges in Chagas disease. The Lancet Infectious diseases. 2015;15(11):1347-56.
- Jannin J, Salvatella R. Estimación cuantitativa de la enfermedad de Chagas en las Américas. Montevideo, Uruguay. : Organización Panemericana de la Salud 2006 Contract No.: OPS/HDM/CD/425-06.
- Bart A, Hodiamont C, Grobusch M, Brink Rvd, Smout A, Gool Tv. De ziekte van Chagas in Nederland: een schatting van het aantal patiënten. Ned Tijdschr Geneeskd. 2011;155(A3170).
- Fabbro DL, Danesi E, Olivera V, Codebo MO, Denner S, Heredia C, et al. Trypanocide treatment of women infected with Trypanosoma cruzi and its effect on preventing congenital Chagas. PLoS neglected tropical diseases. 2014;8(11):e3312.
Infectieziekten Bulletin, jaargang 29, nummer 4, april 2018
Zwanger, contact met waterpokken en geen antistoftiter, wat nu?
Een GGD belt over een vrouw die 32 weken zwanger is en een zoontje heeft met waterpokken. De vrouw zegt dat zij waterpokken heeft gehad toen ze ongeveer 6 maanden oud was. De verloskundige heeft naar aanleiding daarvan een titerbepaling voor waterpokken laten uitvoeren. De IgG was positief maar was volgens de microbioloog te laag en niet beschermend. Vraag van de GGD: kan het zijn dat de titer is weggezakt zoals dat ook bij rodehond wordt gezien? Is mevrouw toch beschermd? Moeten er wel of geen antistoffen gegeven worden?
Zwanger, contact met waterpokken en geen antistoftiter, wat nu?
Waterpokken
Waterpokken is een zeer besmettelijke meestal mild verlopende kinderziekte die gepaard gaat met blaasjes op de huid en jeuk. Vrijwel alle kinderen in Nederland (96%-99 %) maken de ziekte door. Waterpokken worden veroorzaakt door het varicellazostervirus. Het virus wordt verspreid door de lucht (door uitgehoeste vochtdruppeltjes) of door direct contact met de blaasjes. De incubatietijd (de tijd tussen het moment van besmetting en het ontstaan van de eerste blaasjes) is 2 tot 3 weken. De patiënt is besmettelijk vanaf 2 dagen voor het ontstaan van de blaasjes tot het moment dat alle blaasjes ingedroogd zijn. Dat is bij overigens gezonde personen binnen 7 dagen na het ontstaan van de blaasjes. Het varicellazostervirus is hetzelfde virus dat gordelroos (herpes zoster) veroorzaakt op latere leeftijd.
Waterpokken en zwangerschap
Op de RIVM website Zwangerschap en waterpokken is te lezen dat een waterpokkeninfectie in de zwangerschap een verhoogd risico op complicaties geeft voor moeder en kind. In de eerste plaats is er risico op ernstige complicaties, zoals varicellapneumonie, voor de zwangere vrouw zelf. Voor het ongeboren kind is er een klein risico op vroeggeboorte en tot een zwangerschapsduur van 24 weken is er een risico op congenitaal varicellasyndroom (CVS). Tot slot is er risico voor de pasgeborene. Als de moeder rondom de bevalling waterpokken doormaakt kan het kind een ernstig verlopende infectie doormaken. Als de pasgeborene besmet wordt door anderen dan de eigen moeder verloopt een infectie minder ernstig.
Wat nu?
In theorie kan de titer weggezakt zijn, maar omdat de vrouw zo jong waterpokken heeft gehad, is het waarschijnlijker dat ze toen nog maternale antistoffen had en daarom nooit een goede titer heeft opgebouwd.Om alle risico’s te vermijden is het advies om in deze situatie de vrouw passief te immuniseren met immuunglobulinen. Dit is zinvol tot 96 uur na het eerste risicocontact.
Auteur
T. Oomen, Centrum Infectieziektebestrijding, RIVM, Bilthoven
Correspondentie
Literatuur
- LCI-richtlijn Waterpokken en gordelroos
- RIVM webpagina Zwangerschap en waterpokken
- NVMM-richtlijn Varicella 2010
Registratie infectieziekten
Wet publieke gezondheid
De meldingen Wet publieke gezondheid tot en met week 12, 2018
Virologische weekstaten
De meldingen in de virologische weekstaten tot en met week 12, 2018