Infectieziekten Bulletin
November 2019 | Jaargang 30, nummer 6
https://magazines.rivm.nl/2019/11/infectieziekten-bulletin-0
Gesignaleerd
Binnenlandse signalen
Clustering van patiënten met listeriose
In oktober is met whole genome sequencing (WGS) een cluster van 20 patiënten met listeriose aangetoond. Een patiënte kreeg hierdoor een miskraam en 3 patiënten overleden. Dit cluster was er al in het najaar van 2018 en bestond toen uit 7 patiënten. Zij waren gelinkt aan 1 routinematig getest voedselisolaat waarvan het kiemgetal (kve) onder de wettelijk toegestane norm van 2017 lag. Op basis van de gegevens van de patiënten kon geen bron worden aangetoond. En omdat er niet meer patiënten bij kwamen is verder geen onderzoek gedaan. Op 31 juli 2019 werd duidelijk dat het aantal patiënten in het cluster steeg. De Nederlandse Voedsel- en Warenautoriteit (NVWA) werd op de hoogte gebracht van dit cluster met dit voedselisolaat en startte met onderzoek naar de herkomst van het voedselisolaat. Dat bleek een vleesverwerkingsbedrijf te zijn waar vleeswaren worden gesneden. De NVWA nam omgevings- en productmonsters en kon met WGS een match aantonen tussen recente voedselisolaten van deze productielocatie en de humane isolaten. De productie van vleeswaren werd stilgezet en de producten zijn uit de handel gehaald. Ze werden via verscheidene supermarktketens, zorginstellingen en bedrijfskantines aan consumenten aangeboden. Daarnaast werden ook vleeswaren geleverd aan groothandels en luchtvaartcatering. Supermarktketens waar de producten verkocht werden, hebben een veiligheidswaarschuwing uitgedaan en consumenten opgeroepen de producten niet te consumeren en te retourneren.
Listeria monocytogenes is een bacterie die overal in het milieu voorkomt en ook onder ongunstige omstandigheden, zoals droogte en lage temperaturen, kan overleven of zelfs groeien. De bacterie komt vooral voor in rauwe voeding en producten die lang in de koelkast hebben gelegen. Ouderen, mensen met een lage weerstand en pasgeboren baby’s lopen het grootste risico op een symptomatische infectie. Listeriose wordt gekenmerkt door onder andere gastro-enteritis, maar kan ook sepsis en meningitis veroorzaken. Infectie bij zwangere vrouwen, met name in de tweede helft van de zwangerschap, kan leiden tot intra-uteriene vruchtdood en vroeggeboorte. (Zie https://www.rivm.nl/listeriose/listeriose-en-zwangerschap en https://www.nhg.org/actueel/nieuws/listeriose-door-vleeswaren). Listeriose komt zelden voor (gemiddeld 85 meldingen per jaar in de afgelopen 10 jaar) en de risico’s zijn klein. (Bronnen: NVWA, RIVM)
Meer bofmeldingen dan in afgelopen 5 jaar
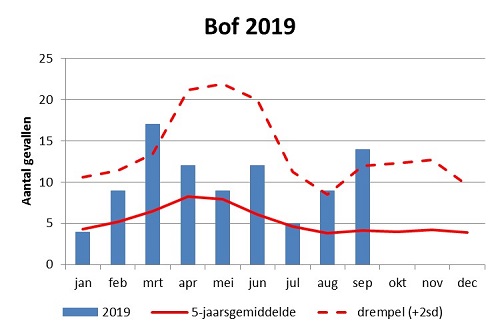
In 2019 zijn tot 9 oktober 91 patiënten met bof gemeld. Dit is meer dan in dezelfde periode in de afgelopen 5 jaar waarin het aantal varieerde tussen 38 en 83 (gemiddeld 51). Het aantal patiënten dat in september ziek werd lag boven de drempelwaarde van het 5-jaarsgemiddelde (zie figuur 1). In maart was dit ook het geval door een bofcluster onder studenten met 9 patiënten. In september en begin oktober waren er voornamelijk meldingen van solitaire bofvirusinfecties. In totaal zijn er t/m 9 oktober 6 clusters waargenomen met in totaal 25 patiënten (2 tot 9 patiënten per cluster) in verschillende GGD regio’s. Ruim de helft van de patiënten (56%) is tussen 15 en 29 jaar oud, een kwart tussen 30 en 39 jaar. De gemiddelde leeftijd van de patiënten in 2019 is, net als in 2018, 28 jaar en is daarmee gestegen ten opzichte van de periode 2010 -2012. Toen waren er bofuitbraken onder studenten met een gemiddelde leeftijd van 23 jaar. Ongeveer de helft van de patiënten in 2019 is student of heeft contact met studenten, variërend van 78% van de leeftijdsgroep 15-19 jaar tot 15% van degenen van 30 jaar en ouder. Van de 73 patiënten die zijn geboren vanaf 1983 (toen BMR-vaccinatie in het Rijksvaccinatieprogramma (RVP) werd aangeboden) en een bekende vaccinatiestatus hadden, was 90% gevaccineerd; de meesten 2 keer. Van de 9 patiënten met complicaties hadden er 8 orchitis, van hen was 25% gevaccineerd. Van de 54 patiënten bij wie het genotype bepaald was, had 93% genotype G. De meeste gevallen van bof in Nederland (en uitbraken in andere Europese landen) worden sinds 2010 veroorzaakt door genotype G. (Bronnen: RIVM)
Figuur 1. Aantal bofmeldingen per maand van 1e ziektedag in 2019 en gemiddeld in 2014-2018. Peildatum 9 oktober 2019
Uitbraak van mazelen op Urk is afgelopen
De uitbraak van mazelen op Urk, met melding van de eerste patiënt op 7 juni, was begin oktober volgens alle beschikbare gegevens afgelopen. In totaal werden 32 patiënten met mazelen gemeld in deze uitbraak (waarvan 20 met een laboratoriumbevestigde diagnose). Hiervan was 53% man, 72% geboren na of in het jaar voorafgaand aan de laatste epidemie in 2013 en 91% was ongevaccineerd. Geen van de patiënten werd opgenomen in het ziekenhuis. Bij 2 patiënten werd een complicatie gemeld (pneumonie en otitis media). De meeste patiënten kwamen uit Urk en omgeving. Vier patiënten woonden niet op Urk maar hadden een epidemiologische link. Bij 18 patiënten werd genotype D8 vastgesteld, met een sequentie die bij veel recente mazelengevallen in Nederland en andere (Europese) landen is aangetoond. De eerste ziektedag van de laatste patiënt was op 26 augustus. Dat betekent dat de incubatietijd van mazelen inmiddels 2 keer is verlopen zonder dat er nieuwe patiënten bij zijn gekomen. GGD Flevoland bevestigt dat op basis van contact met lokale huisartsen en basisscholen er geen nieuwe patiënten meer zijn. Met het eindigen van de uitbraak is ook de maatregel van het lokaal aanbieden van een vervroegde BMR-vaccinatie komen te vervallen. (Bronnen: RIVM, GGD Flevoland)
Opnieuw autochtone tekenencefalitis in het oosten van Nederland
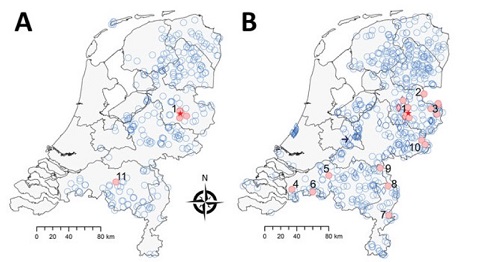
Recent is bij een tweede patiënt autochtone tekenencefalitis vastgesteld op basis van positieve serologie voor tick-borne encefalitisvirus (TBEV). Dit werd bevestigd met virusneutralisatie. Eerder berichtten we over teken, reeën en andere patiënten waarbij TBEV werd vastgesteld (zie figuur 2). Deze tweede patiënt met autochtone TBE dit jaar, werd mogelijk besmet in de provincie Gelderland, ten zuiden van het bekende endemische gebied op de Sallandse Heuvelrug. Hij had een bifasisch ziektebeloop en was in de 6 weken voor de eerste ziektedag niet in het buitenland geweest. De patiënt bevestigde dat hij meerdere tekenbeten had opgelopen voorafgaand aan de eerste ziektedag in juni van dit jaar. De patiënt had zich gemeld met neurologische klachten waardoor een verdenking bestond op neuroborreliose. Het serum van de patiënt was positief voor borrelia-antistoffen, maar de liquor testte negatief. De patiënt werd niettemin behandeld met antibiotica voor neuroborreliose. Omdat de neurologische klachten aanhielden, is alsnog diagnostiek naar tekenencefalitis ingezet. De diagnose TBE werd 14 weken na de eerste ziektedag gesteld. Deze casus illustreert dat clinici en artsen-microbiologen alert moeten zijn op tekenencefalitis bij patiënten die passende neurologische klachten hebben; ook als zij niet in gebieden zijn geweest waar TBEV endemisch is. (Bronnen: GGD Noord- en Oost-Gelderland, RIVM, EID_2019_Rijks et al.)
Figuur 2. Voorkomen van TBEV gebaseerd op serosurveillance in reeën in Nederland gedurende A:2010 en B:2017. Rode stip: positief monster in de TBEV-virusneutralisatietest, blauwe cirkel: negatief testresultaat in deze test of de ELISA. Rode ster: locatie van in 2016 positieve teken voor TBEV. Cirkels en ruiten geven respectievelijk random en doelgerichte plaatsen van sampling aan. De pijl in de rechterkaart geeft de locatie van het Nationaal Park de Utrechtse Heuvelrug aan. Getallen geven bevestigde of mogelijk foci aan. (Bron: CDC_EID2019_Rijks et al.)
Buitenlandse signalen
Eerste autochtone zikavirusinfecties in Europa
In Hyères (departement Var, Frankrijk) is voor het eerst in Europa bij een patiënt een autochtone zikavirusinfectie aangetoond. De diagnose werd begin oktober bevestigd door het Franse nationale referentielaboratorium voor arbovirussen. De risicobeoordeling door het European Centre for Disease Prevention and Control (ECDC) gaat ervan uit dat het zikavirus door een muggenbeet werd overgedragen; er zijn geen aanwijzingen dat de patiënt de ziekte in het buitenland heeft opgelopen of via seksueel contact. Tijdens een buurtonderzoek werd nog een patiënt met een autochtone zikavirusinfectie gevonden. Hij was ook niet in het buitenland geweest en woonde in dezelfde wijk als de eerste patiënt. Beide patiënten zijn inmiddels hersteld. Deze tweede casus versterkt de hypothese van de overdracht van zikavirus door muggen, hoogstwaarschijnlijk door de muggensoort Aedes albopictus. De 2 patiënten waren slechts enkele dagen na elkaar ziek geworden. Daarmee lijkt het waarschijnlijk dat zij tot dezelfde overdrachtscyclus behoren. De Franse autoriteiten doen aanvullend epidemiologisch en entomologisch onderzoek om andere mogelijke patiënten op te sporen en deze lokale overdracht beter in kaart te brengen. Er zijn maatregelen genomen om de muggen te bestrijden om verdere transmissie te voorkomen. Er is nog geen patiënt gevonden die, na zelf te zijn besmet in het buitenland, mogelijk de besmettingsbron is van deze 2 autochtone infecties.
Het aantal reizigers dat besmet met zikavirus naar Europa komt, is sterk afgenomen van meer dan 2000 in 2016 naar minder dan 20 in 2019. Incidenteel raken mensen besmet door seksueel contact of door verticale transmissie van moeder naar kind. De belangrijkste vector van het zikavirus, de muggensoort Aedes aegypti, komt voor in gebieden in Midden-, Noord- en Zuid-Amerika (inclusief het Caribisch gebied). Daar was een epidemie met een piek in 2016. In delen van continentaal Europa komen de muggensoorten Aedes albopictus (de tijgermug) en Aedes japonicus voor, die volgens laboratoriumstudies ook zikavirus kunnen overdragen, maar minder succesvol zijn dan Aedes aegypti. Ondanks de import van zikavirus via terugkerende reizigers naar Europa, was er tot dusverre geen autochtone transmissie via muggen vastgesteld, zoals wel het geval is voor denguevirus en chikungunyavirus. Het risico om een zikavirusinfectie op te lopen in de directe omgeving van Hyères voor lokale bevolking of reizigers wordt niettemin als zeer laag ingeschat. (Bronnen: ECDC, RIVM, l'Agence régionale de santé de Provence-Alpes-Côte d'Azur (l’ARS PACA), ECDC, ECDC-RRA, media-1, media-2)
Westnijlvirusinfecties bij patiënten in Duitsland
Voor het eerst zijn in Duitsland bij 3 patiënten autochtone Westnijlvirus (WNV)-infecties vastgesteld. De patiënten bij wie de infecties met laboratoriumonderzoek werden bevestigd, kwamen uit het oosten van Duitsland (uit Saksen, Saksen-Anhalt en uit Berlijn), waar circulatie van WNV in vogels bekend is. In Duitsland zijn dit jaar t/m 25 oktober 27 paarden en 53 vogels met WNV geregistreerd, voornamelijk in het oosten van Duitsland, en bij Hamburg. In 2018 werd het WNV voor het eerst gesignaleerd bij vogels en paarden in het oosten van Duitsland Dit wijst erop dat het virus endemisch is in dat gebied. Tot en met 24 oktober zijn er dit jaar in Europa 441 patiënten met WNV-infecties gemeld, voornamelijk in Griekenland, Roemenië, Italië, Hongarije en Cyprus. Hiervan zijn 44 patiënten overleden. Verder zijn er 77 uitbraken onder paarden gemeld, in Griekenland, Duitsland, Italië, Frankrijk, Hongarije, Oostenrijk, Spanje en Portugal.WNV wordt vooral door de muggensoort van het geslacht Culex verspreid. Deze soort komt in heel Nederland voor. Het virus vermeerdert zich in vogels. Ook paarden en mensen kunnen besmet worden, maar zij zijn eindgastheren en dragen niet bij aan verdere verspreiding via muggen. Bij mensen en paarden verloopt de infectie veelal zonder klinische symptomen. Ongeveer 10-20% van de besmettingen bij mensen leidt tot griepachtige ziekteverschijnselen en bij ongeveer 1% verloopt de ziekte zeer ernstig. Het transmissieseizoen voor WNV in Europa loopt doorgaans van juni tot november. Bronnen: RKI, Fli, ECDC, Ziegler et al, 2019.
Patiënten met autochtone dengue in Spanje en Frankrijk
Het ECDC heeft een risicobeoordeling uitgebracht over enkele patiënten uit Frankrijk en Spanje met autochtone dengue.
Spanje
- De eerste patiënt van dit seizoen werd gemeld op 16 september door de Catalaanse gezondheidsautoriteiten. De patiënt kwam uit Barcelona en de diagnose was bevestigd met laboratoriumonderzoek . Hij had geen relevante reisgeschiedenis.
Frankrijk
- De gezondheidsautoriteiten van Frankrijk rapporteerden op 20 september een patiënt met autochtone Dengue uit Vallauris (departement Alpes-Maritimes). Zijn diagnose was ook bevestigd met laboratoriumonderzoek. Hij was ziek geworden op 30 augustus en had ook geen relevante reisgeschiedenis. Door deur-aan-deuronderzoek rondom het huis van de patiënt werden nog 4 patiënten gevonden, waarvan 3 met serologisch onderzoek positief testten en 1 PCR-positief was. Ook werd een patiënt ontdekt die wel besmet was geraakt in het buitenland. Hij was een hoogstwaarschijnlijk de indexpatiënt van dit cluster.
- Uit Caluire-et-Cuire, een buitenwijk van de stad Lyon, werd een patiënt gemeld met een vermoedelijk autochtone infectie Hij was ziek geworden op 14 juli en ook hij had geen relevante reisgeschiedenis. Met epidemiologisch onderzoek kon een andere patiënt aangetoond worden die besmet was geraakt in het buitenland en ziek was geworden op 30 juni. Deze patiënt woonde vlak bij de andere patiënt.
Er is voor zover bekend geen epidemiologische link tussen deze 3 (clusters van) patiënten. Verder epidemiologisch en entomologisch onderzoek is gaande. Er wordt actief gezocht naar patiënten in gebieden met mogelijke transmissie. Sporadische gevallen of kleine clusters van autochtone dengue in het Middellandse Zeegebied en zuidelijke delen van EU/EER landen zijn in de zomer en herfst niet onverwacht, omdat de Aziatische tijgermug (Aedes albopictus) in het gebied aanwezig is. De kans op doorgaande transmissie van het denguevirus is echter zeer laag, mede vanwege de weersomstandigheden die naar verwachting in de komende weken een ongunstige invloed zullen hebben op de het aantal tijgermuggen. Autochtone denguebesmettingen zijn eerder gedocumenteerd in Zuid-Frankrijk (2010, 2013, 2014, 2015 en 2018) en Spanje (2018). (Bron: ECDC RRA)
Legionella-uitbraak onder bezoekers van een landbouwbeurs in de Verenigde Staten
In de Amerikaanse staat North Carolina was een grote uitbraak van legionellose onder bezoekers van een 10-daagse landbouwbeurs. De beurs werd gehouden in Fletcher van 6 tot 15 september. Er waren ongeveer 170.000 bezoekers. Er zijn tot dusver 134 patiënten gemeld met een legionellapneumonie, waarvan 4 zijn overleden, en 8 patiënten met Pontiac fever. De gemiddelde leeftijd van de patiënten is 61 jaar (24 – 91 jaar) en 58% is man. Eerste ziektedagen varieerden van 13 tot en met 27 september. De mogelijke bronnen van besmetting zijn watervernevelingsinstallaties, waaronder bubbelbaden, een luchtbevochtiger en een koelventilator buiten het gebouw. Deze werden pas 12 tot 22 dagen na afloop van de beurs bemonsterd. Het onderzoek leverde geen match op met de humane isolaten. Toch wijst epidemiologisch onderzoek naar de bubbelbad(en) als de meest waarschijnlijke bron. Bezoekers die de beurs bezochten, met name tijdens de laatste 5 dagen van de beurs, en die meer dan 1 uur in het gebouw met de baden doorbrachten, hadden het grootste risico om legionellose op te lopen. Bubbelbaden zijn een bekende bron van legionellose en zijn vaker in verband gebracht met grote puntbronuitbraken. In warm water kan Legionella snel uitgroeien, terwijl het doorblazen met lucht leidt tot de vorming van aerosolen. Daarbij raken niet alleen de mensen in bad besmet, maar ook degenen in de omgeving van het bubbelbad.
De uitbraak in North Carolina lijkt qua omgeving en vermoedelijke besmettingsbron op de legionella-uitbraak in 1999 onder bezoekers van een grote overdekte bloemententoonstelling in Bovenkarspel. Ondanks de uitbraak in Bovenkarspel is er in Nederland nog geen landelijke regelgeving voor legionellapreventie bij evenementen. Wel is regelgeving op lokaal niveau mogelijk, bijvoorbeeld in de algemene plaatselijke verordening of evenementenvergunning. (Bronnen: NCDHHS, media-1,media-2, den Boer et al. EID (2002))
Auteur
S. Mooij, Centrum Infectieziektebestrijding, Rijksinstituut voor Volksgezondheid en Milieu, Bilthoven
Correspondentie
Infectieziekten Bulletin, jaargang 30, nummer 6, november 2019
Een schoolvoorbeeld van noro
Situatiebeschrijving
Op woensdag 28 augustus belde een directeur van een kleine basisschool naar de afdeling Infectieziektebestrijding van GGD Groningen om te melden dat er 33 kinderen en 4 leerkrachten ziek waren met klachten van diarree en braken. Op de school zitten 98 kinderen en er werken 12 leerkrachten en andere medewerkers..
Tijdens het telefoongesprek werd de verpleegkundige geïnformeerd over het aantal zieken, de eerste ziektedag, diagnostiek, mogelijke besmettingsbronnen, of er al maatregelen waren genomen en zo ja, welke? De directeur vertelde dat er op de eerste dag na de zomervakantie in de aula van de school een feestelijke opening was geweest voor alle leerlingen en leerkrachten. Met ranja en koekjes, gekocht in een winkel. In het klaslokaal van groep 3/4 had vlak voor de feestelijke opening een kind gebraakt. Vanaf maandagavond op dinsdag waren veel kinderen en leerkrachten ziek geworden met klachten van braken en diarree. De directeur maakte zich zorgen en vroeg zich af wat ze kon doen.
| Groep | Aantal kinderen | Aantal zieke kinderen |
|---|---|---|
| 1/2 | 27 | onbekend omdat de kleuters vrij zijn op woensdag |
| 3/4 | 23 | 15 |
| 5/6 | 23 | 9 |
| 7/8 | 25 | 9 |
Nadat ze de melding had geregistreerd sprak de verpleegkundige met de directeur af om later op de ochtend terug te bellen en maatregelen te bespreken. Echter, na overleg op de GGD tussen de verpleegkundige, de arts infectieziektebestrijding en de deskundige infectiepreventie, werd besloten dat het wenselijk was dat de GGD nog dezelfde middag de school zou bezoeken. Vanwege het grote aantal zieken. De verpleegkundige en de deskundige infectiepreventie gingen daarop naar de school en hadden 5 testkits voor fecesdiagnostiek bij zich, om uit te delen aan de ouders van de zieke kinderen.
Op school spraken zij met 2 leerkrachten die niet ziek waren. Eén leerkracht was de bewuste maandag niet op school geweest, De andere wel, maar die had geen koekjes en ranja gehad. De combinatie van braken en diarree en ranja en koekjes deed vermoeden dat norovirus de oorzaak was en de ranja en koekjes de bronnen van besmetting. Ook zou aerogene verspreiding op school een rol kunnen hebben gespeeld. Want de moeder van het kind dat had overgegeven, had het braaksel opgeruimd met handdoeken, die zij vervolgens in de wasmand in de keuken van de school had gestopt. Daarna was zij gaan helpen met het klaar zetten van de ranja en koekjes. De GGD ging ook kijken in de keuken en de Uit de inspectie van de keuken en het sanitair bleek dat in de toiletten voor de leerlingen flacons met vloeibare zeep stonden en papieren handdoekjes lagen en in het toilet voor de leerkrachten hing een handdoek. In de keuken stond een open wasmand voor de vuile was.
Diagnostiek
Vanwege het vermoeden van de GGD dat het om besmetting met norovirus ging, waren tijdens het bezoek van de GGD 5 testkits voor diagnostiek uitgedeeld aan ouders. Het lukte de ouders echter niet om fecesmonsters op te vangen omdat de kinderen vooral moesten braken en geen diarree hadden. In overleg met het laboratorium mocht toen ook braaksel opgestuurd worden voor onderzoek. Alle 5 bij het laboratorium ingeleverde monsters bleken positief voor norovirus. Op donderdag waren 50 leerlingen, 4 leraren en de directeur ziek.
Maatregelen
Op basis van het bezoek aan de school adviseerde de GGD de volgende maatregelen:
- Zieke leerlingen moeten thuisblijven, om verdere verspreiding van norovirus op school te voorkomen. De leerlingen mogen 24 uur nadat zij zijn hersteld weer naar school.
- De ouders worden per mail geïnformeerd over de uitbraak en krijgen daarbij advies over te nemen hygiënemaatregelen.
- Zolang de uitbraak duurt mogen kinderen niet trakteren. Zelfgemaakte traktaties (door mogelijk zieke kinderen/ ouders) zouden dan weer een besmettingsbron kunnen worden.
- Het bedrijf dat de school schoonmaakt heeft uitleg en instructies gekregen van de deskundige infectiepreventie over het extra reinigen en desinfecteren van hoogrisico- oppervlakken zoals deurknoppen, toiletten en de keuken. Dit moet dagelijks gebeuren tijdens de uitbraak, tot 3 dagen daarna.
- De mand met vuile was mag niet meer in de keuken staan.
- Zowel de leerlingen als de leerkrachten moeten extra aandacht besteden aan handhygiëne: wassen met vloeibare zeep en drogen met papieren handdoekjes. Beide producten zijn al aanwezig in de toiletten
Conclusie
De GGD gaat ervan uit dat de koekjes en/of de ranja die op maandag werden uitgedeeld besmet zijn geraakt met norovirus, via de handen van de mensen die de traktaties hadden. klaargezet. Na 24 uur werden de eerste zieken gemeld en de uitbraak heeft 5 dagen geduurd. Degenen die wel op school waren maar geen ranja of koekjes hadden gegeten zijn niet ziek geworden. Daarentegen werden sommige ouders van zieke kinderen ook ziek en hadden daarbij dezelfde klachten. Na het weekend werden geen nieuwe patiënten meer gemeld en waren bijna alle leerlingen en leraren weer op school.
De school was erg blij met onze komst, want de uitbraak zorgde voor een onplezierige en onrustige start van het schooljaar. Door onze betrokkenheid, heldere informatie, duidelijke acties en uitleg over de verspreidingsweg en besmettingsbron, konden we ouders, leerlingen en leerkrachten gerust stellen. Daarom was ook iedereen bereid om de maatregelen in acht te nemen. Iedereen op school was zich bewust van het belang van goede hygiëne en in het bijzonder van goede handhygiëne, zeker bij het bereiden van voedsel. Wij zijn van mening dat dit niet zo goed gelukt zou zijn, als we alleen telefonisch contact met de school hadden gehad.
Auteur
T. Boersema, GGD Groningen
Correspondentie
trea.boersema@ggd.groningen.nl
Infectieziekten Bulletin, jaargang 30, nummer 6, november 2019
Fecesonderzoek bij contacten van shigellosepatiënten is te uitgebreid
Achtergrond
Gastro-enteritis veroorzaakt door Shigella is een veel voorkomende aandoening in de open populatie. Slechts een klein deel van de mensen met klachten gaat naar de huisarts. Meestal zal de huisarts geen laboratoriumdiagnostiek aanvragen (1,2). Een aanzienlijk aantal patiënten met vermoedelijk shigellose wordt dus niet bij de GGD gemeld. Desondanks komen in Nederland nauwelijks grote uitbraken voor. En in de leeftijdsgroep waar verspreiding het meest voorkomt, kinderen van 0-6 jaar, blijkt dat slechts 1 op de 4 een ander besmet. (3)
In de richtlijn Shigellose (2019) van de landelijke Coördinatie Infectieziektebestrijding (LCI) wordt aanbevolen om bij bepaalde contacten van de indexpatiënt fecesonderzoek te doen. Deze onderzoeken kosten de GGD veel tijd. Contacten moeten worden opgespoord en gemotiveerd om een fecesmonster in te sturen. De tijd die het duurt om het contact te spreken, om een fecesmonster te laten afnemen en om het fecesmonster op het laboratorium te krijgen, zijn van invloed op de uitslag. Hoe langer alles duurt, hoe kleiner de kans op een positieve kweekuitslag. Vooral bij fecesmonsters met een laag bacterieaantal zal het onderzoek resulteren in (mogelijk fout-)negatieve kweekuitslagen. Het is niet waarschijnlijk dat de factoren die vertraging veroorzaken geoptimaliseerd kunnen worden. Bovendien valt het te betwijfelen of optimalisatie invloed zal hebben op het aantal shigelloseclusters. De vraag is dus: Wat is de meerwaarde van fecesonderzoek bij contacten van patiënten met shigellose?
Methode
- Literatuuronderzoek naar de secundaire transmissie van Shigella in Nederland.
- Alle GGD’en kregen een vragenlijst over het proces van fecesonderzoek van contacten, en het aantal patiënten met shigellose en uitbraken in de afgelopen jaren in hun regio.
- 13 microbiologische laboratoria - 3 in academische centra, 4 huisartsenlaboratoria, 6 laboratoria in perifere ziekenhuizen - ontvingen een vragenlijst over de wijze waarop zij shigelladiagnostiek uitvoeren.
- Bij de GGD’en van Utrecht, Haaglanden, Rotterdam en Groningen zijn gegevens verzameld over 2016 en 2017 over het aantal contacten bij wie fecesonderzoek geïndiceerd was, hoe vaak het fecesmonster daadwerkelijk verstuurd is en wat de uitslagen van het onderzoek waren.
Resultaten
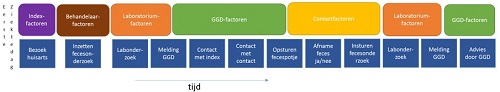
We hebben in kaart gebracht hoe het proces van contactonderzoek verloopt (figuur 1). Wat we over elk onderdeel van het proces tijdens het regioproject onderzocht hebben wordt hieronder besproken.
Figuur 1. Factoren van invloed op contactonderzoek Shigella. Klik hier om de afbeelding te vergroten
Indexpatiënt
Haagsma et al. hebben een surveillancepiramide voor Shigella opgesteld voor Nederland, op basis van data en modellering. (4) Hierbij gingen zij uit van de volgende gegevens:
- 8% van de mensen met niet-bloederige diarree bezoekt de huisarts,
- 31% van de mensen met bloederige diarree bezoekt de huisarts,
- 25% van de patiënten met shigellose heeft bloederige diarree.
Op basis van deze percentages en modellering concluderen Haagsma et al. dat gemiddeld 14% van de patiënten met shigellose de huisarts bezoekt. Na modellering schatten zij dat er per jaar in Nederland ongeveer 17.000 patiënten met shigellose zijn en dat hiervan ongeveer 2.300 naar de huisarts gaan.
Behandelaar
Voor een groot deel van de mensen die met diarreeklachten naar de huisarts gaan, wordt geen diagnostiek aangevraagd. De schatting is dat de huisarts van 82% van de mensen die langer dan 2 dagen bloederige diarree hebben, ontlasting instuurt; van mensen met niet-bloederige diarree is dit 10%. Voor shigellose komt dit neer op 1.182 fecesonderzoeken per jaar. (4) Op basis van aannames over het aantal diagnostiekaanvragen bij Shigella en de sensitiviteit van de test, zijn vermoedelijk 329 van 1.182 fecesonderzoeken positief voor Shigella. Van de geschatte 17.000 patiënten met shigellose worden dus 329 patiënten gediagnosticeerd, dat is 1 op de 53. Dit betekent dat tegenover elke melding van een patiënt, 52 patiënten niet gemeld worden. Dat wil zeggen dat 98% (52 van de 53) van de patiënten niet gemeld wordt en bij hen dus geen contactonderzoek wordt gedaan.
Figuur 2. Stroomschema ten aanzien van bezoek huisarts en inzetten diagnostiek, weergegeven in aantallen en % per jaar, gebaseerd op Haagsma et al.
Laboratoriumonderzoek
Er is weinig literatuur over de optimale condities voor het kweken van Shigella en bovendien is de informatie niet eenduidig. Onder de ideale omstandigheden is de kweekopbrengst maximaal 80%.(5) Het beste moment voor het inzetten van een kweek is óf direct na afname en verwerken binnen maximaal 8 uur, óf het gebruik van een transportmedium en verwerken binnen 48 uur. Ook is de informatie over de optimale bewaartemperatuur tegenstrijdig, alhoewel meestal 4°C wordt geadviseerd. (6)
In de LCI-richtlijn Shigellose staat: De opbrengst van de feceskweek wordt geleidelijk minder (fout-negatieve kweek) als het fecesmonster pas na > 24 uur op het laboratorium ingezet kan worden. Inzetten van de kweek na meer dan 3 dagen heeft weinig zin.
Vragenlijst laboratoria
Dertien laboratoria uit alle regio’s in Nederland - 4 huisartsenlaboratoria, 3 in academische centra en 6 in perifere ziekenhuizen - hebben in 2018 een vragenlijst ingevuld over hun methode van diagnostiek naar Shigella. De respons was 100%. Uit de antwoorden blijkt:
- Alle laboratoria zetten eerst een PCR in; als deze positief is, vaak meer dan 24 uur na binnenkomst, wordt een kweek ingezet,
- 7 laboratoria zetten 1 dag na ontvangst van het fecesmonster, PCR in,
- 10 van de 13 laboratoria zetten in het weekend geen diagnostiek in.
Hieruit blijkt dat een kweek inzetten binnen 8 uur na monsterafname voor de meeste laboratoria niet haalbaar is.
GGD
In 2017 hebben alle GGD’en (n=25) een vragenlijst gekregen over hoe zij te werk gaan met contacten van indexpatiënten met shigellose en het aantal patiënten en uitbraken in de afgelopen jaren. De respons was 84%. Uit de antwoorden blijkt dat de GGD’en die afwijken van de LCI-richtlijn Shigellose (n=5) niet méér uitbraken of méér meldingen hadden dan de andere GGD’en (n=16). [link naar Alle resultaten]
Gegevens van 4 grote GGD’en
Voor meer informatie over indexpatiënten en hun contacten in de jaren 2016 en 2017, hebben we hebben gegevens verzameld van de GGD’en regio Utrecht, Haaglanden, Rotterdam-Rijnmond en Groningen. Van GGD regio Utrecht zijn alleen de gegevens over 2017 gebruikt. We hebben geanalyseerd hoe vaak volgens deze GGD’en fecesonderzoek geïndiceerd was bij een contact, hoe vaak het fecesmonster daadwerkelijk verstuurd is en wat de uitslag was.
- In de jaren 2016 en 2017 werden 194 indexpatiënten gemeld. Bij 38 indexpatiënten (20%) kwamen 1 of meer contacten in aanmerking voor onderzoek; in totaal werden 67 contacten geïdentificeerd. Het aantal contacten op 100 indexpatiënten was gemiddeld 35. Het viel op dat dit aantal per GGD uiteenliep van geen contact tot 77 contacten. Dit betekent dat GGD’en verschillend omgaan met de criteria in de LCI-richtlijn voor fecesonderzoek bij contacten.
- Bij 37 van de 67 contacten werd fecesonderzoek gedaan. Dat is gemiddeld 55% (82% Utrecht, 47% Haaglanden, 30% Rotterdam en 0% Groningen). 29 van de 37 fecesmonsters werden getest met PCR, waarvan 11 (38%) positief waren. Bij 4 van de 11 was ook de uitslag van de kweek positief (36%). Bij 5 contacten werd direct een kweek ingezet en die waren bij alle 5 negatief. Bij 3 contacten kon de uitslag niet uit de data worden gehaald.
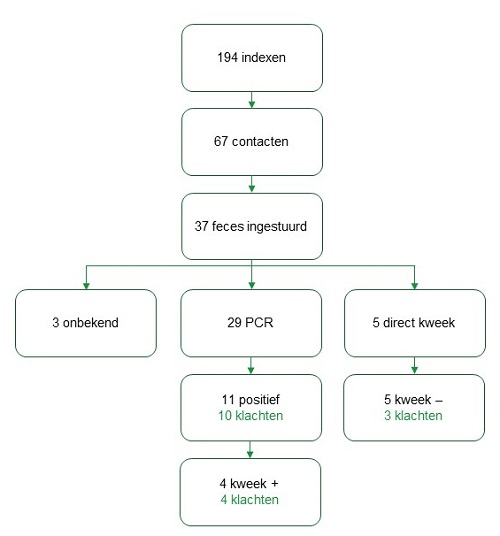
- Alle 4 contacten bij wie de PCR- en kweekuitslag positief waren, hadden klachten. Verder hebben we gekeken naar het aantal contacten met klachten en een PCR-positieve /kweek-negatieve uitslag. Het blijkt dan dat 6 van de 7 contacten met een negatieve kweekuitslag en een positieve PCR-uitslag klachten hadden. Tevens hadden 3 van de 5 contacten met een negatieve kweekuitslag bij wie geen PCR was gedaan klachten (figuur 3). Het hoge percentage klachten bij contacten met een negatieve kweekuitslag kan duiden op een vals-negatieve uitslag van de kweek.
Figuur 3. Geagrgregeerde data van de GGD'en Regio Utrecht (alleen 2017), Haaglanden, Rotterdam-Rijnmond en Groningen, 2016-2017
Extrapolatie van gegevens naar de rest van Nederland
We hebben de gegevens uit het artikel van Haagsma et al. en die van de 4 GGD’en geëxtrapoleerd naar de rest van Nederland. Dan ontstaat het volgende beeld:
In de periode 2015-2017 zijn gemiddeld 446 patiënten met shigellose gemeld (gegevens uit het Infectieziekten Bulletin). Dit is meer dan in de periode 2001-2005 waar Haagsma et al vanuit gaan. 13,5% van de mensen die shigellose hebben, gaat naar de huisarts en bij ongeveer 14,3% van hen wordt Shigella aangetoond. (4) Dit betekent dat er in de periode 2015-2017 ongeveer 3100 mensen met shigellose per jaar naar de huisarts gingen (figuur 2) en dat er per jaar ongeveer 23.000 patiënten waren.
Bij de 4 GGD’en waren in 2016 en 2017 194 indexpatiënten met 67 contacten; bij 37 contacten werd fecesonderzoek gedaan en 4 van hen bleken positief. Als we de cijfers meenemen uit de jaarverslagen van de GGD Amsterdam - de GGD met de grootste Shigella case load (2016-2017: 391 indexpatiënten met een onbekend aantal contacten, 102 fecesonderzoeken bij contacten, 18 waren positief) – dan waren er in dezelfde periode bij de 5 GGD’en samen, 585 indexpatiënten en 139 fecesonderzoeken van contacten (24%) waarvan 22 positief (16%) testten. Wanneer we deze percentages toepassen op het gemiddelde van 446 indexpatiënten in de jaren 2015-2017, betekent dit dat er in heel Nederland bij 107 contacten fecesonderzoek is gedaan (24%) waarvan 17 positief testten (16%) (tabel 1).
Tabel 1. Fecesonderzoek in Nederland 2015-2017
Op basis van cijfers Haagsma et al. (periode 2001 – 2005) | Op basis van cijfers Infectieziekten Bulletin (periode 2015-2017) |
|---|---|
| Jaarlijkse schatting | Jaarlijkse schatting |
| 17.000 mensen in de populatie met klachten van shigellose | 23.000 mensen in de populatie metklachten van shigellose |
| 2300 bezoeken aan huisarts (13,5%1) | 3100 bezoeken aan huisarts (13,5%1) |
| 329 (2) cases opgespoord/gemeld (14,3%1) | 446 cases opgespoord/gemeld (14,3%1) |
| 107 fecesonderzoeken bij contacten (24%3) | |
| 17 kweekpositieve contacten in NL (16%3) |
(1) Gebaseerd op artikel Haagsma et al. 2013 (4)(2) Gemiddeld aantal meldingen bij RIVM in die periode(3) Geëxtrapoleerd op basis van gegevens van de 4 GGD'en + GGD Amsterdam, 2016-2017
Expertmeeting
Wij hebben de resultaten van ons onderzoek gepresenteerd tijdens een expertmeeting met GGD-artsen/verpleegkundigen, epidemiologen, vertegenwoordigers van de LCI, regionaal arts-consulenten en artsen-microbiologen, uit alle regio’s van Nederland (tabel 2). Het doel van de bijeenkomst was om te bepalen of de huidige criteria voor contactonderzoek volgens de LCI-richtlijn Shigellose moeten worden herzien.
De discussie werd gevoerd aan de hand van een aantal stellingen . De afspraak was om alleen criteria aan te passen als daarover consensus was. Dit resulteerde in het voorstel om bij de volgende contacten fecesonderzoek te doen:
- Symptomatische contacten die werken in de levensmiddelensector of een verzorgend beroep hebben. Bij deze groep is het belangrijk om zicht te hebben of de indexpatiënt de contactpersoon besmet heeft. Dat is ook van belang bij eventuele juridische claims van werkgevers, bezoekers of patiënten. De contacten moeten geweerd worden tot klinisch herstel.
- Asymptomatische immuungecompromiteerde contacten, werkzaam in de levensmiddelensector of zorg. Zij kunnen langdurig asymptomatisch drager zijn en moeten geweerd worden van werk tot de kweek negatief is.
Er was consensus over de contacten bij wie fecesonderzoek niet meer nodig is:
- Asymptomatische gezins-of vergelijkbare contacten. Ook niet als ze in de levensmiddelensector werken of een verzorgend beroep hebben. Deze groep draagt weinig bij aan verdere verspreiding als blijkt dat zij drager zijn.
- Symptomatische volwassen gezins-of vergelijkbare contacten die niet in de levensmiddelensector werken of een verzorgend beroep hebben. Met deze groep worden altijd hygiënemaatregelen afgesproken, onafhankelijk van de kweekuitslag. De verspreiding zal vooral binnen het gezin blijven.
- Symptomatische gezins-of vergelijkbare contacten die op school of een kindercentrum zitten. (4) Zieke kinderen moeten thuisblijven totdat zij beter zijn. Op een kindercentrum - niet op school - zijn verscherpte hygiënemaatregelen en alertheid op nieuwe ziektegevallen gedurende 1 week nodig.
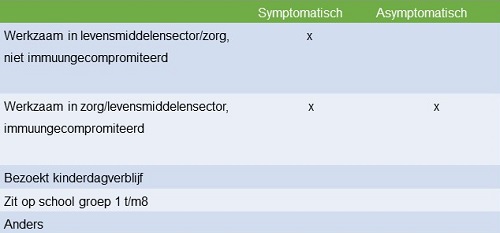
Bovengenoemde bevindingen hebben geleidt tot een aantal aanbevelingen voor de herziening van de shigelloserichtlijn (figuur 4).
Figuur 4. Bij de gezins - of vergelijkbare contacten met een X is het verrichten van fecesonderzoek zinvol, op basis van consensus tijdens de expertmeeting
Er moet meer onderzoek gedaan worden naar hoe vaak asymptomatisch dragerschap voorkomt en of asymptomatische dragers nog besmettelijk zijn. Ook moet overwogen worden of shigellapositieve PCR-uitslagen meldingsplichtig moeten worden. PCR is bij alle laboratoria de diagnostiek die het eerst wordt ingezet en vaker positief is dan kweek. Alhoewel PCR geen goed onderscheid kan maken tussen EIEC en STEC, blijkt uit de IBESS-studie dat het klinisch beeld en de invloed van EIEC en STEC op de volksgezondheid, gelijk zijn.(7)
Discussie
In de praktijk blijkt dat bij bijna de helft van de contacten van shigellosepatiënten geen fecesonderzoek wordt uitgevoerd. De fecesonderzoeken die wel worden gedaan leveren zeer weinig positieve kweken op (naar schatting jaarlijks 17 voor heel Nederland). Dit heeft met verschillende factoren te maken, zowel bij de indexpatiënt, de behandelaar, het laboratorium, de GGD als bij de contacten. Wij veronderstellen dat de tijd en kosten die met het motiveren van de contacten gepaard gaan, in veel gevallen niet opwegen tegen het aantal positieve kweken. Deze kweken zijn namelijk vaak positief bij contacten die al klachten hebben. Dan is wering op basis van het klinisch beeld voldoende.
Gevolgen van minder contactonderzoek
Het niet meer uitvoeren van fecesonderzoek bij bepaalde contacten gaat (vermoedelijk) geen significante impact hebben op de verspreiding van Shigella. Deze conclusie sluit aan bij andere artikelen die hierover gepubliceerd zijn. (1,2) Wel blijft het zinvol om bij contacten die werken in de voedselbereiding en de zorg fecesonderzoek te doen, omdat verspreiding via hen grote impact op de volksgezondheid kan hebben. Dat is een van de redenen waarom de meldingsplicht voor shigellose en het uitvoeren van bron-en contactonderzoek gerechtvaardigd blijven.
De nadelen van minder contactonderzoek zijn:
- Er zullen minder surveillancegegevens beschikbaar zijn over bijvoorbeeld antibioticaresistentie,
- Contacten die er niet zeker van zijn dat zij shigellose hebben, kunnen minder gemotiveerd zijn om geadviseerde hygiënemaatregelen op te volgen,
- Door het beperken van fecesonderzoek beschikt de GGD over minder informatie om een uitbraak of andere bijzondere situatie op te sporen.
Conclusies
Wij concluderen dat er veel argumenten zijn om het fecesonderzoek bij contacten van patiënten met shigellose te beperken. In overleg met de redactie LCI-richtlijnen zal deze aanbeveling bij de herziening van de LCI-richtlijn meegenomen worden. Dit regioproject laat zien welke methoden gebruikt kunnen worden om het nut van contactonderzoek te onderzoeken. Voor andere ziekten waarbij fecesonderzoek wordt gedaan, zoals buiktyfus en STEC, zou een soortgelijk onderzoek kunnen worden gedaan. Hierdoor kan onnodig contactonderzoek door GGD’en zoveel mogelijk worden ingeperkt.
Dit regioproject werd gefinancierd vanuit het regionale programmabudget van het RIVM voor Infectieziektebestrijding. Het volledige verslag van de resultaten is te vinden op de RIVM website
Auteurs
S.L. Niemansburg (1,2), A.M.L. Tjon-A-Tsien (2), F. van Kolfschoten (2), E.E. Stobberingh (2), H.A.C.M. Voeten (2)
- GGD Zuid-Holland Zuid.
- GGD Rotterdam-Rijnmond
Correspondentie
Literatuur
- Niessen W en Ott A. Wanneer contactonderzoek bij shigellose? Geen reden voor uitgebreid contactonderzoek bij solitaire patiënt. Commentaar. Ned Tijdschr Geneeskd. 2015;159:A8170
- Niessen W, J. van Steenbergen, T. Waegemaekers, C. Hoebe. Bron- en contactonderzoek bij individuele meldingen? Een aanzet tot een discussie. Opinie. Infectieziekten Bulletin. 2016;27(1):12-15
- Bovee L, J. Whelan, G. Sonder, A. van Dam en A. van den Hoek. Risk factors for secondary transmission of Shigella infection within households: implications for current prevention policy. BMC Infectious Diseases. 2012,12:347
- Haagsma JA, Geenen PL, Ethelberg S, Fetsch A, Hansdotter F, et al. Community incidence of pathogen-specific gastroenteritis: reconstructing the surveillance pyramid for seven pathogens in seven European Union member states. Epidemiol Infect. 2013 Aug;141(8):1625-39
- Medscape. Shigella Infection Workup, June 2016
- WHO Global Foodborne Infectious Network, Laboratory protocol: Isolation of Salmonella and Shigella from faecal specimen. November 2010
- https://www.rivm.nl/sites/default/files/2018-11/Samenvatting_Invasieve_B...
Infectieziekten Bulletin, jaargang 30, nummer 6, november 2019
Vaccinatiegraad Haagse stadsdelen in kaart
Een hoge vaccinatiegraad is belangrijk om uitbraken van infectieziekten te voorkomen.(1,2) Wanneer voldoende mensen zijn ingeënt, zijn namelijk niet alleen zijzelf maar ook de mensen om hen heen beschermd: de zogeheten groepsimmuniteit. Volgens de normen van de Wereldgezondheidsorganisatie (WHO) is een vaccinatiegraad van 95% nodig om groepsbescherming tegen een besmettelijke ziekte als mazelen te garanderen. In Nederland wordt een vaccinatiegraad van 90% als een kritische grens gezien.(1,2)
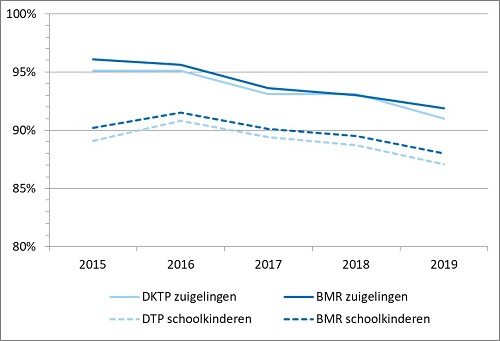
In de afgelopen jaren daalde de vaccinatiegraad in Nederland, maar in verslagjaar 2019 lijkt hier een einde aan te komen. De landelijke vaccinatiegraad bleef voor de meeste vaccinaties ongeveer gelijk aan het jaar ervoor.(3) Dit geldt echter niet voor sommige steden, zoals Den Haag. Daar daalde de vaccinatiegraad ook in verslagjaar 2019 voor alle vaccinaties behalve voor de vaccinatie tegen humaan papillomavirus (HPV). Voor de meeste vaccinaties bedroeg deze daling 1 tot 2% ten opzichte van het voorgaande jaar (figuur 1). (https://statline.rivm.nl/#/RIVM/nl/dataset/50055NED/table. Geraadpleegd: 27-09-2019).
Gemeente Den Haag presenteert een aanvalsplan
Deze ontwikkelingen zijn voor de gemeente Den Haag aanleiding om actie te ondernemen. Begin juli organiseerde zij de ‘Haagse Vaccinatie Summit’. Tijdens deze bijeenkomst wisselden zorgprofessionals, ouders en vertegenwoordigers van kinderdagverblijven ervaringen en ideeën uit om de vaccinatiegraad in Den Haag te verhogen.
Figuur 1. De vaccinatiegraad voor DKTP en BMR onder Haagse zuigelingen (2 jaar) en schoolkinderen (10 jaar) in de afgelopen vijf jaar. Den Haag, verslagjaar 2015-2019
De resultaten van de summit zijn verwerkt in een ‘Aanvalsplan vaccinatie’ dat wethouder Kavita Parbhudayal eind juli presenteerde.(4) Het plan zet in op 3 pijlers:
- Het wegnemen van belemmeringen voor (ouders van) kinderen die in aanmerking komen voor vaccinatie,
- Het communiceren en informeren over vaccinatie, gericht op zowel ouders als professionals en
- Het versterken van professionals door hen met elkaar in contact te brengen, kennis te delen en deskundigheid te bevorderen.
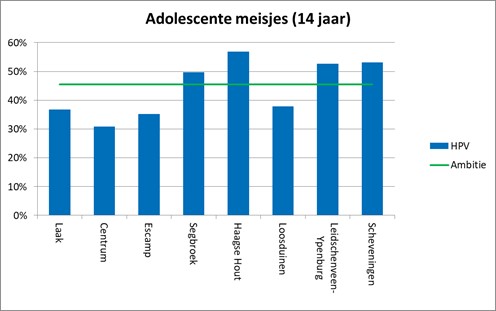
De ambitie van het aanvalsplan is om de vaccinatiegraad te verhogen naar 95% voor alle Haagse zuigelingen, kleuters en schoolkinderen. In verslagjaar 2019 varieert de vaccinatiegraad in Den Haag, afhankelijk van de leeftijdsgroep en het soort vaccinatie, tussen de 87 en 92%. Voor de HPV-vaccinatie onder adolescente meisjes is de ambitie om het landelijke vaccinatiepercentage te halen. In verslagjaar 2019 was dit 45,5%, ten opzichte van 42,1% in Den Haag.
GGD Haaglanden onderzoekt de vaccinatiegraad per stadsdeel
Voor het aanvalsplan is het belangrijk om te weten waar in Den Haag de vaccinatiegraad het laagst is. Dan kunnen namelijk, op lokaal niveau, gerichte acties worden ingezet om de vaccinatiegraad te verhogen. De afdeling Epidemiologie van GGD Haaglanden berekende de vaccinatiegraad in de 8 verschillende stadsdelen van Den Haag. Dit deed zij op basis van gegevens over het aantal (gevaccineerde) kinderen per 4-positie postcodegebied, welke zij verkreeg van het Rijksinstituut voor Volksgezondheid en Milieu (RIVM).
Naast de vaccinatiegraad in de 8 verschillende stadsdelen keek de GGD naar verschillen in de vaccinatiegraad tussen stadsdelen met en zonder achterstand. Dit wordt uitgedrukt in de zogenoemde achterstandsscore, die is gebaseerd op 5 indicatoren: inkomen, langdurige werkloosheid, het aandeel etnische culturele groepen, WOZ (waardering onroerende zaken)-waarde en verhuizingen. De scores worden berekend ten opzichte van het gemiddelde voor geheel Den Haag. Volgens de meest recente cijfers (2017) zijn Centrum en Laak de stadsdelen met de meeste achterstand, gevolgd door Escamp. De overige 5 stadsdelen hebben geen achterstand.(5)
Deze analyse richt zich op de vaccinatiegraad voor 6 vaccinaties op verschillende leeftijden, namelijk die voor zuigelingen (difterie, kinkhoest, tetanus, polio (DKTP) en bof, mazelen, rodehond (BMR)), kleuters (DKTP), schoolkinderen (DTP en BMR) en adolescente meisjes (humaan papillomavirusinfectie (HPV)).
Vaccinatiegraad blijft achter in alle stadsdelen
De vaccinatiegraad verschilt duidelijk tussen de verschillende Haagse stadsdelen. De meest opvallende resultaten zijn:
- De vaccinatiegraad in Den Haag verschilt tussen de 8 stadsdelen. Deze variatie is het grootst onder schoolkinderen en adolescente meisjes. Tussen de 81% en 93% van de schoolkinderen is gevaccineerd tegen DTP en 31% tot 57% van de adolescente meisjes is gevaccineerd tegen HPV (tabel 1).
- Alleen in de stadsdelen Leidschenveen-Ypenburg en Segbroek ligt de vaccinatiegraad voor alle vaccinaties, met uitzondering van HPV, op of boven de 90%.
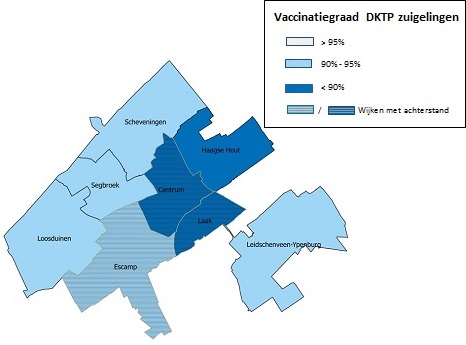
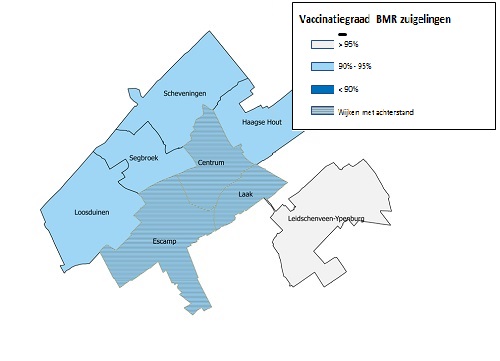
- In 7 van de 8 Haagse stadsdelen ligt de vaccinatiegraad onder zuigelingen voor BMR hoger dan voor DKTP. In Leidschenveen-Ypenburg ligt de vaccinatiegraad voor BMR boven de 95% (figuur 2 a + b). Ook onder schoolkinderen (10 jaar) ligt de vaccinatiegraad voor BMR in alle stadsdelen hoger dan voor DKTP.
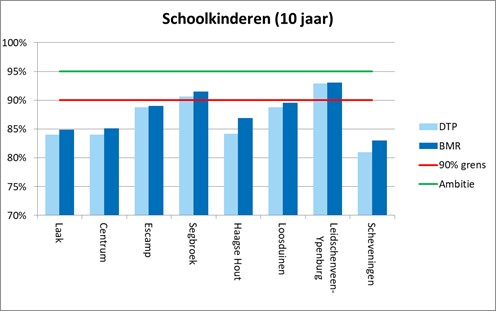
- In 6 van de 8 Haagse stadsdelen is de vaccinatiegraad voor ten minste 3 van de 6 onderzochte vaccinaties lager dan 90%. Vooral onder oudere kinderen (10 en 14 jaar) is de vaccinatiegraad vaak lager dan 90% (figuur 3).
- De vaccinatiegraad is lager in de stadsdelen Centrum en Laak, 2 stadsdelen met achterstand. Zo ligt hier de vaccinatiegraad voor alle vaccinaties, met uitzondering van BMR voor zuigelingen, onder de 90%. In Escamp, het derde stadsdeel met achterstand, ligt de vaccinatiegraad voor zuigelingen en kleuters boven de 90%, maar voor schoolkinderen en adolescente meisjes daaronder. Ook valt in Escamp de vaccinatiegraad voor HPV in negatieve zin op (35%).
- Haagse Hout, een stadsdeel zonder achterstand, volgt met vrij lage vaccinatiepercentages het patroon van Centrum en Laak, stadsdelen met achterstand. Tegelijkertijd heeft Haagse Hout voor de HPV-vaccinatie het hoogste vaccinatiepercentage van Den Haag (57%).
Tabel 1. De vaccinatiegraad onder Haagse kinderen en jongeren (%), naar stadsdeel*, leeftijdsgroep en vaccinatie. Den Haag, verslagjaar 2019
Zuigelingen 2 jaar | Kleuters 5 jaar | Schoolkinderen 10 jaar | Adolescente meisjes 14 jaar | |||||
DKTP | BMR | DKTP | DTP | BMR | HPV | |||
| Laak | 88,0 | 90,1 | 88,0 | 84,0 | 84,9 | 36,7 | ||
| Centrum | 89,9 | 90,7 | 87,7 | 84,0 | 85,1 | 30,8 | ||
| Escamp | 92,1 | 92,0 | 90,8 | 88,8 | 89,0 | 35,2 | ||
| Segbroek | 92,2 | 93,1 | 91,3 | 90,6 | 91,5 | 49,7 | ||
| Haagse Hout | 89,5 | 90,7 | 87,9 | 84,2 | 86,9 | 56,7 | ||
| Loosduinen | 91,5 | 92,1 | 93,2 | 88,7 | 89,5 | 37,8 | ||
Leidschenveen- Ypenburg | 94,9 | 95,1 | 95,8 | 92,9 | 93,0 | 52,6 | ||
| Scheveningen | 90,0 | 92,8 | 91,1 | 80,9 | 83,0 | 53,1 | ||
| Den Haag | 91,0 | 91,9 | 90,5 | 87,1 | 88,0 | 42,1 | ||
* De stadsdelen zijn van boven naar beneden geordend naar achterstandsscore. De stadsdelen Laak, Centrum en Escamp zijn stadsdelen met achterstand. Het stadsdeel Laak heeft de hoogste score (het minst gunstig / de meeste achterstand), Scheveningen heeft de laagste score (= het meest gunstig / geen achterstand).
Figuur 2a. De vaccinatiegraad voor DKTP onder zuigelingen (2 jaar), naar stadsdeel. Den Haag, verslagjaar 2019
Figuur 2b. De vaccinatiegraad voor BMR onder zuigelingen (2 jaar), naar stadsdeel. Den Haag, verslagjaar 2019
Demografische en sociaal-economische kenmerken van de stadsdelen hangen mogelijk samen met de vaccinatiegraad
Er zijn verschillende achtergrondkenmerken die van invloed zijn op de vaccinatiegraad. Denk hierbij aan religieuze of levensbeschouwelijke overtuiging. Zo staan ouders van reformatorische gezindte en antroposofische ouders kritisch tegenover het laten vaccineren van hun kinderen.(6,7) Landelijke gegevens op basis van het Rijksvaccinatieprogramma (RVP) laten zien dat ook onder kinderen in postcodegebieden met een lage sociaal-economische status en onder kinderen van ouders met een migratieachtergrond de vaccinatiegraad lager is.(8) Vooral bij de laatste groep hangt de lagere vaccinatiegraad niet zozeer samen met vaccinatiebereidheid maar meer met praktische - en taalbarrières.(7)
Figuur 3. De vaccinatiegraad onder schoolkinderen (10 jaar) en adolescente meisjes (14 jaar), naar stadsdeel en vaccinatie. Den Haag, verslagjaar 2019
Naast verschillen in achtergrondkenmerken kan ook vertekening een rol spelen bij verschillen in de vaccinatiegraad tussen gebieden. Dit speelt bijvoorbeeld op plaatsen waar relatief veel expats wonen. Kinderen van expats zijn mogelijk wel gevaccineerd, maar zijn niet altijd als zodanig geregistreerd in het RVP.(9) De vaccinatiegraad kan dan ten onrechte lager lijken dan deze in werkelijkheid is.
Tussen de Haagse stadsdelen zijn aanzienlijke verschillen ten aanzien van de migratieachtergrond en sociaaleconomische status van de bevolking. Het percentage inwoners met een (niet-westerse) migratieachtergrond en het percentage inwoners met een lagere sociaaleconomische status is relatief hoog in de stadsdelen met achterstand; Laak, Centrum en Escamp. Het aandeel inwoners met een westerse migratieachtergrond, waaronder zich naar verwachting de meeste expats bevinden, is het hoogst in de stadsdelen Haagse Hout, Scheveningen en Laak.(10) (https://denhaag.incijfers.nl/. Geraadpleegd: 29-10-2019). Deze demografische en sociaal-economische kenmerken van de stadsdelen verklaren mogelijk (deels) de verschillen in vaccinatiegraad. Een oorzakelijk verband kan op basis van de huidige analyses echter niet worden aangetoond.
Een wijkgerichte aanpak is nodig
Op basis van de verschillen in vaccinatiegraad en demografische en sociaal-economische kenmerken tussen de Haagse stadsdelen pleit de GGD voor een wijkgerichte aanpak. Die aanpak dient rekening te houden met aspecten als gezondheidsvaardigheden, toegang tot de jeugdgezondheidszorg, laaggeletterdheid en culturele achtergrond. Samenwerking met professionals in de wijk is daarbij essentieel. Zij horen namelijk dagelijks hoe mensen denken over gezondheid en preventie en kunnen echt het gesprek aangaan met ouders over vaccinaties.
Auteurs
J.E. Brussee (1), M.P.H. Berns (2), V.C. de Ridder – Hagenaars (2), J.D. van der Marel (2), A.S. de Boer (2)
- Lucidus tekst
- GGD Haaglanden
Correspondentie
Literatuur
- World Health Organization (WHO). Global measles and rubella strategic plan: 2012-2020. Genève: WHO, 2012.
- World Health Organization (WHO). Global Vaccine Action Plan 2011–2020. Genève: WHO, 2013.
- Lier EA van, Oomen PJ, Giesbers H, Vliet JA van, Drijfhout IH, Zonnenberg-Hoff IF, et al. Vaccinatiegraad en jaarverslag Rijksvaccinatieprogramma Nederland 2018. RIVM rapport nr. 2019-0015. Bilthoven: Rijksinstituut voor Volksgezondheid en Milieu, 2019.
- Aanvalsplan vaccinatie. Den Haag: Gemeente Den Haag, 2019.
- Den Haag in Cijfers, Onderzoek Kloek Adviezen S&O en OCW/Onderzoek. Rapportage Achterstandsscores Den Haag 2017. Den Haag: gemeente Den Haag, 2017.
- Ruijs WLM. Acceptance of Vaccination among Orthodox Protestants in The Netherlands [proefschrift]. Nijmegen: Radboud Universiteit Nijmegen; 2012.
- Harmsen I. Vaccinating – Self-evident or not? [proefschrift]. Maastricht: Universiteit Maastricht; 2014.
- Lier EA van, Oomen PJ, Zwakhals SLN, Drijfhout IH, de Hoogh PAAM. Vaccinatiegraad Rijksvaccinatieprogramma Nederland. Verslagjaar 2010. RIVM rapport nr. 210021011/2010. Bilthoven: Rijksinstituut voor Volksgezondheid en Milieu, 2010.
- Koolhaas C, van der Linden E, Prevos B, Konings T. Vaccinatierapport. Zoetermeer: JGZ Zuid-Holland West; 2019.
- Ooijevaar J, Verkooijen L. Expat, wanneer ben je het? Den Haag: Centraal Bureau voor de Statistiek, 2015.
Infectieziekten Bulletin, jaargang 30, nummer 6, november 2019
Whole genome sequencing van Mycobacterium tuberculosis
Het MTBC bestaat uit de (sub)species M. tuberculosis, M. canettii, M. orygis, M. pinnipedii, M. caprae, M. bovis, M. bovis BCG, M. microti, M. mungi, M. suricattae, en de zogenoemde dassie bacillus. M. tuberculosis kan worden onderverdeeld in 7 genotypefamilies. Het herkennen van isolaten is van belang voor epidemiologisch onderzoek en de behandeling. M. bovis bijvoorbeeld is niet gevoelig voor pyrazinamide, een antibioticum dat in de eerstelijn wordt gebruikt om tuberculose te behandelen. M. bovis en M. pinnipedii veroorzaken meestal extra-pulmonale tuberculose en hebben bijna altijd een dierlijke bron. M. pinnipedii wordt vrijwel uitsluitend gevonden bij zeehonden, zeeleeuwen en aanverwante soorten. M. bovis BCG wordt gevonden als complicatie na BCG-vaccinatie en na behandeling van blaascarcinomen met een BCG-preparaat. (2-4) Momenteel wordt voor het herkennen van (sub)species gebruik gemaakt van de reverse-line-blot-methode die gebaseerd is op variaties in het gyrase B-gen en een bepaalde grote genomische deletie. Echter, de reverse-line-blotmethode kan geen onderscheid maken tussen M. tuberculosis en M. canettii en ook niet tussen M. africanum, M. pinnipedii en M.orygis. Daarnaast kan de reverse-lineblotmethode géén van de genotypen van M. tuberculosis herkennen.
De klassieke methode om resistentie tegen antibiotica te vinden is het gebruik van de fenotypische Mycobacterium Growth Indicator Tube (MGIT); dit is tevens de internationale referentiestandaard van de World Health Organization (WHO). MGIT is gebaseerd op het testen van de gevoeligheid van M. tuberculosis bij 1 kritische concentratie van een antibioticum. Naast het feit dat de uitslagen van de MGIT soms weken of maanden op zich laten wachten vanwege de langzame groei van M. tuberculosis, is deze methode niet altijd accuraat en reproduceerbaar:
- Het testen van de gevoeligheid tegen pyrazinamide bijvoorbeeld vergt speciale groeicondities: er wordt een relatief groot inoculum van de bacteriën getest vergeleken met de testen voor andere eerstelijnsmiddelen, wat kan leiden tot fout-positieve uitslagen. Daarnaast kan de remming van de bacteriële groei het gevolg zijn van de zure omgeving waarin pyrazinamide uitsluitend actief is in plaats van daadwerkelijke gevoeligheid van M. tuberculosis.
- Een andere, zeer relevante tekortkoming van MGIT is het feit dat in principe uitsluitend 1 kritische concentratie van een middel wordt getest. Hierdoor is het niet mogelijk om een laag niveau van resistentie te vinden, waardoor de desbetreffende isolaten in de MGIT soms onterecht als gevoelig worden beschouwd. Fout-negatieve resistentiebepalingen kunnen resulteren in een slechte behandeluitkomst en uiteindelijk bij de patiënt zelfs tot een terugval leiden als hij/zij ten gevolge van de negatieve uitslag een te lichte behandeling krijgt. Dit is ongewenst, vooral omdat er aanpassingen in de doseringen van isoniazide en rifampicine mogelijk zijn waarbij de patiënt, in geval van een laag niveau van resistentie, met een hogere dosis behandeld kan worden.
Naast de fenotypische testen werden in de afgelopen decennia ook diverse snelle DNA-methoden ontwikkeld om specifieke resistentiemutaties te vinden. (5,6) Echter, deze sneltesten beperken zich tot een aantal bekende resistentiemutaties terwijl de praktijk weerbarstiger is: er komen veel meer variaties voor van resistenties dan je met dit soort testen kunt vinden.
Sinds 1993 worden alle isolaten van M. tuberculosis naar het tuberculosereferentielaboratorium van het RIVM gestuurd voor epidemiologische typering en, op aanvraag, voor resistentiebepalingen en het herkennen van (sub)species. Voor alle isolaten in de periode 2009-2018 werd gebruik gemaakt van de typeringsmethode Variable Number Tandem Repeat (VNTR). Deze methode is gebaseerd op amplificatie van 24 repeterende loci/regio’s in het genoom, wat resulteert in een numerieke code van 24 getallen die het aantal repeats in elk van de 24 geteste genomische regio’s representeert. Isolaten met een identiek 24-loci VNTR-patroon worden aan een VNTR-cluster toegekend, wat een epidemiologisch verband suggereert tussen de betreffende patiënten. De informatie over de clustering van patiënten op basis van VNTR werd tot en met 2018 wekelijks met GGD’en gedeeld ter ondersteuning van het bron-en contactonderzoek. Het onderscheidende vermogen van VNTR was echter niet optimaal. Ondanks actieve bronopsporing van patiënten, vonden GGD’en in de praktijk bij slechts ≈ 26% van de op basis van VNTR geclusterde patiënten een epidemiologisch verband. (7) Op basis van VNTR was er bijvoorbeeld vaak sprake van clustering tussen asielzoekers en immigranten met verschillende achtergronden die GGD’en niet aan elkaar konden linken.
In dit artikel zullen de gepubliceerde resultaten worden samengevat over het gebruik van WGS voor:
- herkennen van (sub)species en genotypen binnen het MTBC
- de bepaling van de gevoeligheid van MTBC-isolaten voor eerstelijnsmiddelen
- het in kaart brengen van de genetische afstand tussen isolaten om transmissie tussen tuberculose- patiënten te volgen
Identificatie van (sub)species en genotypen binnen het MTBC
In samenwerking met de Oxford Universiteit in Engeland is de op WGS gebaseerde SNP-IT(SNPs to Identify TB)-methode ontwikkeld voor het herkennen van (sub)species en genotypen binnen het MTBC. (8) De nieuwe methode is ontwikkeld op basis van een maximaal gevarieerde set - wat betreft (sub)species en genotype families - van 323 isolaten uit collecties van het RIVM en de Oxford Universiteit. SNP-IT is gebaseerd op meervoudige SNPs (fylogenetische SNPs) die uniek zijn voor de desbetreffende (sub)species of genotypen en die dus afwezig zijn in de overige (sub)species en genotypen. Met SNP-IT werden in totaal 13.893 fylogenetische SNPs geïdentificeerd, waarbij M. canettii het grootste aantal karakteristieke fylogenetische SNPs bevat (n = 6.837) en M. bovis het kleinste aantal (n = 23). SNP-IT werd gevalideerd op 614 sequenties van MTBC-isolaten uit de database van Public Health England en een internationale database. Alle 614 sequenties uit de validatieset werden correct geïdentificeerd met SNP-IT.
De interne validatie bij het RIVM van in totaal 742 sequenties liet 2 afwijkingen zien waarbij de isolaten werden aangeduid als M. orygis met de SNP-IT, maar als M. africanum met de reverse-line-blotmethode. Op basis van pncA-mutaties en de VNTR bleken deze 2 isolaten inderdaad tot M. orygis te behoren en dus correct geïdentificeerd met SNP-IT. Verder werden met de reverse-line-blot-methode 699 isolaten als M. tuberculosis geïdentificeerd, terwijl deze met SNP-IT verder onderverdeeld werden in verschillende genotypen zoals Beijing, Delhi/Central-Asian en Euro-American.
Gevoeligheidsbepaling voor eerstelijnsmiddelen
De betrouwbaarheid van WGS ten opzichte van MGIT om de gevoeligheid van M. tuberculosisisolaten te testen tegen de eerstelijnsmiddelen rifampicine, isoniazide, ethambutol en pyrazinamide werd onderzocht in een populatiestudie. (9) Met WGS werden 9 genen en/of promotorregio’s onderzocht op mutaties die geassocieerd zijn met resistentie. De isolaten die niet overeenkomstige resultaten gaven in de MGIT/WGS werden opnieuw getest in de MGIT door de kritische concentratie en een concentratie net onder het breekpunt te testen. Verder werd de incubatietijd in de MGIT verlengd tot 45 dagen. De laatste 2 aanpassingen werden toegepast om ook laagresistente isolaten te vinden. De voorspellende waarden van WGS werden vergeleken met de MGIT-referentiestandaard én met een zogenoemde samengestelde referentiestandaard. Isolaten met (laag) resistentiegeassocieerde mutaties voor rifampicine, isoniazide en ethambutol die vaak als gevoelig worden gerapporteerd met MGIT, maar die een verhoogde minimaal remmende concentratie lieten zien bij het hertesten met MGIT, werden als resistent ingevoerd in de samengestelde referentiestandaard.
Deze studie omvatte 1.121 MTBC-isolaten (met uitzondering van M. bovis BCG) uit 2016 en 2017, waarvan ≈ 11% resistent was tegen 1 of meerdere antibiotica. De vergelijking van WGS- met de initiële MGIT-resultaten toonde 57/1.121 (5.1%) afwijkende isolaten. De meeste afwijkingen voor isoniazide en ethambutol konden verklaard worden doordat deze bacteriële groei lieten zien bij de concentraties net onder het breekpunt wanneer ze opnieuw getest werden met MGIT. De meeste afwijkingen voor rifampicine waren te verklaren doordat deze bacteriële groei vertoonden bij langere incubatie in de MGIT bij het hertesten. Beiden zijn aanduidingen voor een laag niveau van resistentie die normaal bij het testen van 1 breekpunt als ‘gevoelig’ werden gerapporteerd met MGIT. De meeste afwijkingen voor pyrazinamide waren te wijten aan het algemeen bekende probleem van de lage reproduceerbaarheid van de MGIT-gevoeligheidsbepaling voor dit antibioticum. De negatief voorspellende waarde van WGS ten opzichte van de MGIT-referentiestandaard was 100%, 99.8%, 99.9% en 99.3% voor respectievelijk rifampicine, isoniazide, ethambutol en pyrazinamide (tabel 1). Dit houdt in dat wanneer met WGS geen mutaties in de resistentiegenen werden gevonden, dit in ≥ 99.3% van de gevallen ook MGIT-gevoelige isolaten waren. De positief voorspellende waarde van WGS ten opzichte van de samengestelde referentiestandaard steeg aanzienlijk naar 91.2%, 99% en 80% voor respectievelijk rifampicine, isoniazide en ethambutol, wat de tekortkomingen van de MGIT als referentiestandaard weergeeft voor het aantonen van laagresistente isolaten (tabel 1).
Tabel 1. Voorspellende waarden van WGS ten opzichte van de MGIT-referentiestandaard en de samengestelde referentiestandaard voor de 1.121 MTBC-isolaten
| MGIT-referentiestandaard | Samengestelde referentiestandaard | |||||||
sensiti- viteit | specifi- citeit | PVW | NVW | sensiti- viteit | specifi- citeit | PVW | NVW | |
| Rifampicine | 100% | 99.2% | 73.5% | 100% | 96.6% | 99.7% | 91.2% | 99.9% |
| Isoniazide | 97.8% | 99.2% | 91.9% | 99.8% | 98% | 99.9% | 99% | 99.8% |
| Ethambutol | 80% | 98.6% | 20% | 99.9% | 94.1% | 99.6% | 80% | 99.9% |
| Pyrazinamide | 85.1% | 98.8% | 75.5% | 99.3% | - | - | - | - |
| PVW=positief voorspellende waarde; NVW=negatief voorspellende waarde | ||||||||
Epidemiologische typering
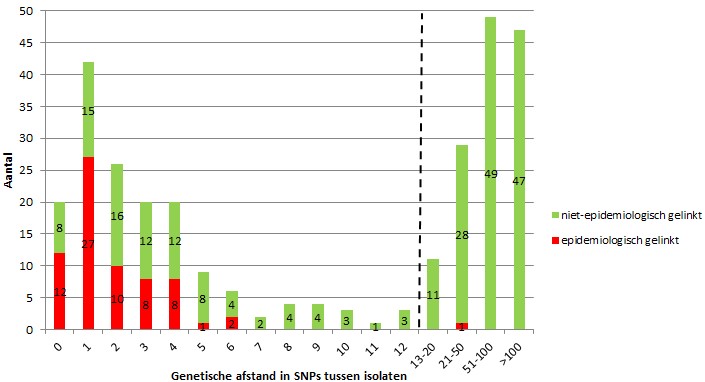
Op alle MTBC-isolaten uit 2016 (10) en 2017 werd zowel de VNTR-typering als WGS toegepast. Isolaten met een identiek 24-loci VNTR-patroon werden als ‘geclusterd’ beschouwd en de patiënten in deze clusters werden doorgegeven aan GGD’en als ‘mogelijk epidemiologisch met elkaar verbonden’. De definitie van clustering van isolaten op grond van WGS was een maximale genetische afstand van 12 SNPs tussen isolaten.
In totaal werden 1.108 isolaten getypeerd met zowel WGS als VNTR, waarvan 427 (39%) clusterden op basis van VNTR en 277 (25%) op basis van WGS. Brononderzoek door GGD’en naar de 427 VNTR- geclusterde patiënten resulteerde in 110 bevestigde epidemiologische verbanden. De genetische afstanden tussen de 427 VNTR-geclusterde isolaten staan in figuur 1. Onder de WGS-geclusterde patiënten werden 108/110 epidemiologische verbanden gevonden. Eén epidemiologisch verband tussen 2 patiënten werd niet gevonden met WGS; volgens de GGD was er voor de vervolgpatiënt risico geweest op blootstelling tijdens de besmettelijke periode van de bronpatiënt, maar beide patiënten waren < 2.5 jaar in Nederland en geboren in landen die hoog endemisch zijn voor tuberculose. Het is mogelijk dat deze patiënten door een andere bron waren geïnfecteerd tijdens de vluchtroute naar Nederland of dat zij al waren geïnfecteerd in het land van herkomst.
Figuur 1. Genetische afstand in SNPs tussen de 427 VNTR-geclusterde isolaten uit 2016 en 2017
Discussie/conclusie
De betrouwbaarheid van WGS voor het herkennen van (sub)species en genotypen, het aantonen van de gevoeligheid tegen eerstelijnsmiddelen en de epidemiologische typering van MTBC-isolaten is groter dan bij de conventionele laboratoriumtechnieken. WGS heeft in de typering een veel hoger onderscheidend vermogen dan VNTR om epidemiologische verbanden op te sporen. Met WGS daalt het aantal geclusterde patiënten aanzienlijk, terwijl alle epidemiologische verbanden wel degelijk worden gevonden. Dit betekent dat GGD’en op een nog efficiëntere wijze bron-en contactonderzoek kunnen uitvoeren. De validatie bij het RIVM en in Engeland geven aan dat de nieuwe op WGS gebaseerde SNP-IT-methode een uiterst betrouwbare benadering is en specifieker is dan de huidige methode, omdat met SNP-IT, naast alle (sub)species, ook de genotypen herkend worden. Daarnaast heeft WGS een zeer hoge negatief voorspellende waarde (≥ 99.3%) voor het voorspellen van gevoeligheid tegen de eerstelijnsmiddelen rifampicine, isoniazide, ethambutol en pyrazinamide, door het uitsluiten van aanwezigheid van resistentiemutaties. De positief voorspellende waarde verschilt echter sterk per mutatie en zal ook als dusdanig worden gerapporteerd. Verder kan met WGS op accurate wijze een laag niveau van resistentie tegen antibiotica gevonden worden. Dit wordt soms met MGIT gemist omdat isolaten onterecht als ‘gevoelig’ worden getest omdat dat slechts 1 kritische concentratie van het antibioticum in de MGIT-bepaling getest wordt.
In Engeland gebruikt men WGS sinds kort voor het herkennen van (sub)species/genotypen, de screening op gevoeligheid en de epidemiologische typering van M. tuberculosis. In Nederland gebruikt men vanaf januari 2019 WGS voor de typering en zal de overstap voor het herkennen van (sub)species/genotypen en het screenen op de gevoeligheid voor antibiotica, in 2020 worden gemaakt. Vanzelfsprekend blijven de fenotypische testen uitgevoerd worden met uitgebreidere concentratiereeksen als er resistentiemutaties worden aangetoond, of op speciaal verzoek.
Al met al is de invoering van WGS in de laboratoriumdiagnostiek van tuberculose een aanzienlijke stap voorwaarts. Op dit moment is de beschreven techniek toepasbaar op positieve MGIT-kweken. Er wordt echter al gewerkt aan het direct toepassen van WGS op klinisch materiaal, waarbij momenteel helaas de onnauwkeurigheid nog een groot probleem vormt vanwege de aanwezigheid van humaan DNA en overig niet-mycobacterieel DNA in de sequenties. Het is wel mogelijk om targeted sequencing toe te passen op klinisch materiaal. Hierbij worden genomische regio’s van interesse, zoals de resistentiegenen, duizenden malen vermenigvuldigd, waardoor de gevoeligheid van de test sterk toeneemt. Hoewel uit deze targeted sequencing minder informatie verkregen kan worden dan uit WGS, wordt dit in de komende periode een belangrijke toepassing in regionale en perifere laboratoria.
Auteurs
R. Jajou, D. van Soolingen, Centrum Infectieziektebestrijding, Rijksinstituut voor Volksgezondheid en Milieu, Bilthoven
Correspondentie
rana.jajou@rivm.nl of dick.van.soolingen@rivm.nl
Literatuur
- RIVM. Tuberculosis keypoints the Netherlands 2018. Beschikbaar via: https://www.rivm.nl/sites/default/files/2019-03/011226_120101_Kerncijfer....
- Lamm DL, van der Meijden PM, Morales A, et al. Incidence and treatment of complications of bacillus Calmette-Guerin intravesical therapy in superficial bladder cancer. J Urol. 1992;147(3):596-600.
- Elkabani M, Greene JN, Vincent AL, et al. Disseminated Mycobacterium bovis after intravesicular bacillus calmette-Gu rin treatments for bladder cancer. Cancer Control. 2000;7(5):476-81.
- Bakker M, Stadhouders NAM, Van Hest NAH, et al. Tuberculose door het BCG-vaccin. Tegen de Tuberculose. 2013;109(3):8-9.
- Boehme CC, Nabeta P, Hillemann D, et al. Rapid molecular detection of tuberculosis and rifampicin resistance. N Engl J Med. 2010;363:1005-15
- Schön T, Miotto P, Koser CU, et al. Mycobacterium tuberculosis drug-resistance testing: challenges, recent developments and perspectives. Clin Microbiol Infect. 2017;23:154-60.
- Slump E, Blijboom L, Bregman IM, et al. Tuberculose in Nederland 2017: Surveillancerapport inclusief rapportage monitoring van interventies. 2018. Beschikbaar via: https://www.rivm.nl/bibliotheek/rapporten/2018-0143.pdf.
- Lipworth S, Jajou R, de Neeling A, et al. SNP-IT Tool for Identifying Subspecies and Associated Lineages of Mycobacterium tuberculosis Complex. Emerg Infect Dis. 2019;25(3):482-8.
- Jajou R, van der Laan T, de Zwaan R, et al. WGS more accurately predicts susceptibility of Mycobacterium tuberculosis to first-line drugs than phenotypic testing. J Antimicrob Chemother. 2019: doi:10.1093/jac/dkz215.
- Jajou R, de Neeling A, van Hunen R, et al. Epidemiological links between tuberculosis cases identified twice as efficiently by whole genome sequencing than conventional molecular typing: A population-based study. PLoS One. 2018;13(4):e0195413.
Infectieziekten Bulletin, jaargang 30, nummer 6, november 2019
Jaaroverzichten
Een terugblik op Listeria, STEC, soa en Salmonella in 2018
Listeria in 2018
Surveillance van Listeria monocytogenes in Nederland in 2018Registraties infectieziekten
Wet publieke gezondheid
De meldingen Wet publieke gezondheid tot en met week 44, 2019
Virologische weekstaten
De meldingen uit de virologische weekstaten tot en met week 44, 2019