Infectieziekten Bulletin
Juni 2018 | jaargang 29, nummer 5/6
https://magazines.rivm.nl/2018/06/infectieziekten-bulletin
Gesignaleerd
Binnenlandse signalen
Griepepidemie na achttien weken ten einde
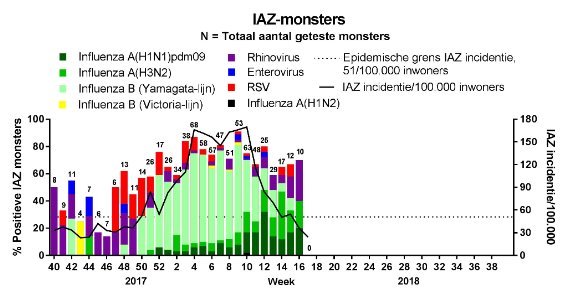
De langdurige griepepidemie in Nederland is officieel ten einde. De incidentie van influenza-achtig ziektebeeld (IAZ) was 24 per 100.000 inwoners in week 17, 2018, en daarmee voor de tweede week onder de epidemische drempel van 51 patiënten met IAZ per 100.000 inwoners. De griepepidemie 18 weken heeft geduurd: van 11 december 2017 tot en met 15 april 2018 (Figuur 1). Wel wordt sporadisch nog steeds influenzavirus gedetecteerd. Aan het begin van de epidemie was influenzavirus type B (Yamagatalijn) dominant. Later in de epidemie werden vaker influenzavirustypen A(H3N2) en A(H1N1)pdm09 gedetecteerd.
Figuur 1. Incidentie van IAZ en laboratoriumuitslagen van monsters van patiënten met IAZ, Nederland, week 40 2017 – week 17 2018 (Bron: Nivel/RIVM)
Verschillende media berichtten tijdens de epidemie over grote drukte in de ziekenhuizen. Omdat er veel patiënten met griep waren en een tekort aan personeel, moesten soms geplande operaties worden uitgesteld. Ook waren er tijdens de epidemie meer patiënten met een pneumonie en was de totale sterfte, vooral onder mensen van 65 jaar en ouder, verhoogd. De cumulatieve totale sterfte tijdens de epidemie was hoog met een oversterfte van ruim 9.000 personen. Dit aantal was hoger dan in de 8 voorgaande seizoenen: van 2009/2010 tot en met 2016/2017 lag de oversterfte tussen 0 en 8.500 tijdens de griepepidemie. Het is bekend dat griep een rol kan spelen bij oversterfte, maar er kunnen ook andere factoren een rol spelen. (Bronnen: RIVM, Sterftemonitoring, Nivel, ErasmusMC, CBS)
Toename invasieve meningokokkenziekte door serogroep W (vervolg)
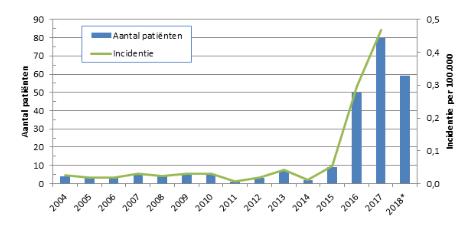
Sinds 2015 is er in Nederland een toename van het aantal patiënten met meningokokkenziekte veroorzaakt door serotype W. Van oktober 2015 tot en met mei 2018 werden er 198 patiënten gerapporteerd (9 in 2015, 50 in 2016, 80 in 2017 en 59 tot en met mei 2018). Vóór 2015 waren er gemiddeld 4 patiënten per jaar met meningokokkenziekte serogroep W (incidentie: 0,03 per 100.000 personen per jaar). De incidentie is gestegen naar 0,47 per 100.000 personen in 2017 (Figuur 2).
Figuur 2. Aantal patiënten en incidentie per 100.000 personen van meningokokkenziekte serogroep W van 2004 tot en met mei 2018. Op basis van melddatum aan het Nederlands Referentie Laboratorium voor Bacteriële Meningitis (AMC/RIVM)
Er is recent veel media aandacht geweest voor deze toename. De ziekte komt het meest voor bij kinderen jonger dan 5 jaar, adolescenten, jongvolwassenen en mensen van 65 jaar of ouder. De patiënten wonen verspreid over Nederland. Er zijn geen gezinsleden of andere contactpersonen in de omgeving van een patiënt met meningokokkenziekte serogroep W, ziek geworden. Vanwege de toename van meningokokkenziekte serogroep W is vanaf 1 mei 2018 de MenC-vaccinatie op 14 maanden vervangen door een vaccinatie met het quadrivalente conjugaatmeningokokkenvaccin tegen groep A, C, W en Y. Per 1 oktober 2018 wordt deze vaccinatie ook aangeboden aan alle tieners die dit jaar tussen 1 mei en 31 december 14 jaar worden. Vaccineren van tieners is het meest effectief om verspreiding van meningokokken W tegen te gaan, omdat bij hen het dragerschap het hoogst is. Er is momenteel beperkt MenACWY-vaccin beschikbaar op de vrije markt. Vaccins voor het RVP worden apart ingekocht. Bronnen: RIVM, Eurosurveillance.
Toename Eritrese minderjarige vluchtelingen met tuberculose
In 2018 werd tot en met 13 juni bij de eerste screening van asielzoekers door GGD Groningen opvallend veel tuberculose gevonden onder alleenstaande minderjarige vluchtelingen uit Eritrea: bij 16 (allen geboren in 2001-’03) en bij 1 elders in het land (totaal 17). In de eerste 5 maanden van dit jaar werd bij 13 van de 350 (3,7%) AMV'ers uit Eritrea tuberculose vastgesteld. Dat is veel hoger dan in dezelfde periode in 2017 (0,9%), en ongekend hoog in de tuberculosebestrijding. Naast hun gemeenschappelijke land van herkomst, is hun reisroute naar Nederland een overeenkomstige factor: via Libië, waar ze vaak vele maanden en met honderden andere mensen in slechte omstandigheden in loodsen en dergelijke verbleven.Tot nu toe is bij 7 van de 17 Eritrese alleenstaande jongeren de pulmonale tuberculose met kweek bevestigd. De variable number of tandem repeats (VNTR) typering van deze 7 patiënten vallen in al bekende VNTR clusters in Nederland. Vier isolaten in een zeer groot VNTR cluster (>100 patiënten/isolaten). De andere, 2 isolaten en 1 isolaat, vallen in twee kleinere VNTR clusters. Er zijn dus meerdere bronnen geweest die de infecties veroorzaakt hebben.Na overleg met diverse deskundigen/organisaties is besloten om de Eritrese AMV'ers die dit jaar in Nederland zijn gekomen, op latente tuberculose-infectie te onderzoeken en preventief te behandelen indien geïnfecteerd. De GGD Groningen zal dit coördineren en afdelingen tuberculosebestrijding van GGD'en informeren over de personen die opgeroepen moeten worden. De GGD Groningen zal ook de opkomst en opbrengst van deze interventie evalueren, alsmede eventueel ervaren knelpunten in de uitvoering. Asielzoekers worden bij aankomst in Nederland opgevangen in het asielzoekerscentrum in Ter Apel. Daar worden zij op tuberculose gescreend door GGD Groningen. Na de binnenkomstscreening worden zij op andere plaatsen in Nederland ondergebracht Asielzoekers met tuberculose worden met tuberculosemedicatie behandeld. De landelijke tuberculosesurveillance laat een dalende trend zien van tuberculose onder asielzoekers (ongeacht leeftijd en land van herkomst), na een eerdere toename in 2015 en 2016. (Bronnen: GGD Groningen, RIVM)
Psittacosemeldingen mogelijk gerelateerd aan dezelfde dierenwinkel
In Orisis zijn 5 patiënten met psittacose gemeld die dezelfde grote dierenwinkel in Noord-Brabant hadden bezocht. De eerste ziektedag van de patiënten, tussen 50-75 jaar oud, was in de periode van 22 februari tot en met 22 april 2018. Alle 5 patiënten werden opgenomen in het ziekenhuis waar met behulp van polymerase chain reaction (PCR) psittacose werd vastgesteld in keel, neus en/of sputum. Alle patiënten houden ook vogels thuis als hobby. Eén van hen had eind februari ook de vogelshow in Zwolle bezocht. (zie Infectieziekte Bulletin, nummer 4, 2018).
De vogels zijn ook onderzocht. De duiven van 1 van de patiënten testten positief op Chlamydia psittaci (genotype B), terwijl bij deze patiënt zelf genotype A was geïsoleerd. De vogels van 2 andere patiënten testten positief op Chlamydia psittaci (genotype A). De vogels van de overgebleven 2 patiënten testten negatief.
De Nederlandse Voedsel- en warenautoriteit (NVWA) heeft de dierenwinkel bemonsterd en de helft van de (feces)monsters van de aanwezige vogels testten positief op Chlamydia psittaci (genotype A). De besmette vogels in de dierenwinkel zullen afgescheiden van andere vogels en bezoekers worden verzorgd, totdat de besmetting over is. (Bronnen: GGD Hart voor Brabant, GGD regio Dienst Gezondheid & Jeugd ZHZ, RIVM, NVWA)
Droge en/of gefermenteerde varkensworst geassocieerd met hepatitis E
Verschillende droge en/of gefermenteerde varkensworsten zijn geassocieerd met blootstelling aan het hepatitis E-virus (HEV). Dit is een van resultaten van een onderzoek door het RIVM en Sanguin naar de risicofactoren voor hepatitis E-virusseropositiviteit bij Nederlandse bloeddonoren. Deze bevinding komt overeen met de resultaten van de HEVIG-studie (Hepatitis E-Virus in de Gemeenschap) naar bronnen en risicofactoren voor acute hepatitis E in Nederland. Beide studies wijzen erop dat hepatitis E in Nederland voornamelijk opgelopen wordt door consumptie van droge en/of gefermenteerde worsten van rauw varkensvlees: cervelaat, salami, boerenmetworst, snijworst, fijnkost, salametti. In mindere mate wordt hepatitis E opgelopen door contact met fecaal verontreinigd water, bijvoorbeeld in een septische tank. De NVWA heeft 90 monsters van droge en/of gefermenteerde worst, gesneden als vleeswaren, onderzocht. Met een gevalideerde, nog niet geaccrediteerde methode, troffen zij in 14 monsters (15.6%) HEV RNA aan. Met deze nieuwe inzichten wordt het bestaande voedingsadvies van het Voedingscentrum, de NVWA en het RIVM aan kwetsbare groepen aangepast, met specifieke vermelding van deze vleesproducten. De bevindingen zijn ook in overeenstemming met het rapport van de vleeswarenindustrie Risico classificeren en beheersen HEV in vleeswaren. In dit rapport staat dat het risico op HEV-besmetting wordt veroorzaakt doordat in het eindproduct het middenrif van het varken wordt verwerkt, met mogelijk daaraan geringe stukken van de lever. Deze eindproducten worden niet voor consumptie verhit. Door niet langer het middenrif te gebruiken zou het risico van HEV in verminderd kunnen worden.
In bijna alle Europese landen is sprake van een stijging van van het aantal patiënten met hepatitis E en een stijging van het aantal met HEV besmette varkens. Daarom zal ook in andere Europese landen aandacht gevraagd worden voor het terugdringen van het besmettingsrisico met HEV door consumptie van droge en/of gefermenteerde worsten van rauw varkensvlees. (Bronnen: RIVM, Sanquin, NVWA, Vereniging voor de Nederlandse Vleeswarenindustrie)
Buitenlandse signalen
Ebola-uitbraak in Democratische Republiek Congo
De Congolese minister van Volksgezondheid maakte op 8 mei bekend dat ebolavirus (sp. Zaire ebolavirus) was aangetoond in 2 patiënten waarvan het vermoeden was dat zij virale hemorragische koorts hadden. De patiënten wonen in het dorp Bikoro in de afgelegen provincie Equateur van de Democratische Republiek Congo (DRC). Op 12 juni waren er 59 patiënten bekend, waarvan 38 met een bevestigde ebolabesmetting. Voor zover bekend zijn er tot nu toe 28 mensen overleden (case fatality 47%), waaronder ook gezondheidswerkers. Meer dan 600 contacten worden gemonitord. De World Health Organization (WHO), Unicef en Artsen zonder Grenzen (AZG) bieden de Congolese overheid ondersteuning bij de bestrijding van het ebolavirus. De WHO oordeelde op 18 mei dat, op basis van de ingezette maatregelen, de volksgezondheidsadviezen en de beschikbaarheid en inzet van een vaccin, deze uitbraak niet als Public Health Emergency of International Concern (PHEIC) wordt beschouwd. Exit screening, ook op luchthavens en havens aan de Congorivier, is van groot belang. Het instellen van een kostbare en arbeidsintensieve entry screening op internationale vliegvelden heeft momenteel geen meerwaarde voor de publieke gezondheid. Dit besluit zal worden herzien als blijkt dat er sprake is van internationale verspreiding of bij een significante uitbreiding van deze uitbraak. Import in Nederland gerelateerd aan deze ebola-uitbraak is uiterst onwaarschijnlijk, maar niet uitgesloten (bijvoorbeeld gezondheidswerkers die in contact zijn geweest met ebolapatiënten). Voor zover bekend zijn er op dit moment geen Nederlandse gezondheidswerkers in de DRC. Aanvullende informatie is te vinden in de LCI-richtlijn Virale Hermorragische koorts - Filovirussen biedt meer informatie over het ebolavirus, transmissie, klinisch beeld, bestrijdingsmaatregelen en meldingsplicht. De WIP- richtlijnen Isolatie en Virale hemorragische koortsen bieden informatie over strikte isolatie en persoonlijke beschermingsmaatregelen in diverse settings. (Bronnen: WHO, AZG)
Zeer resistente Neisseria gonorrhoeae-stam gevonden bij 2 Australische patiënten
Op 5 april 2018 meldden de Australische gezondheidsautoriteiten 2 Australische patiënten bij wie een zeer resistent (high-level resistence) Neisseria gonorrhoeae-stam was geïsoleerd zonder dat er tussen de patiënten een epidemiologische link was of dat er een duidelijke bron van besmetting kon worden aangetoond. Er zijn aanwijzingen dat 1 patiënt besmet was door een sekswerker in Zuidoost-Azië. De Neisseria gonorrhoeae-stam is resistent tegen penicilline, ciprofloxacine, ceftriaxon (MIC = 0,5 mg / L) en azithromycine MIC> 256 mg / L (resistentie op hoog niveau) en gevoelig voor gentamycine en spectinomycine. De stam lijkt fenotypisch op de Neisseria gonorrhoeae-stam die eerder werd geïsoleerd bij een heteroseksuele man uit Engeland. Ook die stam was zeer resistent voor de eerstelijnsmiddelen azitromycine en ceftriaxon en waarschijnlijk afkomstig uit Zuidoost-Azië. Verspreiding van resistente Neisseria gonorrhoeae-stammen kan de bestaande behandelingsmogelijkheden ondermijnen en de nationale en wereldwijde ziektelast van gonorroe verhogen. (Bronnen: Public Health England, Australische Ministerie van volksgezondheid, ECDC-RT, EPIS-STI)
Patiënten met nosocomiale malaria in verschillende Europese landen
Van januari 2016 tot april 2018 zijn in totaal 6 patiënten met nosocomiale malaria gemeld in Duitsland, Griekenland, Italië en Spanje. 5 patiënten met Plasmodium falciparum en 1 patiënt met een dubbelinfectie met Plasmodium malariae en Plasmodium ovale. Bij alle patiënten is er waarschijnlijk sprake geweest van parenterale transmissie van bloed met Plasmodium spp van malariapatiënten die gelijktijdig met hen waren opgenomen op dezelfde afdeling. Transmissie door bloedtransfusie, beenmergtransplantie of orgaantransplantatie werd uitgesloten.Bij de patiënten in Duitsland, Italië en Spanje werd de transmissie van patiënt naar patiënt aangetoond met moleculaire typering van Plasmodium spp. isolaten. Entomologisch onderzoek in de omgeving van de betrokken ziekenhuizen liet geen malariacompetente muggenvectoren zien.
Nosocomiale malaria is vaak geassocieerd met Plasmodium falciparum, waarschijnlijk door de hogere mate van parasitemie vergeleken met andere Plasmodium spp. De patiënt in Spanje laat echter zien dat ook in ziekenhuizen transmissie van Plasmodium malariae en Plasmodium ovale mogelijk is. Het European Centre for Disease Control and Prevention (ECDC) heeft een risicobeoordeling gemaakt van malaria bestaande uit een uitgebreid literatuuronderzoek en onderwerpen voor epidemiologisch, entomologisch en moleculair onderzoek. Hoewel het risico voor verdere verspreiding door nosocomiale malaria als verwaarloosbaar wordt beschouwd, moeten preventiemaatregelen wel worden geïmplementeerd en nieuwe besmettingen worden gemeld. (Bronnen: ECDC RRA, ProMed)
Auteur
S. Raven, B. Schimmer, Centrum Infectieziektebestrijding, RIVM
Correspondentie
Infectieziekten Bulletin, jaargang 29, nummer 6, juni 2018
Uitbraak van shigellose bij een studentenvereniging
Vanaf 31 maart 2017 kreeg de GGD Haaglanden meerdere meldingen van een infectieziekte veroorzaakt door Shigella bij leden van een studentenvereniging in Delft. De GGD zette een vragenlijst uit onder ongeveer 2000 studenten van de vereniging en het personeel. Het bleek om een ongebruikelijk grote uitbraak te gaan. Alhoewel de bron van besmetting zeer waarschijnlijk in het gebouw van de vereniging was, kon dit niet met zekerheid worden vastgesteld. Waarschijnlijk is er sprake geweest van verschillende besmettingsroutes zoals via toiletgebruik, eten in het restaurant en/of aanwezigheid in de bar van de studentenvereniging.
Uitbraak van shigellose bij een studentenvereniging
Op vrijdag 31 maart 2017 kreeg de GGD Haaglanden 3 meldingen van positieve kweken voor Shigella. Het lukte niet om alle drie besmette patiënten meteen te bereiken. Op maandag 3 april kwam er een vierde melding binnen. Uit de bron- en contactonderzoeken bleek dat alle 4 patiënten lid waren van dezelfde studentenvereniging in Delft en op dezelfde dag ziek waren geworden. Later volgde de vijfde positieve kweekuitslag en kreeg de GGD nog 2 meldingen van een positieve PCR-uitslag (zonder positieve kweek) van Shigella. Alle besmettingen waren,gerelateerd aan dezelfde studentenvereniging. Op grond van de eerste 4 meldingen nam de GGD contact op met het bestuur van de studentenvereniging, de Nederlandse Voedsel- en Warenautoriteit (NVWA) en het Centrum Infectieziektebestrijding (CIb) van het Rijksinstituut voor Volksgezondheid en Milieu (RIVM).
De studentenvereniging heeft een eigen eetgelegenheid/restaurant, dat weliswaar openbaar is maar waar in de praktijk alleen leden eten. Er zijn 2 koks in dienst. In de voorafgaande weken waren er veel studenten met buikgriepachtige klachten geweest. De GGD vermoedde dat dit te maken had met het eten op de vereniging. Op 6 april werd een eerste bericht over dit cluster in het Signaleringsoverleg opgenomen.
Onderzoek
Op 10 april brachten de NVWA en de GGD een bezoek aan de studentenvereniging. Tijdens de inspectie van het restaurant werden door de NVWA tekortkomingen geconstateerd bij de voedselbereiding waarvoor een schriftelijke waarschuwing werd afgegeven. Er werden monsters van diverse producten genomen waarin geen pathogenen werden aangetroffen.
De GGD maakte samen met het verenigingsbestuur een inventarisatie op van de activiteiten en maaltijden op de vereniging in de week voorafgaand aan de eerste ziektedag van de eerste gemelde patiënten (op 31 maart). Eén van de koks had ook maag-darmklachten gehad. Bij hem was door de huisarts fecesonderzoek gedaan en de PCR-uitslag was positief voor Shigella/EIEC. Dit werd niet bevestigd door kweekonderzoek en werd daarom niet bij de GGD gemeld. De eerste ziektedag van de kok was 1 dag na die van de eerste 3 patiënten.
Vragenlijst
Omdat de besmettingsbron vermoedelijk in het gebouw van de vereniging was (geweest) werd besloten om aan alle leden een digitale vragenlijst te sturen. Op grond van de werkhypothese, dat de bron gezocht moest worden op de vereniging in de week van 10 tot 16 maart, werden de casusdefinities geformuleerd (Figuur 1). In overleg met de afdeling epidemiologie werd een vragenlijst opgesteld met vragen over persoonsgegevens, gezondheidsklachten, gezondheidsklachten bij personen in de omgeving, aanwezigheid op de studentenvereniging in de week van 10-16 maart en op de vereniging eten en drinken in deze week. Het was voor de GGD Haaglanden de eerste keer dat er bij een uitbraakonderzoek gewerkt is met een digitale vragenlijst (SurveyMonkey).
Casusdefinitie mogelijke primaire besmettingen |
Casusdefinitie bevestigde primaire besmettingen:Bovenstaande + en een positieve laboratoriumuitslag op Shigella (PCR, kweek) |
Casusdefinitie mogelijke secundaire besmettingen |
Casusdefinitie bevestigde secundaire besmettingen:Bovenstaande + en een positieve laboratoriumuitslag op Shigella (PCR, kweek) |
Figuur 1. Casusdefinities
Op 16 april, 2 weken na ontvangst van de eerste melding werd de vragenlijst verstuurd. Op 25 april stond in de nieuwsbrief van de studentenvereniging een reminder. Uit de teruggestuurde vragenlijsten bleek dat er nog steeds een aantal studenten met gastro-enteritis klachten waren. Er is contact met deze studenten opgenomen en gepoogd diagnostiek te laten verrichten. Helaas is dit door uiteenlopende redenen niet meer gelukt.
Informeren andere betrokken partijen
De huisartsen, de huisartsenpost en de artsen-microbiologen in Delft werden geïnformeerd en werden verzocht om nieuwe verdachte gevallen bij de GGD te melden. Ook de afdeling Communicatie van de Technische Universiteit werd geïnformeerd en dit resulteerde in een verhoogd hygiëneregime en het ophangen van informatie in de toiletten in de gebouwen. Er is geen persbericht uitgegaan en er is niet gereageerd op de sociale media.
Resultaten vragenlijsten
Er zijn 1971 vragenlijsten verstuurd. Hiervan zijn 510 teruggekomen, die ook bruikbaar waren voor de analyses (response 26%). Iets meer dan de helft van de respondenten was man (53,5%). 68% van de respondenten was in de week van 10 t/m 16 maart op de studentenvereniging geweest. Vrijwel alle respondenten hadden daar ook iets gegeten of gedronken en de meesten (85%) waren daar ook naar het toilet geweest. Onder de respondenten met klachten waren iets meer vrouwen dan mannen. Dit verschil was echter niet statistisch significant.
Eerste ziektedag
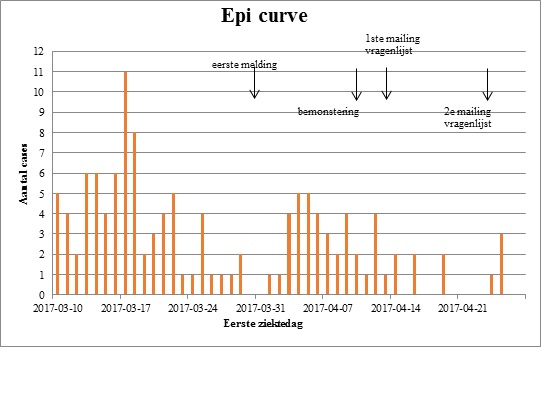
Van de 162 respondenten met diarree of maag-darmklachten vulden 90 de datum van de eerste ziektedag in. Die data liggen tussen vrijdag 10 maart en dinsdag 27 april. Het verloop van de eerste ziektedag laat 2 pieken zien. De eerste op 17 en 18 maart (waaronder de 7 patiënten bij wie de besmetting met laboratoriumonderzoek was aangetoond) en een tweede kleinere piek op 4 en 5 april (Figuur 2).
Figuur 2. Epicurve van patiënten met gastro-enteritisklachten
Diarree
Van de 162 respondenten met gastro-enteritis klachten gaven 117 aan (23% van de respondenten) ook diarree te hebben gehad. 32 respondenten voldeden aan de primaire casusdefinitie en 28 aan de secundaire casusdefinitie. Helaas was dit bij de overgebleven 53 respondenten niet met zekerheid te bepalen, omdat ze niet meer wisten wanneer de klachten begonnen waren en/of wanneer ze op de studentenvereniging geweest waren. Tenslotte waren er nog 45 respondenten met maag-darmklachten zonder diarree.
Aanwezigheid op de vereniging
68% van de respondenten was in de week van 10 t/m 16 maart op de studentenvereniging geweest. De dinsdag en donderdag waren de meest bezochte dagen en woensdag was de rustigste dag. Opvallend was, dat juist onder de groep respondenten die woensdag 15 maart ook op de vereniging gegeten had, significant meer mensen waren die diarree kregen; 13 van hen werden ziek op 17 of 18 maart.Het onderzoek gaf verder inzicht in de dagelijkse gang van zaken op de studentenvereniging:
- het toilet van de keukenmedewerkers wordt soms door studenten gebruikt;
- barpersoneel (studenten) maken hergebruik van glazen zonder deze om te spoelen;
- studenten helpen met het uitdelen van de maaltijden.
- (in dit geval) studenten en stafmedewerkers bleven de vereniging bezoeken terwijl ze maag-darmklachten hadden
De GGD heeft rondom deze zaken een aantal adviezen aan de studentenvereniging gegeven om hier in het vervolg anders mee om te gaan.
Bespreking en conclusie
Het onderzoek had een aantal beperkingen:
- Er zat veel tijd tussen de eerste zieken en het versturen van de vragenlijst, waardoor er mogelijk sprake was van recall bias;.
- Door het anoniem invullen van de vragenlijst was het mogelijk voor respondenten om dit meer keren te doen. Mogelijk omdat het programma tijdens het invullen vastliep. Wij hebben een paar keer een vragenlijst ontvangen die voor een deel was ingevuld, gevolgd door een geheel ingevulde vragenlijst met gedeeltelijk precies dezelfde antwoorden. Wij hebben die gedeeltelijk ingevulde vragenlijsten verwijderd;
- Het was niet verplicht alle vragen te beantwoorden;
- Achteraf gezien was het gekozen tijdsinterval (10-17 maart) te beperkt.
De uitkomsten van het onderzoek laten echter zien dat er sprake is geweest van een ongewoon grote uitbraak. Er waren meer dan 150 patiënten met maag-darmklachten in een tijdsbestek van 2 maanden. Bij 7 patiënten is de ontlasting onderzocht en werd Shigella aangetoond. Er waren 2 pieken in het aantal patiënten: op 17 en 18 maart (de hoogste) en op 4 en 5 april.
Er blijken voor de peildatum van de enquête (10 maart) echter ook al studenten met klachten te zijn geweest. De eerste piek rond 17 en 18 maart werd waarschijnlijk mede veroorzaakt door het eten van voedsel op de vereniging op woensdag 15 maart. Een bron was daarom niet met zekerheid vast te stellen. Norovirus kon worden uitgesloten als oorzaak van de klachten, omdat slechts 14% van de respondenten aangaf ook last van braken te hebben gehad. In geval van een norovirusinfectie had dit rond de 70% moeten liggen. (1) Hoogstwaarschijnlijk is er sprake geweest van verschillende besmettingsroutes zoals via toiletgebruik, voedsel en/of de bar. Dit hebben we niet apart kunnen analyseren.
Voor de GGD Haaglanden zijn de volgende leerpunten uit deze uitbraak naar voren gekomen:
- Het is belangrijk om een digitale enquête zo snel mogelijk uit te laten gaan
- Door het gebruiken van niet-anonieme enquêtes kan de GGD indien nodig respondenten na het invullen van de vragenlijst benaderen. Het is dan mogelijk om werkhypothes bij te stellen. Voor deze casus betekent dit dat de GGD de respondenten zou hebben benaderd die al voor de peildatum van 10 maart klachten hadden.
Auteurs
M. de Boer, M. Petrignani, D. van der Zande, M. Berns, GGD Haaglanden
Correspondentie
Literatuur
1. Kirby A.E. et al. (2016). Vomiting as a Symptom and Transmission Risk in Norovirus illness: Evidence from Human Challenge Studies. PLoS ONE 11(4): e0143759. doi:10.1371/journal.pone.0143759
Een kwalijk luchtje in de werkomgeving
De laatste 3 jaar kreeg GGD Fryslân driemaal een melding van huisartsen over patiënten met een zeer waarschijnlijk arbeidsgerelateerde campylobacterinfectie. Alle patiënten werkten in pluimveeslachterijen of werkten met slachtafval ( bij 3 verschillende bedrijven). Ook een aantal Regionaal Arts Consulenten (RAC’ers)van het RIVM en Regionaal Veterinair Consulenten (RVC’s) van de Nederlandse Voedsel- en Warenautoriteit (NVWA) werd besmet tijdens een bedrijfsbezoek aan een pluimveeslachterij. Uit onderzoek bleek dat zij zeer waarschijnlijk aërogeen besmet waren geraakt. Het is zorgelijk dat de werkomgeving in pluimveeslachterijen en in bedrijven waar men in aanraking komt met slachtafval niet veilig is waardoor werknemers kunnen worden blootgesteld aan biologische agentia. (1,2)
Een kwalijk luchtje in de werkomgeving
Achtergrond
Uit onderzoeken blijkt dat er een structurele onderrapportage is van beroepsziekten.(3) Zo kunnen werknemers van pluimveeslachterijen of mensen die werken met slachtafval, worden blootgesteld aan biologische agentia, zoals Campylobacter jejuni, in aërosolen en kunnen daardoor ziek worden. In Nederland zijn naar schatting 250 000 mensen die werken met dieren en/of dierlijke producten in de voedingsindustrie en landbouw, die werken met afval, of in contact komen met afvalwaterrioolwater en/of proceswater.
Campylobcteriose is een verzamelnaam voor infectieziekten die worden veroorzaakt door de Gram-negatieve bacteriën van het genus(geslacht) Campylobacter. De bacterie is een bekende verwekker van zooönotische infectieziekten. Mensen die besmet raken met Campylobacter kunnen klachten krijgen van diarree, buikpijn, krampen, malaise, koorts, misselijkheid en braken. Als zij daarnaast een gestoorde/incomplete antistofproductie tegen Campylobacter hebben, kan de bacterie in de bloedbaan komen en langdurige gastro-intestinale klachten veroorzaken. Besmetting van mens-op-mens komt vrijwel niet voor.
Campylobacteriose is een meldingsplichtige ziekte groep B2 indien de patiënt behoort tot een groep van 2 of meer patiënten die binnen 24 uur hetzelfde hebben gegeten of gedronken en dezelfde symptomen hebben of bij wie de infectie door laboratoriumonderzoek is bevestigd. (4)
Casus 1
Ongeveer 3 jaar geleden kreeg de GGD een melding binnen over een man die binnen ruim 1 jaar 2 keer gediagnosticeerd was met campylobacteriose door Campylobacter jejuni. Het werk van de man was het reinigen van ruimtes met (pluimvee)slachtafval met een hogedrukspuit. Hij had in de betreffende periode tenminste 3 keer klachten van gastro-enteritis gehad, waarbij 2 keer een kweek was ingezet. Hij had enige tijd niet kunnen werken. Tijdens zijn werk droeg de man een schort, handschoenen, laarzen en een beschermbril. De geadviseerde persoonlijke beschermingsmiddelen in de Arbocatalogus pluimvee (5) zijn adembescherming, handschoenen, overmouwen, schort en een beschermbril. De man had enige bedenkingen om contact te hebben met de GGD omdat hij geen klokkenluider wilde zijn. Hij vermoedde dat er een relatie was tussen zijn infecties met Campylobacter jejuni en het werk dat hij deed. Een ex-werknemer van dit bedrijf meldde dat het gebruikelijk was dat nieuwe medewerkers gastro-enteritisklachten ontwikkelden.
Casus 2
Ongeveer 1 jaar geleden kwam bij de GGD een melding binnen over een patiënt met campylobacteriose door Campylobacter jejuni. De man werkte via een detacheringsbedrijf als monteur van machines voor kippenslachtbedrijven. Hij gaf aan altijd last te hebben van moeheid en brijige ontlasting nadat hij in slachtruimtes had gewerkt. Tijdens zijn werk als monteur droeg hij een overall en handschoenen en betrachtte naar eigen zeggen goede handhygiëne. Vanwege zijn ziekte was hij tijdelijk gestopt met zijn werk als monteur en had administratief werk gedaan totdat hij was hersteld. Het detacheringsbedrijf zou contact opnemen met het kippenslachtbedrijf om maatregelen te bespreken ter voorkoming van nieuwe besmettingen.
Casus 3
Ongeveer een half jaar geleden werd een patiënt gemeld met campylobateriose door Campylobacter jejuni. De man werkte bij een pluimveeslachtbedrijf en was mogelijk al eerder besmet geweest. Hij had toen ook klachten van diarree maar er was geen fecesonderzoek gedaan. De man werkte op verschillende afdelingen van de slachterij. Het bedrijf deed er volgens hem alles aan om een veilige werkomgeving te creëren. Hij gaf niet aan welke maatregelen hiervoor werden gehanteerd.
Casus 4
9 van 14 artsen-consulenten en veterinair consulenten van het RIVM en de NVWA kregen gastro-enteritisklachten 2-4 dagen na een bedrijfsbezoek aan een vleeskuikenslachterij. Tijdens het bezoek waren zij niet in contact geweest met met levende of dode kippen. Bij 4 patiënten werd fecesonderzoek gedaan en werd Campylobacter jejuni aangetoond. Alle 4 patiënten waren waarschijnlijk aërogeen besmet. Alle patiënten droegen tijdens het bezoek een wegwerpoverall, een haarnet en plastic schoenhoezen en een snoetje voor degenen met snor of baard.
Besmettingsroute van alle casussen
Vermoedelijk werden alle patiënten uit bovenstaande 4 casussen aërogeen besmet. Deze besmettingsroute blijkt echter niet in alle campylobacterrichtlijnen te worden genoemd. Zo staat hij niet in de richtlijn van het RIVM en ook niet - althans niet met betrekking tot Campylobacter - in de verplichte risico-inventarisatie & -evaluatie (RI&E) voor werkgevers (5) Daarentegen staan in de Arbocatalogus Pluimvee wel richtlijnen om aërogene besmetting met Campylobacter te voorkomen.
Acties van de GGD
- Casus 1. De GGD heeft 2 keer telefonisch contact gehad met de patiënt over onder andere zijn gezondheidssituatie en persoonlijke beschermingsmaatregelen. De GGD heeft de arbo-arts en de kwaliteitsmedewerker van het bedrijf geïnformeerd over besmettingsroutes van Campylobacter. Ook heeft de kwaliteitsmedewerker advies gekregen over passende beschermingsmaatregelen bij het werken met biologische agentia en het voorlichting te geven aan de medewerkers. RI&E zou binnen een half jaar worden uitgevoerd.
- Casus 2. De patiënt zou zelf met zijn leidinggevende en eventueel arbo-arts overleggen wat te doen om een besmetting met Campylobacter te voorkomen.
- Casus 3. Na éénmalig mailcontact wilde de patiënt geen contact meer hebben met de GGD. De GGD heeft hem geadviseerd contact op te nemen met de arbo-arts over maatregelen om een besmetting te voorkomen.
- Adviseren LCI over het aanvullen van de richtlijn Campylobacter met de aërogene transmissieroute.
Knelpunten
Alle campylobacterbesmettingen in de 4 casussen waren aan arbeid gerelateerd. Ze waren niet meldingsplichtig omdat ze niet gerelateerd waren aan het consumeren van besmet voedsel. De besmettingen werden wel gemeld aan de GGD, maar die kon vanwege het ontbreken van een meldplicht, weinig doen. Ook was er vanuit de patiënten zelf weinig bereidheid om mee te werken aan een oplossing om nieuwe besmettingen te voorkomen. Arbo-artsen zien niet alle werknemers met Campylobacteriose waardoor zij geen goed beeld hebben van de omvang van het probleem.
Conclusie
- Casuïstiek is suggestief voor aërogene transmissie
- Aërogene transmissie blijkt risico voor de gezondheid
- Risicobedrijven zijn bedrijven die met biologische agentia werken zoals pluimveeslachterijen
Aanbevelingen
- Voorlichting over beroepsrisico en veilig werken is nodig.
- Voer structureel een RI&E uit met betrekking tot aanwezigheid en verspreiding van biologische ziekteverwekkers.
- Werk aan bewustwording van medewerkers op mogelijke klachten passend bij Campylobacteriose.
- Werk aan bewustwording van huisartsen en GGD’en met betrekking tot beroepsgerelateerde infecties.
Auteur
G. Broekman, GGD Fryslân
Correspondentie
Literatuur
- Posch J, Feierl G, Wuest G, et al. Transmission of Campylobacter spp in a poultry slaughterhouse and genetic characterisation of the isolats by pulsed-field gel electrophoresis. British Poultry Science. 2006 Jun; 47(3) 286-93
- Marie A de Peiro , R. Todd Niemeier, Seth J. Levine, Karen Gruszynski and John D. Gibbins Campylobacter Infection in Poultry-Processing Workers, Virginia, USA, 2008-2011. CDC-EID journal-Volume 19-Number 2-February 2013
- Infectieziekten en werk. Hoe pak ik dit aan? Preventie van beroepsziekten. Folder RIVM, Ministerie Sociale Zaken en Werkgelegenheid, TNO, 2017
- Richtlijn Campylobacter-infecties LCI RIVM
- Arbocatalogus Pluimvee van Sociale Zaken Pluimvee Industrie
Infectieziekten Bulletin, jaargang 29, nummer 6, juni 2018
Het gebruik van antibiotica binnen de Haagse verpleeghuiszorg: een bittere pil of niet…….?
Bacteriële ongevoeligheid voor gangbare antibiotica rukt in een rap tempo vanuit het buitenland op en wint helaas ook in eigen land gestaag terrein. De problematiek alhier manifesteert zich het meest nadrukkelijk binnen intramurale zorginstellingen, waar de antibioticumconsumptie hoog is en de infectieziektedruk groot. Beide omstandigheden gaan naast ziekenhuizen ook op voor verpleeghuisinstellingen. (1) Verpleeghuizen dragen immers zorg voor een uiterst kwetsbare patiëntengroep, die ook nog eens frequent met de ziekenhuizen wordt uitgewisseld. ( 2) Wij hebben daarom onderzocht hoe de specialist ouderengeneeskunde bij het starten van een antibiotische behandeling tot zijn besluiten komt en welke bijbehorende maatregelen hij inzet. Wat zijn de determinanten, die bij dit afwegingsproces een rol spelen, welke factoren beïnvloeden zijn uiteindelijke keuze voor een specifiek antibioticum en biedt het bestaande beleid ruimte voor verbetering? In het artikel beschrijven we eerst de opzet van het onderzoek en vervolgens de bevindingen die uit de interviews met de artsen naar voren zijn gekomen. Het eindigt met enkele aanbevelingen om binnen deze zorgsector tot een uniformer en beter gestructureerd antibioticumbeleid te komen.
Het gebruik van antibiotica binnen de Haagse verpleeghuiszorg: een bittere pil of niet…….?
Overmatig antibioticumgebruik en internationaal personenverkeer werken resistentievorming in de hand. Een daarbij komende complicerende factor is het feit dat er de voorbije halve eeuw nauwelijks nog nieuwe antibiotica aan het therapeutisch arsenaal zijn toegevoegd. Het ontwikkelen van nieuwe generaties antibiotica zal in het ontstane tekort moeten gaan voorzien, maar dit is een kostbaar en langdurig proces, dat voor het keren van de toenemende resistentievorming eigenlijk nu al niet meer volstaat. (3)
Een maatregel die wel op korte termijn effect moet sorteren, is het promoten van antibiotic stewardship: het geheel van onderzoeken, afspraken en interventies dat tot een zo optimaal mogelijk antibioticumgebruik moeten leiden. Met een suboptimaal of onjuist antibioticumgebruik bedoelt men doorgaans een omstreden indicatie voor het inzetten van een antibiotische behandeling, een inadequate voorschrijfduur of een dubieuze keuze voor het toegepaste antibioticum zelf. De ministeriële doelstellingen, die in juni 2015 zijn geformuleerd, zijn zonder meer ambitieus te noemen: het streven is om in het kader van antibiotic stewardship het aantal verkeerd voorgeschreven antibiotica binnen 5 jaar tijd met 50 % terug te dringen. Binnen diezelfde periode moet ook het aantal vermijdbare en aan zorg gerelateerde infecties tot de helft zijn teruggebracht. (4)
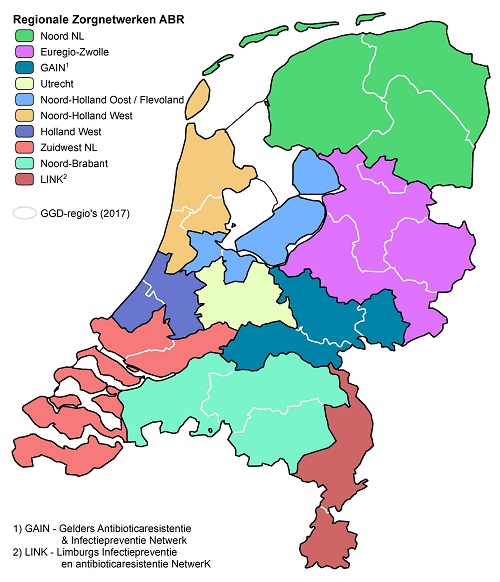
De beoogde stewards zijn niet alleen de voorschrijvende artsen, maar ook andere zorgprofessionals die bij het tegengaan van verspreiding van resistente micro-organismen een taak in het werkveld hebben. Zij krijgen ondersteuning van 10 Regionale Zorgnetwerken Antibioticaresistentie (ABR), die middels coördinatie, advisering en onderzoek mede invulling aan dit streven moeten geven. (5) Het geografisch bereik van deze teams komt overeen met het verzorgingsgebied van het Regionaal Overleg Acute Zorgketen (ROAZ). Het besluit om de schaalgrootte van de Regionale Zorgnetwerken ABR te koppelen aan die van de regionale samenwerkingsverbanden voor de acute zorg is een rationele keuze geweest, aangezien het gros van de verwijzingen en overplaatsingen zich binnen de grenzen van dit verzorgingsgebied afspeelt. Het Regionale Zorgnetwerk ABR Holland West (figuur 1) omvat de GGD-en Haaglanden en Hollands Midden. Het heeft een specialist ouderengeneeskunde in de kerngroep die als liaison voor zijn beroepsgroep optreedt. Alle verpleeghuizen die aan dit onderzoek hebben deelgenomen maken deel van dit regionetwerk uit.
Figuur 1. De 10 regionale zorgnetwerken antibioticaresistentie (6)
Onderzoeksmethode
Het door ons verrichte onderzoek is kwalitatief van opzet, waarbij we voor de interviews met de specialisten ouderengeneeskunde gebruik hebben gemaakt van een semigestructureerde vragenlijst. We hebben toestemming gekregen om de vragenlijst, die door Laura van Buul werd opgesteld voor haar promotieonderzoek, in onze eigen vragenlijst op te nemen. Van Buul heeft in 2015 onderzoek gedaan naar het voorschrijven van antibiotica aan ouderen in verpleeghuizen. De vraagstelling komt dus overeen maar het werkveld, waarop het promotieonderzoek zich heeft gericht was veel breder omdat Van Buul ook verzorgingshuizen heeft betrokken en artsen en verpleegkundigen heeft ondervraagd. (7)
Onze vragenlijst focust op de praktische omgang met het voorschrijven van antibiotica en op het beleid binnen de eigen verpleeghuisinstelling. De semi-gestructureerdheid van de lijst en de face-to-face-interviews boden ons gelegenheid om nader in te gaan op meer subjectieve aspecten, zoals de persoonlijke betrokkenheid bij resistentieproblematiek en de manier waarop de respondent de samenwerking met anderen op dit gebied waardeert. De grootte van de studiepopulatie hing af van het moment van informatieverzadiging. De interviews zijn gehouden door een arts en een onderzoeker. De specialisten ouderengeneeskunde zijn in hun eigen werkomgeving geïnterviewd en hebben toestemming gegeven om de gesprekken op te nemen. Om een goed inzicht te krijgen in de subjectieve aspecten, hebben we bewust geprobeerd om tijdens de gesprekken een sfeer van vertrouwelijkheid te creëren. Wij hebben ons bij onze vraagstelling niet door een normatief of belerend kader hebben laten leiden.
Resultaten
Wij hebben in de tweede helft van 2016 10 verpleeghuizen bezocht. Bij 5 verpleeghuizen werden de specialist ouderengeneeskunde en de zaalarts ondervraagd. De laatsten waren op dat moment nog basisarts of specialist ouderengeneeskunde in opleiding. Alle verpleeghuizen hebben zowel somatische als psychogeriatrische afdelingen, 1 verpleeghuis heeft ook de beschikking over een revalidatie-unit. Acht huizen maken onderdeel uit van een koepel, de andere 2 zijn particuliere huizen, die zich bij de inschrijving op sociaal specifiekere doelgroepen hebben gericht. Bij de keuze voor de verpleeghuizen hebben wij rekening gehouden met het aantal bedden en met de geografische verdeling binnen de regio Haaglanden. De belangrijkste bevindingen staan hieronder in 8 onderwerpen weergegeven; citaten zijn enkel dan aangehaald, wanneer ze een breder gedragen opvatting representeren. Wij hebben bemerkt dat er na 15 interviews een verzadiging in de informatie-inwinning op trad.
Urgentiegevoel
Bij de specialisten ouderengeneeskunde is het besef terdege aanwezig dat antibioticumresistentie een toenemend gezondheidsprobleem is en dat verpleeghuizen hierbij een belangrijke rol spelen. De bereidwilligheid om aan dit onderzoek deel te nemen was dan ook groot. Daar staat dan wel tegenover dat het probleem doorgaans niet als bijzonder urgent wordt ervaren: ‘resistente bacteriën zijn niet altijd ziekmakend en er is tot op heden nog altijd wel een antibioticum dat werkt’. Mogelijk is dit gevoel voor een deel gebaseerd op het feit dat er tot op dat moment in geen van de ondervraagde verpleeghuizen een grote uitbraak was geweest veroorzaakt door resistente bacteriën. De beruchte carbapenemaseproducerende enterobacteriaceae (CPE) , die praktisch voor ieder antibioticum ongevoelig is geworden, heeft zich nog niet in deze regio aangediend.
De respondenten zijn terughoudend zijn met het voorschrijven van antibiotica. Zij zijn ook van mening dat Nederland vooroploopt, wanneer het gaat om de aanpak van en aandacht voor resistentieproblematiek. Sommige respondenten geven aan dat de huidige situatie acceptabel is en dat doorgaan op dezelfde voet niet per sé onverantwoord is. Zij vragen zich af of het afdwingen van al te veel of al te rigoureuze beleidsveranderingen wel zoveel meerwaarde heeft.
Op de vraag of het een goed idee zou zijn om opgenomen patiënten te screenen op resistente micro-organismen, reageert 1 respondent positief. De meeste andere respondenten schrikken hiervoor terug, vooral omdat zo’n opsporingsactie de ‘doos van Pandora’ zou kunnen openen die zich daarna niet meer zo gemakkelijk laat sluiten.
Enkele respondenten hechten eraan te wijzen op de verbeteringen, die in de afgelopen jaren op het gebied van de bestrijding van antibioticaresistentie al zijn bereikt. Zo is men - al dan niet gedwongen - kritischer geworden op het handhaven van hygiënestandaarden en het gebruik van breedspectrumantibiotica. Alle respondenten beschouwen de antibiotische behandeling van een klachtenvrije patiënt met bacteriën in de urine, tegenwoordig als een ‘kunstfout’.
Voorschrijfgedrag
Het besluit om een bepaald antibioticum voor te schrijven is het sluitstuk van een afwegingsproces. Dit gaat in principe aan elk behandelbesluit vooraf en is niet voorbehouden aan de verpleeghuiszorg. Wel benoemen de respondenten enkele sectorspecifieke factoren die binnen het verpleeghuis zwaarder wegen dan elders:
- De patiënt en zijn familie hebben een grotere invloed op het behandelplan dan in een ziekenhuis gebruikelijk is, ook al worden behandelplannen doorgaans al voordat de patiënt in het verpleeghuis komt, tijdens de intakegesprekken besproken. Gelet op de medische problematiek is curatie lang niet altijd doel op zich maar wordt er vaak voor een palliatieve behandeling gekozen. (8)
- De verzorgenden spelen een prominente rol in de besluitvorming omdat zij als ‘ogen en oren’ van de behandelaar vaak de eersten zijn om veranderingen in gedrag en conditie van patiënten op te merken en te rapporteren.
- Niet alle verpleeghuizen beschikken over voldoende diagnostische hulpmiddelen. Dit bemoeilijkt het maken van een risico-inschatting en de uiteindelijke antibioticumkeuze. Specialisten ouderengeneeskunde werken doorgaans zelfstandig en maken meestal zelf de afweging om al dan niet een behandeling in te zetten. Zij geven aan dat ze zich houden aan de protocollen van de Vereniging van Specialisten Ouderengeneeskunde (Verenso) of aan de instellingsgebonden formularia die hiervan zijn afgeleid.
Urineweginfecties
Urineweginfecties zijn de meest voorkomende infectieziekten binnen de verpleeghuiszorg. (9) Uit het promotieonderzoek van Van Buul bleek dat bij 32% van de verpleeghuispatiënten met een urineweginfectie er sprake was van een dubieuze antibioticumkeuze. (10) Dit percentage is aanmerkelijk hoger dan bij luchtweg- of huidinfecties (respectievelijk 13 en 6 %). De diagnostiek en medicamenteuze behandeling van urineweginfecties kregen in de interviews dan ook onze bijzondere aandacht.
Alle respondenten hebben ruime ervaring met de behandeling van urineweginfecties vanwege de hoge incidentie. Dit betekent echter niet dat het een aandoening is die gemakkelijk te diagnosticeren of te behandelen is. De Verenso-richtlijn Urineweginfecties biedt de behandelaar een aanzienlijke mate van handelingsvrijheid omdat de symptomatologie juist bij deze patiëntengroep vaak moeilijk te beoordelen is en de nodige subjectieve interpretatie toelaat. Die handelingsvrijheid uit zich onder meer in de keuze uit verschillende vervolgdiagnostiek en de keuze uit verschillende antibiotica. De urinekweek is nog altijd de gouden standaard maar wordt door de respondenten wisselend toegepast. Als nadeel van de urinekweek worden onder andere de relatief hoge kosten en de niet direct beschikbare uitslag genoemd. Daarnaast is er voor een betrouwbare bepaling bij voorkeur vers geloosde urine nodig en dit is bij deze patiënten vaak alleen met een katheterisatie of een blaaspunctie te verkrijgen is. Deze praktische bezwaren werpen drempels op die van verpleeghuis tot verpleeghuis en van behandelaar tot behandelaar verschillen.
Het verbaast mij dat er nog steeds collega's zijn die geen dipslide inzetten, maar die gewoon altijd kweken of juist nooit. Dan ik denk van: ‘joh, je bent ook nog eens een dief van je eigen portemonnee (specialist ouderengeneeskunde)
Niet-medische determinanten
De meeste artsen beschouwen hun somatische en psychogeriatrische afdelingen niet in de eerste plaats als klinische behandelcentra maar vooral als een leef- en woonomgeving waarin ernstig beperkte patiënten hun laatste levensperiode doorbrengen. Sociaal en fysiek beperkende maatregelen zoals langdurige verzorging door verpleegkundigen in beschermende kleding of afzondering van medepatiënten door contactisolatie, staan op gespannen voet met het gevoel van huiselijkheid dat men in deze laatste levensfase nastreeft. In die zin weegt het belang van de individuele patiënt bij de meeste respondenten vooralsnog zwaarder dan het veelal onbekende risico op horizontale transmissie naar contactpersonen binnen en buiten het verpleeghuis.
De meeste respondenten vinden in het management van hun eigen verpleeghuis geen vanzelfsprekende bondgenoot bij het terugdringen van antibioticumresistentie en het bevorderen van infectieziektepreventie. Screening, uitbraakbestrijding en geïsoleerde verpleging zijn volgens het management niet alleen belastend voor de patiënt maar ook nog eens kostbaar en arbeidsintensief.
Ook voor de verpleegkundigen heeft de verzorging van een patiënt met een besmetting door een resistente bacterie aanzienlijke consequenties. Extra hygiënemaatregelen trekken een zware wissel op de toch al schaarse zorgcapaciteit en kunnen de zorgcontinuïteit op een afdeling gemakkelijk verstoren. De inbreuk die deze maatregelen maken op de huiselijke sfeer is al eerder benoemd. De meeste artsen zijn terughoudend om al te snel of al te uitgebreid een contactonderzoek op te zetten.
Volgens sommige respondenten moet het tekort aan financiële ruimte en de personele krapte eerst structureel opgelost worden voordat de focus effectief naar andere aandachtsgebieden kan worden verlegd. Verbeterprojecten, zoals een strikter hygiënebeleid of oefening in infectieziektepreventie, verliezen hierdoor aan aandacht en prioritering. Het tekort aan financiële ruimte roept nogal eens een gevoel op van moedeloosheid en wordt vooral door de meer ervaren artsen als een belemmerende factor gezien. Eén van hen verzucht zelfs dat de immunologische weerbaarheid van ouderen dramatisch zou verbeteren wanneer er maar voldoende personeel zou zijn waardoor zijn nog mobiele patiënten dagelijks een rondje om het huis kunnen lopen.
Verzorgend personeel
De respondenten geven in de regel hoog op over de inzet en betrokkenheid van het verzorgend personeel. Toch merkt een aantal van hen op dat de buitenwereld nogal eens de neiging heeft om het verpleegkundig niveau binnen een verpleeghuisinstelling te overschatten. Goed gekwalificeerd personeel is moeilijk te werven en vast te houden. Wanneer er al hbo-verpleegkundigen in dienst zijn, dan stromen die doorgaans snel naar de meer beleidsmatige functies door. De directe zorg aan bed komt daarmee in handen van verzorgenden met een mbo-opleiding en dit stelt grenzen aan wat erop preventief, diagnostisch en communicatief gebied van hen mag worden verwacht. Bijscholing en structurele oefening in hygiënisch werken zijn voorwaarden om de kwaliteit van zorg naar een hoger plan te tillen. Maar ook dan blijft het basale opleidingsniveau van verzorgenden onverminderd een punt van zorg.
Het klinkt misschien gek maar in verpleeghuisland is een groot deel van de zorg zorgniveau 2. Niveau 2, dan moet je je een monteur voorstellen, die in de autogarage de banden onder de auto mag zetten, maar niet aan de motor mag komen. Bij ons moeten ze in één keer wel heel veel kunnen in dat verpleeghuis. Dat is niks ten nadele maar het is misschien net iets te veel (specialist ouderengeneeskunde in opleiding)
Regionaal niveau opererend zorgnetwerk
Een meerderheid van de respondenten geeft aan dat ze de komst en sturing van een Regionaal Zorgnetwerk ABR zeker zouden accepteren. Sommigen geven zelfs aan dat ze dit van hogerhand ook min of meer verwachten. Zo bestaat er een algemene bereidheid om zich aan regionaal beleid te confirmeren wanneer een specifieke ontwikkeling op resistentiegebied hiertoe zou nopen. Bijvoorbeeld, als de microbioloog op basis van een lokaal resistentiepatroon zou aanraden om bij een infectieziekte over te schakelen op een ander antibioticum dan het antibioticum van eerste keus, dan zijn de artsen zonder meer bereid om aan dit advies gehoor te geven. De belangrijkste voorwaarde is wel dat die wijziging helder wordt gecommuniceerd en ook door de gehele zorgregio wordt gedragen én nageleefd.
Intercollegiale toetsing
Wat tijdens de interviews opviel was dat binnen verpleeghuizen een aanspreekcultuur veelal ontbreekt. Dit fenomeen doet zich met name voor tijdens avond- en weekenddiensten wanneer artsen voor elkaar waarnemen, maar het gebeurt zeker ook binnen het eigen verpleeghuis. Enkele respondenten geven aan soms bedenkingen te hebben bij het antibiotische behandelbeleid van hun collega’s. Toch zijn ze eerder geneigd om een al opgestarte therapie voort te zetten dan om die bij hun collega ter discussie te stellen.
Je respecteert ook wel heel erg de keuze van je collega’s. Ik zie ook wel eens Ciproxin voorbij komen, waarvan ik denk: moet dat nu echt? Maar dan ga ik dat toch ook weer niet direct bevragen (specialist ouderengeneeskunde)
Ook tussen ziekenhuizen en verpleeghuizen ontbreekt een aanspreekcultuur. Dit is het geval als patiënten na verblijf in het ziekenhuis (terug)komen in het verpleeghuis. Wellicht speelt de hiërarchie tussen ziekenhuizen en verpleeghuisinstellingen hierbij een rol. Illustratief hiervoor is de toelichting van een van de respondenten die zijn klinische loopbaan in de verpleeghuiszorg afsluit. Hij schrikt er niet voor terug om in te grijpen in de medicatielijst die zijn patiënten uit het ziekenhuis mee krijgen, ook niet wanneer het om de antibiotische onderhoudsbehandeling van urineweginfecties gaat.
Interventiebeleid
In het tweede deel van haar proefschrift heeft Van Buul een interventieprogramma opgesteld waarvan de onderdelen in onderstaande tabel zijn weergegeven. (7) Het interventieprogramma is door Van Buul bij 5 verpleeghuizen en 2 verzorgingshuizen geïmplementeerd en na een half jaar geëvalueerd. Het bleek dat het voorschrijfgedrag ten aanzien van antibiotica bij geen van de deelnemende verpleeghuizen significant was veranderd of verbeterd.
Tabel 1. Interventieprogramma uit het proefschrift van L. van Buul
Interventies |
| Verbetering van de kennis van artsen |
| Verbetering van de communicatie tussen de artsen en de verpleging |
| Optimaliseren van het medicatiereview |
| Begrijpen van een lokaal resistentiepatroon |
| Verhogen van gebruik van diagnosemiddelen |
| Verbetering van de samenwerking tussen artsen in een waarneemgroep |
Wij hebben met de respondenten de interventies doorgenomen en hen daarna expliciet gevraagd, waarom zij denken dat die niet tot de beoogde resultaten hebben geleid. Nagenoeg alle respondenten vinden het door Van Buul opgestelde interventieprogramma zinvol. De meerwaarde van het verbeteren van de communicatie met de verpleegkundigen wordt door sommigen in twijfel getrokken omdat die ruimschoots voldoet. De respondenten kunnen geen andere interventies bedenken die van toegevoegde waarde zouden kunnen zijn. Eén respondent is van mening, dat de evaluatietijd van een half jaar te kort was om uitspraken te doen: het vraagt meer tijd om ingesleten patronen bij te stellen en het welslagen van een interventieprogramma hangt vooral ook af van het herhalen van de boodschap.
Conclusies
De respondenten zijn zich bewust van de ABR-problematiek en de cruciale positie die verpleeghuizen hebben binnen de zorgketen. Er is sprake van een algemene bereidheid om zich aan regionale afspraken te confirmeren. Het urgentiebesef is niet bijzonder hoog: ABR is niet minder belangrijk, maar zeker ook niet belangrijker dan de vele andere problemen waarmee zij in hun praktijk geconfronteerd worden. Zij herkennen zich niet in het beeld dat er in hun manier van voorschrijven of werken dramatische veranderingen nodig zijn om de trend van toenemende antibioticaresistentie te keren.
De ook binnen de regio veelgehoorde noodkreet om meer financiële armslag is inmiddels politiek gehonoreerd. De regering heeft toegezegd om in de komende kabinetsperiode 2 miljard extra in de intramurale ouderenzorg te investeren. Het tekort aan goed geschoold personeel zou in de nabije toekomst nog wel eens een nijpender probleem kunnen worden dan het tekort aan financiële middelen zelf. Het gaat bij het effectief tegengaan van antibioticaresistentie immers niet uitsluitend om voldoende handen aan bed maar net zo goed om voldoende gekwalificeerde handen aan bed. Aanvullende scholing en vooral repeterende oefening in hygiënisch werken zullen de te verwachten lacunes in kennis en vaardigheid op dit gebied moeten opvullen.
Het aanleren en toepassen van een adequater voorschrijfgedrag is een proces dat tijd kost. Ons onderzoek toont aan dat er binnen de verpleeghuiszorg meerdere medische, logistieke en zelfs morele factoren zijn, die een snelle en soepele aanpassing van voorschrijfgedrag in de weg staan. Deze bezwaren zijn over het algemeen legitiem en een deel van de problematiek speelt zich ook af in verpleeghuizen. Het is daarom noodzakelijk om sturing en begeleiding te bieden.
Aanbevelingen.
Specialisten ouderengeneeskunde werken relatief zelfstandig en sommige respondenten beschouwen dit ook als een van de charmes van het vak. Door verschillen in schaalgrootte en organisatiestructuur zijn strengere uniforme controlesystemen, zoals die binnen ziekenhuizen worden gehanteerd, niet zonder meer toe te passen in verpleeghuizen.
Een praktisch alternatief is om ten minste 1 keer per jaar een farmacotherapeutisch overleg te agenderen dat uitsluitend in het teken van antibioticumgebruik en antibioticumresistentie komt te staan. De regionale microbioloog en de toeleverende apotheker zouden aan een dergelijk overleg een actieve bijdrage moeten leveren. Inventarisatie van regionale kweekresultaten geeft inzicht in lokale verwekkers en een overzicht van plaatselijke kengetallen maakt een vergelijking mogelijk van het antibioticumgebruik tussen afzonderlijke verpleeghuizen. Het doel van deze regionale surveillance van antibioticaresistentie is dat door een kritische beschouwing de uitschieters in het gebruik zullen afvlakken en de kengetallen op de middellange termijn in zowel kwalitatief als kwantitatief opzicht naar elkaar zullen toegroeien.
Het is van het grootste belang om de diagnosemiddelen bij vooral urineweginfecties te uniformeren en duidelijk aan te geven wanneer ze moeten worden ingezet. Op dit moment is het inzetten van de middelen nog relatief willekeurig.
De Verenso-protocollen zijn veelal afgeleid van de standaarden van het Nederlands Huisartsen Genootschap (NHG). Sommige respondenten zouden deze nog nadrukkelijker op de specifieke karakteristieken van de hun patiëntenpopulatie toegespitst willen zien. Omdat de verzorgenden een grote invloed hebben op het besluitvormingsproces bij de behandeling van urineweginfecties, is het advies om ook hun aandeel hierin protocollair vast te leggen.
Het bijeenbrengen van alle betrokken disciplines binnen een regionaal zorgnetwerk antibioticaresistentie biedt een unieke gelegenheid voor het onderhouden van korte lijnen en het opzetten van vraaggericht onderzoek. Goede onderlinge afstemming moet er dan toe leiden dat best practices breed worden gedeeld en dat de resultaten van lokale projecten ook bijdragen aan landelijke beleidsafspraken en consensusvorming.
Antibiotic stewardship is meer dan uitsluitend een ‘academische exercitie’. Het nastreven van stewardship heeft immers betrekking op vrijwel iedere werknemer die binnen de zorgsector werkzaam is. Zo zijn het promoten van handhygiëne en het maken van een (cultuur)omslag naar ‘schoner’ werken de hoekstenen van dit beleid. Dit laatste gaat zeker ook op voor de verpleeghuiszorg omdat incontinentieproblematiek hier nadrukkelijk aan de orde is. Bovendien zijn zowel de prevalentie van resistente micro-organismen alsook de risico’s op intramurale transmissie er nog grotendeels onbekend.
Een laatste aanbeveling is om ook het niet-medisch management veel nadrukkelijker bij dit proces te betrekken dan tot dusverre gebeurt. De problematiek en de nadelige gevolgen van antibioticaresistentie ‘blijven’ nu nog teveel op de werkvloer en worden door het management vooral als een onwelkome kostenpost beschouwd. Ook bij het management moet het besef doordringen dat de bestrijding van antibioticaresistentie niet alleen een zaak is binnen verpleeghuizen maar ook het algemene publiek aangaat.
Dit onderzoek werd mede mogelijk gemaakt door financiële steun vanuit het programmabudget van het project Regionale Ondersteuning van het RIVM Centrum Infectieziektebestrijding
Auteurs
C.G. Dirksen 1, R. van Veldhuizen 2, R. Brugmans 1
- GGD Haaglanden
- Radboud Universiteit, Nijmegen
Correspondentie
Riany.Brugmans@ggdhaaglanden.nl
Literatuur
- Van Buul LW, van der Steen JT, Veenhuizen RB, Achterberg WP, Schellevis FG et al.. Antibiotic use and resistance in long-term facilities. Journal of the American Medical Directors Association 2012 Jul. 31: 13 (6): 568:e1-13
- Laxminarayan R, Duse A, Wattal C, Zaidi AK et al. Antibiotic resistance-the need for global solutions. The Lancet Infectious Diseases 2013 Dec 31:13 (12): 1057-98
- Gill EE, Franco OL, Hancock RE Antibiotic adjuvants: diverse strategies for controlling drug resistant pathogens. Chemical Biology & Drug Design. 2015 Jan 1: 85(1): 56-78.
- Ministerie van Volksgezondheid, Welzijn en Sport. Kamerbrief van 24 juni 2015 betreffende de aanpak van antibioticaresistentie (https://rijksoverheid.nl/onderwerpen/antibioticaresistentie/inhoud/antib... in-de- gezondheidszorg)
- Brugmans R, van der Zouwe N. Zorgnetwerk Antibioticaresistentie Holland West’ van start. Epidemiologisch Bulletin 2017 nummer 3: 21-25
- Ministerie van Volksgezondheid, Welzijn en Sport. Factsheet Regionale zorgnetwerken, (https://www.actiz.nl/stream/factsheet-zorgnetwerken-abr-16-mei-2017.pdf)
- Van Buul LW. How to impact antibiotic prescribing? A contribution to antibiotic stewardship in long-term care(Proefschrift VU Amsterdam, mei 2015
- Hendriks SA. Understanding the clinical course of dementia. A search to optimize palliative care for nursing home residents. Proefschrift V U Amsterdam, april 2017
- Went P, Achterweg W, Brugging R, van Veelen J e.a. Verenso-protocol, richtlijn Urineweginfecties mei 2006
- Van Buul LW, Veenhuizen RB, Achterberg WP, Schellevis RG et al. Antibiotic prescribing in Dutch nursing homes: how appropriate is it? Journal of the American Medical Directors Association 2015 Mar1: 16 (3): 229-37
- https://www.zorgvoorbeter.nl/hygiene/inspectie-gezondheidszorg Inspectie Gezondheidszorg en Jeugd (IGJ), Zorg voor Beter, kennisplein voor verpleging, verzorging, zorg thuis en eerste lijn, oktober 2017
- Van Buul LW, Sikkens JJ, Van Agtmael M. A et al. Participatory action research in antimicrobial stewardship: a novel approach to improving antimicrobial prescribing in hospitals and long- term facilities Journal of Antimicrobial Chemotherapy 2014 July, Vol. 69 I 7 p1734-41
Infectieziekten Bulletin, jaargang 29, nummer 6, juni 2018
Veranderingen in pathogenen en pneumokokkenserotypen bij patiënten met een thuis opgelopen pneumonie
Sinds de invoering van pneumokokken conjugaatvaccins in het Rijksvaccinatieprogramma (RVP) is de incidentie van invasieve pneumokkenziekte in Nederland netto gedaald, ondanks het feit dat er sprake was van een toename van niet-vaccin serotype ziekte. Bij kinderen en ook bij ouderen wordt de daling in invasieve pneumokkenziekte toegeschreven aan groepsimmuniteit. De bevindingen beschreven in dit artikel tonen dat er ook sprake lijkt te zijn van dergelijke groepsimmuniteit bij volwassenen opgenomen met een thuis opgelopen pneumonie zonder invasieve pneumokkenziekte.
Veranderingen in pathogenen en pneumokokkenserotypen bij patiënten met een thuis opgelopen pneumonie
Invasieve pneumokkenziekte (IPZ) is gedefinieerd als een infectie door de bacterie Streptococcus pneumoniae van een normaal steriele lichaamsvloeistof, zoals bloed en liquor cerebrospinalis. In 2006 werd het 7-valente pneumokokkenconjugaatvaccin (PCV7) ingevoerd in het RVP). PCV7 heeft de potentie om bescherming te bieden tegen 7 van de ruim 90 pneumokokkenserotypen. In tegenstelling tot pneumokokkenpolysacharidenvaccins zijn conjugaatvaccins in staat om T-celimmuniteit op te wekken waardoor antistoffenbescherming al op jonge leeftijd kan optreden. PCV7 werd in 2011 vervangen door een 10-valent vaccin (PCV10) wat bescherming kan bieden tegen 10 serotypen. Uit surveillance door het RIVM is gebleken dat de incidentie van IPZ na invoering van PCVs is gedaald. In de gevaccineerde leeftijdsgroep (kinderen < 5 jaar) is er sprake van een sterke IPZ-incidentiedaling (van 18.6 naar 7.8 patiënten / 100.000 per jaar). Verder daalde de IPZ-incidentie bij ouderen ≥ 65 jaar door groepsimmuniteit (van 57.6 naar 49.0 patiënten / 100.000 per jaar). De daling van IPZ-incidentie in zowel gevaccineerde- als niet-gevaccineerde leeftijdsgroepen is het gevolg van een afname van vaccinserotypedragerschap in kinderen, waardoor er minder verspreiding in de gemeenschap optreedt (groepsimmuniteit). Ondanks een toename van de incidentie van dragerschap van serotypen waartegen de vaccins niet beschermen en ziekte, is er sprake van een netto IPZ-incidentiedaling.(2,3) (1,2)
Bij volwassenen die in het ziekenhuis worden opgenomen vanwege een thuis opgelopen pneumonie (community-acquired pneumonia, hierna afgekort als CAP) is S. pneumoniae in Nederland de meest aangetoonde verwekker (16%-37%).(3,4) Naar schatting is bij ongeveer 25% van de pneumokokken-CAP-patiënten sprake van een bacteriemie. De meeste van deze patiënten (ongeveer 75%) hebben dus een niet-invasieve ofwel niet-bacteremische pneumokokken-CAP.(5)
Wat het effect is van de pneumokkenvaccinatie van kinderen op pathogeen- en serotypeverdeling bij volwassenen, die opgenomen zijn vanwege een niet-bacteremische (pneumokokken-)CAP, is minder duidelijk. Twee studies onder volwassen patiënten die hiervoor opgenomen waren toonden eerder aan dat vaccinatie van kinderen bescherming lijkt te bieden tegen 7 respectievelijk 13 serotypen waartegen de 2 onderzochte vaccins (PCV7 en PCV13) bescherming zouden moeten bieden. (6,7)
Onduidelijk is of er in Nederland vergelijkbare effecten zijn opgetreden na de introductie van PCV10 in het RVP. Bovendien zouden veranderingen in het aantal patiënten met pneumokokken-CAP gevolgen kunnen hebben voor de pathogeenverdeling in CAP als geheel. Het doel van dit onderzoek was om deze 2 zaken op te helderen.
Opzet/methode
Het onderzoek werd uitgevoerd met data van 3 prospectieve studies (1 cohort en 2 gerandomiseerde trials) onder volwassen patiënten die in het ziekenhuis waren opgenomen met een CAP. Deze 3 studies werden uitgevoerd in de periode voor en na opname van de pneumokkokkenvaccinaties in het RVP (cohort 1 = pre-PCV7; oktober 2004 - augustus 2006, n=201), na aanvang van PCV7 (cohort 2 = PCV7 (en pre-PCV10); november 2007 en juni 2009, n=304) en na aanvang van PCV10 (cohort 3 = PCV10; oktober 2012 en oktober 2016, n=300). De inclusie- en exclusiecriteria van de 3 studies waren vergelijkbaar. (8,9, 10) De patiënten in alle 3 studies waren volwassenen met een radiologisch bewezen CAP. De meeste waren in het St. Antonius Ziekenhuis opgenomen. De belangrijkste verschillen in criteria waren dat er in cohort 1 patiënten zaten die direct waren opgenomen op een intensivecareafdeling of een indicatie hadden voor systemische corticosteroïden (of huidig gebruik hiervan). In de andere 2 cohorten werden deze patiënten geëxcludeerd.
In alle cohorten werd uitgebreide conventionele microbiologische diagnostiek ingezet: sputum- en bloedkweken, urineantigeentesten op Streptococcus pneumoniae en Legionella pneumophila en PCR-testen (polymerase chain reaction) op keelswabs en/of sputum voor atypische pathogenen (Mycoplasma pneumoniae, Legionella pneumophila, Coxiella burnetii, Chlamydophila pneumoniae en Chlamydophila psittaci). Daarnaast werd een aantal patiënten, afhankelijk van het cohort, getest op virale respiratoire verwekkers met serologische testen, viruskweken of PCR.
Bij de patiënten van wie er een vroeg of laat serummonster beschikbaar was, werden aanvullend serotypespecifieke pneumokokkenantistoffen gemeten (vergelijking van titers in serum dat in een vroeg en een later stadium van de ziekte werd afgenomen). Met deze methode kon door middel van specifieke titerstijgingen (voor 14 serotypen) ook de diagnose pneumokokkenpneumonie worden gesteld. Deze methode is elders uitgebreid beschreven.(11) De resultaten van deze test werden alleen meegenomen als er met conventionele diagnostiek geen verwekker was gevonden.
Op basis van de resultaten uit alle diagnostiek werden de patiënten in 4 etiologische categorieën ingedeeld:
- Pneumokokken-CAP
- CAP door een atypisch pathogeen
- CAP door een ander pathogeen
- CAP door een onbekend pathogeen
De patiënten met pneumokokken-CAP bij wie een infecterend serotype kon worden geïdentificeerd (door middel van de kapselzwelling/Quellungreactie of op basis van de serologieuitslag voor 14 serotypen) werden verder onderverdeeld in 4 serotypegroepen:
- PCV7-serotypen (4, 6B, 9V, 14, 18C, 19F of 23F)
- PCV10 extra-serotypen (1, 5 of 7F)
- niet-PCV7-serotypen (1, 5 of 7F of een ander niet PCV7-serotype)
- niet-PCV10-serotypen (niet-vaccinserotypen)
Deze 4 groepen werden verder opgedeeld in bacteremische en niet-bacteremische patiënten.
Proporties van gedetecteerde pathogenen over 3 perioden (pre-PCV7, PCV7 en PCV10) werden met elkaar vergeleken. Proporties van serotypegroepen werden op dezelfde manier vergeleken: tussen alle patiënten, tussen de patiënten met CAP en tussen patiënten met CAP met een bekend serotype. Ten slotte werden de serotypegroepen vergeleken tussen patiënten met een bacteremische pneumonie en degenen met een niet-bacteremische pneumonie.
Resultaten
Populatie
In tabel 1 staan de patiëntkarakteristieken weer op het moment van ziekenhuisopname. Het meest opvallende verschil tussen de perioden is het aandeel patiënten met COPD in de voorgeschiedenis (p<0.001 tussen de pre-PCV7 en PCV7 + PCV10 periodes).
Tabel 1. Patiëntkarakteristieken van de 3 cohorten
| pre-PCV7 2004-2006 | PCV7 2007-2009 | PCV10 2012-2016 | |
| (n=201) | (n=304) | (n=300) | |
| Geslacht (man) | 124 (62) | 171 (56) | 178 (59) |
| Leeftijd (jaren) | 64 (17) | 63.7 (18) | 64.4 (16) |
| Comorbiditeiten* | |||
| Nierziekte | 10 (5) | 30 (10) | 41 (14) |
| Diabetes mellitus | 35 (17) | 43 (14) | 75 (25) |
| Leverziekte | 0 (0) | 2 (1) | 3 (1) |
| Maligniteit | 26 (13) | 19 (6) | 12 (4) |
| Hartfalen | 19 (10) | 48 (16) | 26 (9) |
| COPD | 64 (32) | 34 (11) | 60 (20) |
| PSI klasse | |||
| Klasse 1-3 | 117 (58) | 161 (53) | 177 (59) |
| Klasse 4-5 | 84 (42) | 143 (47) | 123 (41) |
| Dagen ziek voor opname | 5.2 (4.9) | 5.7 (5.3) | 5.4 (5.4) |
| Antibiotische voorbehandeling | 48 (24) | 82 (27) | 83 (28) |
Data gepresenteerd als aantal (%) of gemiddelde (SD). Afkortingen: PSI, ‘pneumonia severity; COPD, ‘chronic obstructive pulmonary disease’.* gedefinieerd zoals gebruikt om PSI-klassen te berekenen. (12)
Verdeling pathogenen
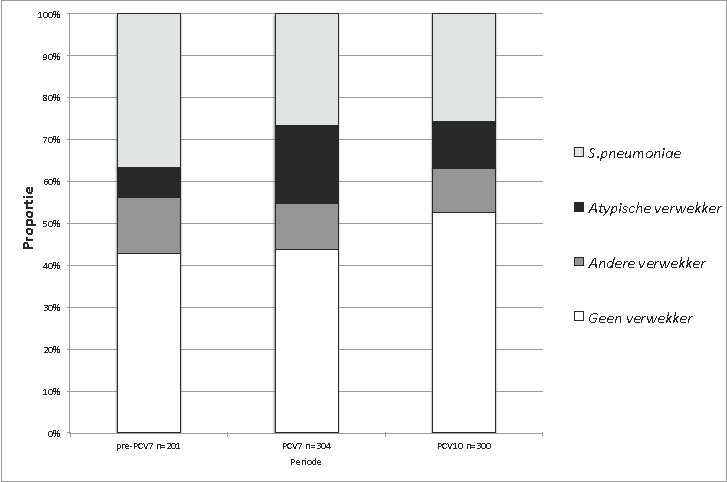
Figuur 1 laat zien dat de proportie pneumokokken-CAP afnam van 37% in de pre-PCV7-periode naar 26% in de PCV7-periode (RR 0.70, 95% BI: 0.54-0.91). Deze afname ging gepaard met een significante toename van CAP door een atypisch pathogeen (met name Q-koorts en psittacose, Tabel 2). In de PCV10-periode nam de proportie atypische verwekkers weer af, maar de proportie pneumokokken-CAP bleef vrijwel ongewijzigd ten opzichte van de PCV7-periode.
Figuur 1. Proporties van verwekkers binnen CAP-patiënten in de pre-PCV7-, PCV7-, pre-PCV10- en PCV10-perioden
Tabel 2. Proporties van verwekkers binnen CAP-patiënten in de pre-PCV7, PCV7-, pre-PCV10- en PCV10- perioden
Pre-PCV7 2004-2006 | PCV7 2007-2009 | PCV10 2012-2016 | PCV7 vs pre-PCV7 | p- waarde | PCV10 vs PCV7 | p- waarde | PCV10 vs pre-PCV7 | p- waarde | |
| (n=201) | (n=304) | (n=300) | |||||||
| No. (%) | No. (%) | No.(%) | RR 95% BI a | RR 95% BI b | RR 95% BI c | ||||
| S.pneumoniae | 74 (37) | 81 (27) | 77 (26) | 0.72 (0.56-0.94) | 0.02 | 0.96 (0.74-1.26) | 0.79 | 0.70 (0.54-0.91) | 0.01 |
| Atypische verwekker | 14 (7) | 57 (19) | 34 (11) | 2.69 (1.54-4.70) | <0.01 | 0.60 (0.41-0.9) | 0.01 | 1.63 (0.90-2.95) | 0.10 |
| Andere verwekker | 27 (13) | 33 (11) | 31 (10) | 0.81 (0.50-1.30) | 0.38 | 0.95 (0.60-1.51) | 0.84 | 0.77 (0.47-1.25) | 0.28 |
| Geen verwekker | 86 (43) | 133 (44) | 158 (53) | 1.02 (0.83-1.25) | 0.83 | 1.20 (1.02-1.42) | 0.03 | 1.23 (1.02-1.49) | 0.03 |
Serotypeverdeling
Tabel 3. Cijfers over de veranderingen in serotypeverdeling
| Pre-PCV7 2004-2006 | PCV7 2007-2009 | PCV10 2012-2016 | PCV7 vs pre-PCV7 | PCV10 vs PCV7 | PCV10 vs pre-PCV7 | |
| No. (%) | No. (%) | No. (%) | RR 95% BI a | RR 95% BI b | RR 95% BI c | |
| Binnen alle CAP-patiënten | 201 (100) | 304 (100) | 300 (100) | |||
| PCV7 | 25 (12) | 13 (4) | 2 (1) | 0.34 (0.18-0.66) | 0.16 (0.04-0.68) | 0.05 (0.01-0.22) |
| PCV10extra | 11 (5) | 12 (4) | 8 (3) | 0.72 (0.32-1.6) | 0.68 (0.28-1.63) | 0.49 (0.2-1.19) |
| niet-PCV10 | 14 (7) | 26 (9) | 34 (11) | 1.23 (0.66-2.29) | 1.33 (0.82-2.15) | 1.63 (0.9-2.95) |
| niet-PCV7 | 25 (12) | 38 (13) | 42 (14) | 1.01 (0.63-1.61) | 1.12 (0.74-1.69) | 1.13 (0.71-1.79) |
| Binnen alle pneumokokken CAP-patiënten | 74 (100) | 81 (100) | 77 (100) | |||
| PCV7 | 25 (34) | 13 (16) | 2 (3) | 0.48 (0.26-0.86) | 0.16 (0.04-0.69) | 0.08 (0.02-0.31) |
| PCV10extra | 11 (15) | 12 (15) | 8 (10) | 1 (0.47-2.12) | 0.7 (0.3-1.62) | 0.7 (0.3-1.64) |
| niet-PCV10 | 14 (19) | 26 (32) | 34 (44) | 1.7 (0.96-2.99) | 1.38 (0.92-2.06) | 2.33 (1.37-3.98) |
| niet-PCV7 | 25 (34) | 38 (47) | 42 (55) | 1.39 (0.94-2.06) | 1.16 (0.85-1.58) | 1.61 (1.11-2.36) |
| Binnen alle pneumokokken CAP | 50 (100) | 51 (100) | 44 (100) | |||
| met bekend serotype | ||||||
| PCV7 | 25 (50) | 13 (25) | 2 (5) | 0.51 (0.3-0.88) | 0.18 (0.04-0.75) | 0.09 (0.02-0.36) |
| PCV10extra | 11 (22) | 12 (24) | 8 (18) | 1.07 (0.52-2.2) | 0.77 (0.35-1.72) | 0.83 (0.37-1.87) |
| niet-PCV10 | 14 (28) | 26 (51) | 34 (77) | 1.82 (1.08-3.06) | 1.52 (1.11-2.07) | 2.76 (1.72-4.43) |
| niet-PCV7 | 25 (50) | 38 (75) | 42 (95) | 1.49 (1.08-2.05) | 1.28 (1.08-1.52) | 1.91 (1.44-2.54) |
| Binnen bacteremische pneumokokken CAP | 17 (100) | 24 (100) | 19 (100) | |||
| met bekend serotype | ||||||
| PCV7 | 11 (65) | 7 (29) | 0 (0) | 0.45 (0.22-0.92) | NA | NA |
| PCV10extra | 5 (29) | 8 (33) | 4 (21) | 1.13 (0.45-2.87) | 0.63 (0.22-1.78) | 0.72 (0.23-2.24) |
| niet-PCV10 | 1 (6) | 9 (38) | 15 (79) | 6.38 (0.89-45.73) | 2.11 (1.19-3.71) | 13.42 (1.98-91.14) |
| niet-PCV7 | 6 (35) | 17 (71) | 19 (100) | 2.01 (1-4.01) | 1.41 (1.09-1.82) | 2.83 (1.49-5.39) |
| Binnen niet-bacteremische pneumokokken CAP | 33 (100) | 27 (100) | 25 (100) | |||
| met bekend serotype | ||||||
| PCV7 | 14 (42) | 6 (22) | 2 (8) | 0.52 (0.23-1.18) | 0.36 (0.08-1.62) | 0.19 (0.05-0.76) |
| PCV10extra | 6 (18) | 4 (15) | 4 (16) | 0.81 (0.26-2.6) | 1.08 (0.3-3.86) | 0.88 (0.28-2.79) |
| niet-PCV10 | 13 (39) | 17 (63) | 19 (76) | 1.6 (0.96-2.67) | 1.21 (0.84-1.74) | 1.93 (1.2-3.11) |
| niet-PCV7 | 19 (58) | 21 (78) | 23 (92) | 1.35 (0.95-1.93) | 1.18 (0.94-1.49) | 1.6 (1.17-2.19) |
Bij alle CAP- patiënten
In de PCV7-periode nam de proportie PCV7-serotypen af tot 4% (in vergelijking met 12% in de pre-PCV7-periode (RR 0.34 95% CI: 0.18-0.66)). Deze daling zette door in de PCV10-periode naar 1% (p<0.01). Er werden geen significante veranderingen gezien in PCV10extra-, niet-PCV7- en niet-PCV10- serotypeproporties tussen de 3 perioden.
Bij patiënten met een pneumokokken-CAP waarbij het serotype bekend is
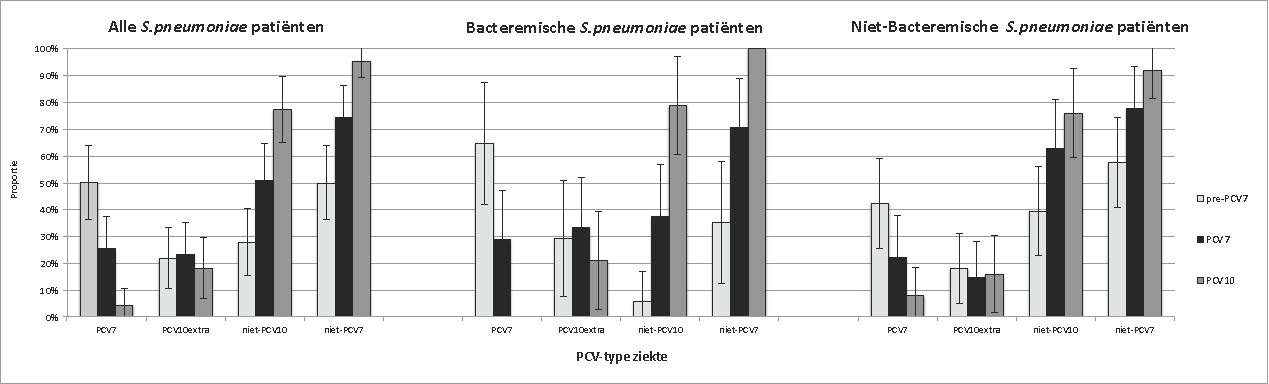
Ook binnen deze groep patiënten daalde de proportie PCV7-serotype CAP significant in de 2 periodes volgend op de pre-PCV7-periode. De PCV10-serotype proportie bleef statistisch gezien gelijk in de 3 periodes. Wanneer deze groep patiënten verder werd uitgesplitst naar patiënten met een bacteremische en met een niet-bacteremische pneumokokken-CAP, bleef de richting van de verschillen gelijk, maar waren ze relatief minder uitgesproken bij de patiënten met een niet-bacteremische pneumokokken-CAP (Figuur 2).
Figuur 2. Serotypeverdeling binnen alle pneumokokken-CAP-patiënten met een bekend serotype. Proporties van pneumokokken vergeleken tussen de perioden (pre-PCV7, PCV7 en PCV10). Balken zijn onderverdeeld in de verschillende serotypegroepen (PCV7-serotype, PCV10extra-serotype, niet-PCV7-serotype en niet-PCV10-serotype ziekte) . Foutbalken tonen het 95% betrouwbaarheidsinterval.
Discussie
De belangrijkste bevindingen van dit onderzoek zijn:
- In de 2 opvolgende perioden na de introductie van de pneumokokkenvaccinaties in het RVP is er een afname te zien van het aantal patiënten met een pneumokokken-CAP;
- Er is een significante afname te zien van het aantal patiënten met CAP veroorzaakt door 1 van de serotypes in PCV7; zowel bij patiënten met een bacteremische - als met een niet-bacteremische pneumokokken-CAP.
De afname van het aantal patiënten met een pneumokokken-CAP in de PCV7-periode ging gepaard met een toename van het aantal patiënten met een CAP veroorzaakte door atypische verwekkers. Dit kan verklaard worden door de Q-koortsepidemie en 2 uitbraken van psittacose. Desalniettemin bleef het aantal patiënten met een pneumokokken-CAP gelijk in de PCV10-periode, ook na verstrijken van de Q-koortsepidemie. Het aantal CAP-patiënten bij wie geen ziekteverwekker werd gevonden nam toe, terwijl de hoeveelheid uitgevoerde diagnostiek niet wezenlijk verschilde tussen de 3 perioden (supplement Tabel 1). Dit suggereert dat er sprake is van een aanhoudende afname van de proportie pneumokokken als ziekteverwekker bij patiënten opgenomen met een CAP.
Supplement Tabel 1. Ingezette diagnostiek en verschillen tussen testen gebruikt voor het identificeren van de verwekkers van CAP
| Pre-PCV7 2004-2006 | PCV7 2007-2009 | PCV10 2012-2016 | |
| (n=201) | (n=304) | (n=300) | |
| No. (%) | No. (%) | No. (%) | |
| Sputumkweek | 148 (74) | 143 (47) | 188 (63) |
| Sputum PCR a | 78 (39) | 91 (30) | 113 (38) |
| Urine antigeen L.pneumophila b | 186 (93) | 289 (95) | 287 (96) |
| Urine antigeen S.pneumoniae b | 183 (91) | 288 (95) | 287 (96) |
| Bloedkweek | 182 (90) | 259 (85) | 271 (90) |
| Conventionele serologie c | 130 (65) | 252 (83) | NA |
| Keelswab virale PCR d | NA | 225 (74) | 220 (73) |
| Keelswab atypische pathogenen e | NA | NA | 73 (24) |
| Virale kweek f | 88 (44) | NA | NA |
| Pneumokkenserologie g | 109 (54) | 169 (56) | 211 (70) |
Afkortingen: PCV7, 7-valente pneumokokken conjugaatvaccin; PCV10, 10-valente pneumokokken conjugaatvaccin; No.: aantal personen; a Sputum PCR voor atypische verwekkers: Legionella pneumophila, Mycoplasma pneumoniae en Chlamydophila pneumoniae/psittaci.b Urine antigeen testen voor de detectie van Legionella pneumophila serogroup 1 en Streptococcus pneumoniae (BinaxNOW®). c Gepaarde serologische testen (dag 1-3 en dag 10-21, respectievelijk) voor de detectie van antistoffen tegen Mycoplasma pneumoniae, Coxiella burnetii, Chlamydophila spp. of luchtweg virussen (adenovirus, influenza virus A en B, parainfluenza en respiratoir syncytieel virus).d Keelswab PCR voor virale verwekkers: (para)influenza, adenovirus, respiratoir syncytieel virus. e Keelswab PCR voor atypische verwekkers: Legionella pneumophila, Mycoplasma pneumoniae en Chlamydophila pneumoniae/psittaci.f Keelswab voor virale kweek: influenza.g Serotype-specifieke pneumokokkenantistoffen in serum werden getest voor de ontwikkeling van serotype-speciefieke pneumokokkenantistoffen door middel van specifieke titerstijgingen (14 serotypen).
De afname van het aantal patiënten met een CAP veroorzaakt door een van de serotypen in het PCV7 vanaf het begin van de pneumokokkenvaccinaties in het RVP, suggereert dat er bij volwassenen groepsimmuniteit is opgetreden. Werkhoven et al. toonde eerder vergelijkbare bevindingen in een Nederlands cohort, maar in deze studie was de observatieperiode, vanaf de invoering van PCV10 in het RVP, te kort om al PCV10-effecten aan te kunnen tonen.(6) Ook in onze studie zagen we - tot 6 jaar na de introductie van PCV10 in het RVP - geen duidelijke daling in het aantal patiënten met een niet-bacteremische pneumokokken-CAP veroorzaakt door een van de PCV10 extra-serotypen .
De kracht van dit onderzoek zit in het feit dat de resultaten voortkomen uit data van 3 goed omschreven cohorten die samenvallen met periodes kort vóór en na de invoering van de 2 pneumokokkenvaccinaties in het RVP. In alle cohorten werd uitgebreide conventionele microbiële diagnostiek verricht, wat is aangevuld met een serotypespecifieke immuno-assay om meer pneumokokkeninfecties, inclusief het infecterende serotype, te kunnen identificeren. Gezien het observationele karakter heeft dit onderzoek ook beperkingen. Verschillen in patiëntkarakteristieken tussen de cohorten kunnen invloed hebben gehad op de resultaten. Om aan te tonen dat het onwaarschijnlijk is dat het verschil in aantal patiënten met COPD in de voorgeschiedenis tussen de cohorten invloed heeft gehad, hebben we een sensitiviteitsanalyse uitgevoerd. Uitsluiting van deze patiënten uit de analyses leverde vergelijkbare resultaten op. Hetzelfde gold voor uitsluiting van alle patiënten die direct op een intensivecareafdeling waren opgenomen (alleen van toepassing op cohort 1).
Conclusie
Onze bevindingen suggereren dat pneumokokkenvaccinatie in het RVP geresulteerd heeft in groepsimmuniteit bij volwassen die opgenomen werden met een CAP. Dit blijkt uit een aanhoudende reductie van de proportie PCV7-serotypen na de introductie van PCV7 en PCV10. Daarnaast was er in de onderzochte populatie sprake van een reductie in de proportie pneumokkenziekte, zonder dat er een toename van andere pathogenen gezien werd. Deze gunstige neveneffecten vormen een extra argument om de pneumokokkenvaccinaties in het RVP te houden.
Dit artikel is eerder gepubliceerd in Vaccine [Internet]. 2017 Jul 24 [cited 2018 Feb 1];35(33):4112–8. http://www.ncbi.nlm.nih.gov/pubmed/28668570
Auteurs
G. H.J. Wagenvoort*1,2, S. M.T. Vestjens*3, B. J.M. Vlaminckx 1, E. M.W. van de Garde 4
*gelijkwaardige bijdrage
1. Afdeling Medische Microbiologie en Immunologie, St. Antonius Ziekenhuis, Utrecht/Nieuwegein
2 Laboratorium voor Medische Microbiologie en Infectieziekten, Isala, Zwolle
3. Afdeling Interne Geneeskunde, St. Antonius Ziekenhuis, Utrecht/Nieuwegein
4. Afdeling Klinische Farmacie, St. Antonius Ziekenhuis, Utrecht/Nieuwegein
Correspondentie
s.vestjens@antoniusziekenhuis.nl
Literatuur
- Wagenvoort GHJ, Sanders EAM, Vlaminckx BJ, Elberse KE, de Melker HE, van der Ende A, et al. Invasive pneumococcal disease: Clinical outcomes and patient characteristics 2–6 years after introduction of 7-valent pneumococcal conjugate vaccine compared to the pre-vaccine period, the Netherlands. Vaccine [Internet]. 2016 Feb 17 [cited 2017 May 29];34(8):1077–85. Available from: http://www.ncbi.nlm.nih.gov/pubmed/26778420
- Knol MJ, Wagenvoort GHJ, Sanders EAM, Elberse K, Vlaminckx BJ, de Melker HE, et al. Invasive Pneumococcal Disease 3 Years after Introduction of 10-Valent Pneumococcal Conjugate Vaccine, the Netherlands. Emerg Infect Dis [Internet]. 2015 Nov [cited 2018 Mar 29];21(11):2040–4. Available from: http://www.ncbi.nlm.nih.gov/pubmed/26488415
- Vestjens SMT, Wagenvoort GHJ, Grutters JC, Meek B, Aldenkamp AF, Vlaminckx BJM, et al. Changes in pathogens and pneumococcal serotypes causing community-acquired pneumonia in The Netherlands. Vaccine [Internet]. 2017 Jul 24 [cited 2018 Feb 1];35(33):4112–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/28668570
- Postma DF, van Werkhoven CH, van Elden LJR, Thijsen SFT, Hoepelman AIM, Kluytmans JAJW, et al. Antibiotic Treatment Strategies for Community-Acquired Pneumonia in Adults. N Engl J Med [Internet]. 2015 Apr 2 [cited 2018 Feb 1];372(14):1312–23. Available from: http://www.nejm.org/doi/10.1056/NEJMoa1406330
- Said MA, Johnson HL, Nonyane BAS, Deloria-Knoll M, O′Brien KL, Team for the AAPBS. Estimating the Burden of Pneumococcal Pneumonia among Adults: A Systematic Review and Meta-Analysis of Diagnostic Techniques. Hill PC, editor. PLoS One [Internet]. 2013 Apr 2 [cited 2018 Feb 2];8(4):e60273. Available from: http://dx.plos.org/10.1371/journal.pone.0060273
- van Werkhoven CH, Hollingsworth RC, Huijts SM, Bolkenbaas M, Webber C, Patterson S, et al. Pneumococcal conjugate vaccine herd effects on non-invasive pneumococcal pneumonia in elderly. Vaccine [Internet]. 2016 Jun 14 [cited 2018 Feb 1];34(28):3275–82. Available from: http://www.ncbi.nlm.nih.gov/pubmed/27171754
- Rodrigo C, Bewick T, Sheppard C, Greenwood S, Mckeever TM, Trotter CL, et al. Impact of infant 13-valent pneumococcal conjugate vaccine on serotypes in adult pneumonia. Eur Respir J [Internet]. 2015 Jun [cited 2018 Feb 1];45(6):1632–41. Available from: http://erj.ersjournals.com/lookup/doi/10.1183/09031936.00183614
- Endeman H, Schelfhout V, Paul Voorn G, van Velzen-Blad H, Grutters JC, Biesma DH. Clinical features predicting failure of pathogen identification in patients with community acquired pneumonia. Scand J Infect Dis [Internet].2008 Jan 8 [cited 2018 Feb 1];40(9):715–20. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19086245
- Meijvis SCA, Hardeman H, Remmelts HHF, Heijligenberg R, Rijkers GT, van Velzen-Blad H, et al. Dexamethasone and length of hospital stay in patients with community-acquired pneumonia: a randomised, double-blind, placebo-controlled trial. Lancet (London, England) [Internet]. 2011 Jun 11 [cited 2016 Dec 22];377(9782):2023–30. Available from: http://linkinghub.elsevier.com/retrieve/pii/S0140673611606077
- Registratie website https://clinicaltrials.gov/ct2/show/NCT01743755
- van Mens SP, Meijvis SCA, Endeman H, van Velzen-Blad H, Biesma DH, Grutters JC, et al. Longitudinal analysis of pneumococcal antibodies during community-acquired pneumonia reveals a much higher involvement of Streptococcus pneumoniae than estimated by conventional methods alone. Clin Vaccine Immunol [Internet]. 2011 May [cited 2018 Feb 1];18(5):796–801. Available from: http://cvi.asm.org/lookup/doi/10.1128/CVI.00007-11
- Fine MJ, Auble TE, Yealy DM, Hanusa BH, Weissfeld LA, Singer DE, et al. A prediction rule to identify low-risk patients with community-acquired pneumonia. N Engl J Med [Internet]. 1997 Jan 23 [cited 2016 Dec 22];336(4):243–50. Available from: http://www.nejm.org/doi/abs/10.1056/NEJM199701233360402
Infectieziekten Bulletin, jaargang 29, nummer 6, juni 2018
Mijd de mijt
In 2016 startte het project ‘Mijd de Mijt’ van GGD Hollands Midden. De GGD zocht naar een gecoördineerde aanpak van scabiës (schurft) in studentenhuizen in Leiden. Met hun aanpak won de GGD bij de Transmissiedag de Jim van Steenbergenprijs.
Mijd de mijt
“Vroeger kwam scabiës veel meer voor dan nu. Toch zien we het steeds meer binnen bepaalde risicopopulaties, zoals asielzoekers, maar ook in studentenhuizen”, vertelt Timo Boelsums, arts infectieziektebestrijding bij GGD Hollands Midden. “Er komen meer vragen bij onze GGD over jeukklachten. Vooral het aantal vragen uit studentenhuizen is toegenomen. Bij studenten zien we steeds vaker scabiës. In veel gevallen is bij de huisarts dan al scabiës vastgesteld, maar het blijkt lastig om het hele studentenhuis mee te behandelen.”
Waarom is het lastig voor een huisarts om een heel studentenhuis mee te behandelen?
“Niet alle studenten zitten bij dezelfde huisarts. Op het spreekuur ziet een huisarts 1 student en dan kan hij een middel voorschrijven voor die ene student. Maar omdat vermoedelijk meer studenten uit hetzelfde huis ook scabiës hebben, heeft behandeling van alleen die ene student geen zin. De kans dat hij opnieuw besmet wordt is namelijk groot. Je krijgt dan een pingpongeffect. Je moet dus in dit soort gevallen alle anderen in huis mee behandelen. De huisarts kan dan wel zeggen dat de rest zich ook moet laten behandelen, maar je kunt niet altijd al je – soms wel 20 – huisgenoten op tijd bereiken. Om deze reden bedachten we dat de GGD hier een mogelijke rol in kan hebben.”
Hoe pak je dat aan?
“Met die vraag begon ons project. We begonnen met een scabiësspreekuur. We schatten in dat als we studenten met scabiës op ons spreekuur zien, we dan goede voorlichting kunnen geven en meteen voor alle studenten in het studentenhuis een recept kunnen voorschrijven.”
Jullie doen ook de diagnostiek?
“Dat klopt. Met een dermatoloog uit de regio hebben we onze aanpak besproken, omdat deze diagnostiek normaal alleen door dermatologen wordt gedaan. Je neemt een huidschraapsel af van een verdachte plek en bekijkt dit onder de microscoop. Als je daar een mijt in aantreft, dan weet je zeker dat de student scabiës heeft. Omdat je de diagnostiek meteen bij de GGD kunt doen, heeft de student binnen 10 minuten zekerheid. Je kunt meteen folders en recepten meegeven voor zijn huisgenoten.”
Betaalt jullie GGD dit zelf?
“De kosten voor de diagnostiek dragen we zelf. Het consult wordt betaald door de zorgverzekeraar; het valt, net zoals het consult bij de huisarts, buiten het eigen risico. Dat maakt het spreekuur laagdrempelig. De aanpak lijkt effectief. We merken dat de diagnostiek en het zien van de mijt – we maken er vaak een foto van – erg motiverend werkt bij de behandeling.”
Hoe kwamen de studenten erachter dat er een scabiësspreekuur bestond?
“We hebben het rustig aangepakt. Alleen studenten met jeukklachten die contact met ons opnamen, nodigden we uit voor het spreekuur. We zien nu dat er door mond-op-mondreclame steeds meer animo voor het spreekuur is. Naast het opzetten van het spreekuur gaan we ook onderzoek doen om het scabiësprobleem in Leiden beter in kaart te brengen en willen we de voorlichting aan studenten verbeteren. Uiteindelijk hopen we hiermee ons doel te bereiken: het verminderen van verspreiding van scabiës in Leidse studentenhuizen.”
Heb je al reacties gehad van GGD’en uit andere studentensteden?
“We horen af en toe wel eens van uitbraken in andere studentensteden. GGD’en hebben al geïnformeerd hoe wij het aanpakken. Ik heb nog niet gehoord dat andere steden het idee gaan overnemen, maar interesse is er zeker.”
Auteur
K. Kosterman, eindredacteur Infectieziekten Bulletin
Aankondigingen
Wijzigingen LCI-richtlijnen
Een overzicht met alle wijzigingen van 1 maart tot en met 8 juni 2018 in de richtlijnen van de Landelijke Coördinatie Infectieziektebestrijding (LCI) van het RIVM en de daarvan afgeleide producten is onlangs online gepubliceerd op https://lci.rivm.nl/aankondigingen-2018-juni.
Registratie infectieziekten
Wet publieke gezondheid
De meldingen Wet publieke gezondheid tot en met week 20, 2018
Virologische weekstaten
De meldingen in de virologische weekstatebn tot en met week 20, 2018