Infectieziekten Bulletin
November 2018 | Jaargang 29, nummer 9
https://magazines.rivm.nl/2018/11/infectieziekten-bulletin
Gesignaleerd
Binnenlandse signalen
Bof onder studenten in Brabant
In de GGD-regio’s Brabant-Zuidoost en Hart voor Brabant is een cluster van bof gemeld. De eerste ziektedagen van de 8 patiënten (leeftijd van 20 tot 24 jaar) variëren van 14 tot en met 22 oktober. De patiënten zijn studenten in Eindhoven. Zeven patiënten waren volledig gevaccineerd tegen bof en 1 patiënt was niet gevaccineerd. Bij 5 patiënten werd bof bevestigd door laboratoriumdiagnostiek en de andere 3 konden alleen epidemiologisch worden gelinkt. Een duidelijke bron is niet gevonden maar vermoedelijk zijn ze tegelijk besmet tijdens een activiteit van een studentenvereniging. In overleg met de GGD hebben de studentenvereniging en de universiteit alle studenten in Eindhoven per e-mail geïnformeerd: studenten worden geadviseerd om hun vaccinatiestatus te controleren en zich te laten vaccineren als ze niet of maar 1 keer gevaccineerd zijn, verder worden ze verzocht zich te melden bij de GGD als ze gezondheidsklachten hebben die passen bij bof en bij ziekte thuis te blijven. Uit het genotyperingsonderzoek blijkt dat de bof bij de studenten wordt veroorzaakt door genotype G. De bepaalde korte sequentie is identiek aan recent gedetecteerde bofvirussen in o.a. de Verenigde Staten, Canada en Schotland. Om de clusteromvang in kaart te brengen is het ook bij nieuwe bofpatiënten zinvol om materiaal in te sturen voor typeringsonderzoek. In overleg met de GGD kan dit in het kader van de openbare gezondheidszorgdiagnostiek. In Nederland zijn dit jaar tot en met 24 oktober 2018, 50 patiënten met bof gemeld. In 2016 en 2017 waren dit respectievelijk 71 en 46 patiënten. (Bronnen: GGD Brabant Zuid-Oost, GGD Hart voor Brabant, RIVM)
Meerdere gezinsclusters van hepatitis A na een reis naar Marokko
Op 9 oktober kreeg de GGD Rotterdam-Rijnmond melding van 3 kinderen met hepatitis A uit hetzelfde gezin. Het gezin was 6 weken daarvoor teruggekomen uit Marokko voor vakantie en langdurig familiebezoek. Uit het contactonderzoek bleek dat het gezin in Marokko veel tijd had doorgebracht met 3 andere gezinnen die daar ook op vakantie waren, en gezamenlijk maaltijden hadden genuttigd. Vier van de 6 kinderen uit 1 van deze gezinnen hadden klachten gehad passend bij hepatitis A. Na onderzoek bleek dat alle 6 kinderen positief waren voor hepatitis A IgM. Drie van de 9 kinderen waren PCR-positief en de typeringen bevestigden een stam die geassocieerd is met herkomst Marokko; bij de andere 6 kinderen was de PCR negatief.
Zes van de 9 kinderen met hepatitis A waren gedurende hun besmettelijke periode naar de basisschool geweest; 1 basisschool met 2 kinderen verspreid over 2 klassen en 1 basisschool met 4 kinderen verspreid over 4 klassen. Er is nog geen secundaire transmissie op de scholen aangetoond. De leerlingen en medewerkers van beide basisscholen hebben een hepatitis A-vaccinatie aangeboden gekregen. Dit heeft vooral als doel om secundaire transmissie naar ouders en andere volwassenen te voorkomen. Bij 1 basisschool kon de vaccinatie beperkt blijven tot 2 klassen en bij de andere school is aan alle leerlingen en medewerkers vaccinatie aangeboden. Dit soort uitbraken toont aan dat reizigers geïnformeerd moeten worden over het belang van vaccinatie, ook voor hun kinderen. (Bron: GGD Rotterdam-Rijnmond)
Verheffing van Salmonella Goldcoast in Nederland
Sinds september 2018 is in de landelijke Salmonella laboratoriumsurveillance een significante toename van het aantal humane isolaten van Salmonella enterica serotype Goldcoast te zien. Op basis van whole genome sequencing (WGS) is er sprake van een uitbraak van 16 patiënten vanaf week 27 dit jaar. Het gaat om 7 mannen en 9 vrouwen in de leeftijd van 2- 87 jaar. Patiënten wonen verspreid over het land. Het echte aantal geïnfecteerde personen ligt naar schatting velen malen hoger. De uitbraak lijkt vooralsnog beperkt tot Nederland. GGD’en zijn gevraagd om een vragenlijst af te nemen bij de patiënten voor bronopsporing, waarbij specifiek wordt gevraagd naar de consumptie van varkensvleesproducten. Uit de geretourneerde vragenlijsten komt tot nu toe geen specifiek product naar voren. 2 isolaten afkomstig van varkenskarkassen die bemonsterd werden tijdens routineonderzoek van de Nederlandse Voedsel- en Warenautoriteit (NVWA) in een slachthuis (in week 29 en week 32), bleken te matchen met de uitbraakstam. Dit wijst er op dat de bron zeer waarschijnlijk gezocht moet worden bij varkens(-slachterij). De NVWA is gestart met het in kaart brengen van de processtromen van deze varkens(karkassen) vanaf het oorsprongsbedrijf naar de verwerkende industrie. Het is vooralsnog niet duidelijk in welke schakel van de voedselketen de bron van deze uitbraak zich bevindt. Getracht zal worden om een focus aan te brengen in de forward tracering (richting levensmiddelen) om daarmee mogelijke aanknopingspunten in bronnen voor eventuele beheersmaatregelen te vinden. Eerdere uitbraken van S. Goldcoast in het buitenland werden gelinkt aan onder andere varkensvlees en schelpdieren. (Bronnen: RIVM, NVWA)
Buitenlandse signalen
Westnijlvirusinfecties in Duitsland
Het transmissieseizoen in Europa voor het westnijlvirus (WNV) van 2018 startte eerder dan gebruikelijk en er zijn al meer meldingen dan die van de afgelopen 5 jaren tesamen. In 2018 zijn voor het eerst in Duitsland westnijlvirusinfecties bij meerdere dieren (paarden, roofvogels) en een persoon vastgesteld. Deze eerste autochtone besmetting was bij een 31-jarige dierenarts die autopsie had uitgevoerd op een Laplanduil (Strix nebulosa) die was gevonden in een wildpark in Beieren. Drie dagen na de autopsie kreeg de dierenarts griepachtige klachten en vlekkerige huiduitslag. Een gepaard serumsample liet seroconversie van IgM antistoffen zien tegen WNV samen met een significante titerstijging van IgG tegen WNV en andere flavivirussen. De patiënt was gevaccineerd tegen tekenencefalitis (TBE) en gele koorts, hetgeen de significante titerstijging van IgG kan verklaren. Infectie met westnijlvirus nadat een patiënt een autopsie op besmette vogels had uitgevoerd, is vaker beschreven. Beschermingsmaatregelen, zoals het dragen van handschoenen, schort en oogbescherming zijn belangrijk om dit risico zo klein mogelijk te houden. De gebruikelijke transmissieroute van WNV naar mensen via muggen, was in dit geval onwaarschijnlijk. Maar omdat het een bijzonder hevig transmissieseizoen is voor het westnijlvirus, is het toch van belang dat reizigers die naar gebieden waar westnijlinfecties voorkomen gaan en bewoners in deze gebieden, preventieve maatregelen nemen tegen muggenbeten (o.a. het dragen van bedekkende kleding). (Bronnen: OIE, CDC, ProMED)
Autochtone dengue in Spanje en Zuid-Frankrijk
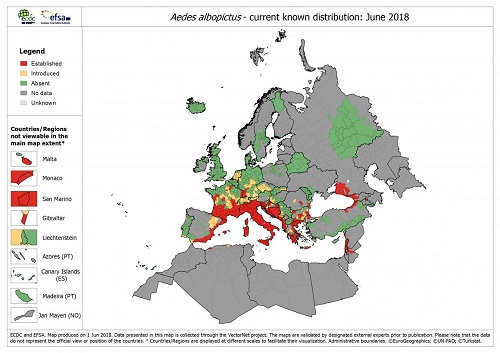
Het European Centre for Disease Prevention and Control (ECDC) heeft een snelle risicobeoordeling uitgebracht over autochtone dengue binnen de Europese Unie(EU) in oktober 2018. Begin oktober werd bij 9 patiënten na laboratoriumonderzoek dengue aangetoond: 3 patiënten in Zuid-Spanje en 6 in Frankrijk.De patiënten in Zuid-Spanje komen uit 1 familie en zijn zeer waarschijnlijk besmet geraakt in de regio Murcia of de provincie Cadiz. Dit is de eerste laboratoriumbevestigde autochtone dengue-uitbraak in Spanje. Het denguevirus wordt onder andere overgedragen via Aziatische tijgermuggen, Aedes albopictus, die in de regio Murcia al waren gevestigd en nu ook in de provincie Cadiz voorkomen (Figuur 1). Het Spaanse ministerie van Volksgezondheid voert in samenwerking met deze regio’s aanvullend entomologisch onderzoek uit in de omgeving van de mogelijke blootstellingsplaatsen. Gezondheidsmedewerkers en laboratoria zijn geïnformeerd om tijdige opsporing en melding van nieuwe denguevirusinfecties mogelijk te maken.In Frankrijk is bij 5 patiënten in Saint Laurent du Var dengueserotype 2 vastgesteld en bij 1 niet-gerelateerde patiënt in Montpellier serotype 1. Aedes albopictus is normaal tot begin november actief in de omgeving van Saint Laurent du Var en tot begin december in Montpellier. In Zuid-Frankrijk zijn in 2010, 2013, 2014 en 2015 denguepatiënten gemeld die ter plaatse besmet waren. Deze uitbraken bleven altijd beperkt tot maximaal 7 patiënten. (Bronnen: , VectorNet, ECDC)
Figuur 1. Verspreiding van Aedes albopictus in Europa op regionaal/provinciaal niveau
Uitbraak van Burkholderia cepacia complex infecties op de IC in Duitsland
In augustus 2018 werd in Duitsland een bovenregionale uitbraak geconstateerd van Burkholderia cepacia-complex onder patiënten op de intensivecare-afdeling van een aantal ziekenhuizen. De uitbraak werd veroorzaakt door het gebruik van besmet mondwater. Tot nu toe zijn 16 patiënten met een infectie of kolonisatie gemeld in 3 ziekenhuizen in 2 federale deelstaten. Twee patiënten met ernstige comorbiditeit zijn overleden. De WGS-gegevens ondersteunen het verband tussen de B. cepacia-isolaten van 2 patiënten en het mondwater. Het mondwater (niet op alcoholbasis) dat voornamelijk voor de Duitse markt wordt geproduceerd, is teruggeroepen door de producent in Luxemburg. Burkholderia cepacia kan tot een pneumonie leiden bij immuungecompromitteerde patiënten, bij patiënten die beademd worden en ook bij patiënten met cystic fibrose. Bij gezonde personen leidt het zelden tot infectie. In het verleden is al eerder een B. cepacia-uitbraak beschreven in Duitsland door besmet mondwater. Bronnen: RKI Epidemiologisches Bulletin, Eurosurveillance, BfArM, Martin et al., 2012.
Uitbraak van listeriose gerelateerd aan zalmproducten in enkele Europese landen
De Europese Voedselautoriteit (EFSA) en het European Centre for Disease Prevention and Control (ECDC) hebben een langer bestaande uitbraak van listeriose gemeld, veroorzaakt door Listeria monocytogenes sequentietype (ST) 8. Deze uitbraak werd geïdentificeerd door middel van WGS-analyse in 3 landen: Denemarken (6 patiënten), Duitsland (5) en Frankrijk (1). Er zijn 4 patiënten overleden. In oktober 2015 werd de eerste patiënt vastgesteld in Denemarken en de meest recente patiënt werd in mei 2018 in Duitsland gemeld. In 2017 werd een eerste uitbraak door Denemarken onderzocht en gelinkt aan gerookte- zalmproducten. In oktober 2017 meldde Frankrijk een overeenstemmende L. monocytogenesstam in voedselisolaten van gemarineerde zalm die afkomstig was van hetzelfde Poolse verwerkingsbedrijf dat ook werd geïdentificeerd in het Deense uitbraakonderzoek. Dit ondersteunt de hypothese dat er mogelijk besmetting heeft plaatsgevonden bij het verwerkingsbedrijf in Polen. Maar omdat de WGS-gegevens over de isolaten in de milieu- en voedselmonsters uit de Poolse verwerkingsfabriek ontbreken, is het niet mogelijk om dit te bevestigen.
Verontreiniging op het niveau van de primaire productie kan vooralsnog ook niet worden uitgesloten, totdat gedetailleerde informatie over de Noorse producenten van de zalm die in de besmette partijen is gebruikt, wordt gerapporteerd en beoordeeld. Er zijn in september 2017 bestrijdingsmaatregelen geïmplementeerd bij het Poolse verwerkingsbedrijf; o.a. aanvullende schoonmaak/desinfectie van materialen en ruimten en intensivering van het testbeleid van voedselsamples.
Ondanks deze maatregelen wijst de identificatie van dezelfde stam in een zalmproduct in Frankrijk en een nieuwe patiënt met listeriose in Duitsland erop dat de bron van besmetting nog steeds actief is. Mogelijk zijn besmette producten gedistribueerd naar andere landen van de Europese Unie (EU). De omvang van deze uitbraak is waarschijnlijk groter omdat de uitbraak werd geïdentificeerd met WGS dat slechts in een aantal Europese landen (waaronder Nederland) routinematig wordt gebruikt om L. monocytogenes-isolaten te karakteriseren. Er is voor zover bekend geen distributie naar Nederland geweest van besmette producten. Ook zijn er geen Nederlandse patiënten gemeld die gerelateerd zijn aan deze uitbraak. (Bronnen: NVWA, ECDC-EFSA , S. Schjørring et al. Eurosurveillance (2017).
Snelle toename van invasieve pneumokokkenziekte in Engeland en Wales door non-vaccin serotype 7C
In een artikel in Emerging Infectious Diseases (EID) rapporteren onderzoekers over een plotselinge en snelle toename van invasieve pneumokokkenziekte door serotype 7C in Engeland en Wales. Dit serotype is niet opgenomen in een pneumokokkenvaccin. In de periode 2000/2001 tot en met 2015/2016 waren er jaarlijks gemiddeld 3 patiënten en in 2016/2017 waren dit er 29. De toename werd bijna volledig veroorzaakt door klonale expansie van sequentietype 177, die eerder geassocieerd werd met vaccinserotype 19F. In Nederland is geen sprake van een toename van serotype 7C. In de surveillance van het Nederlands Referentie Laboratorium voor Bacteriële Meningitis (NRLBM) werd 1 patiënt met invasieve pneumokokkenziekte serotype 7C gezien in 2018, 1 in 2007 en 2 in 2006. (Bronnen: EID, NRLBM)
Auteur
B. Schimmer, Centrum Infectieziektebestrijding, RIVM
Correspondentie
Infectieziekten Bulletin, jaargang 29, nummer 9, November 2018
Extramurale scabiësbestrijding
In de afgelopen jaren zijn er veel grote scabiës uitbraken gemeld bij de GGD. Wanneer externe partijen een grote scabiësuitbraak melden, is dit niet alleen vanwege de meldingsplicht (1) maar ook omdat zij de GGD willen betrekken bij de bestrijding van de uitbraak. De bestrijding van scabiës is intensief: meerdere mensen moeten tegelijk behandeld moeten worden en het is belangrijk dat de bijbehorende hygiënemaatregelen op de juiste manier worden uitgevoerd. Om een scabiësuitbraak effectief te kunnen bestrijden is goede coördinatie en communicatie een voorwaarde. Wanneer een uitbraak bij de GGD gemeld wordt is er regelmatig al sprake van veel onrust en onduidelijkheid bij de melder, zowel onder de patiënten als het personeel. (2) Dit is vooral het geval als er geen (medische)coördinatie is, bijvoorbeeld als het gaat om scabiës in de thuiszorg (zelfsturende teams), in kleinschalige woonvoorzieningen, in gezinnen, in studentenhuizen en in dak- en thuislozenopvanglocaties. GGD Haaglanden heeft onderzoek gedaan om de coördinatie en communicatie bij scabiësuitbraken in deze extramurale zorgomgevingen, te verbeteren.
Extramurale scabiësbestrijding
Methode
Het doel van het project was om hulpmiddelen (tools) te ontwikkelen die bijdragen aan de verbetering van de coördinatie en uitvoering van scabiësbestrijding.
Wij hebben meerdere scabiëscasussen geanalyseerd, interviews afgenomen met degenen die erbij betrokken waren en een expertmeeting georganiseerd met artsen/verpleegkundigen van andere GGD’en. Met de verkregen informatie hebben we tools ontwikkeld die ter beoordeling zijn voorgelegd aan de expertgroep. (3)
Casusanalyse
Er zijn 7 casussen van scabiësuitbraken onderzocht. Dit waren uitbraken in de thuiszorg, in opvanglocaties voor daklozen, bij gezinnen en onder studenten. Uit de analyses van deze uitbraken werden bestrijdingsknelpunten zichtbaar gemaakt die vervolgens werden besproken tijdens de interviews
Interviews
De deelnemers aan de interviews waren GGD- verpleegkundigen en - artsen, verpleegkundigen en verzorgenden van de thuiszorg, managers van een thuiszorgteam, studentenartsen en medewerkers van de daklozenopvang.
Expertmeeting
Aan de expertmeeting namen 4 projectmedewerkers deel, 8 verpleegkundigen en 1 arts van 8 verschillende GGD’en. Aan de hand van de 7 casusbeschrijvingen werd besproken of zij de knelpunten herkenden en welke oplossingen zij daarvoor hadden.
Resultaten
Knelpunten
Op basis van de analyses, de interviews en de expertmeeting werden de volgende knelpunten vastgesteld:
- Scabiësuitbraken worden niet altijd tijdig gesignaleerd;
- Hoe ‘hard’ moet de diagnose scabiës zijn om de omvang van de bestrijdingsmaatregelen te verantwoorden? (4)
- Het is lastig om te bepalen wie behandeld gaat worden;
- Geheimhouding, coördinatie van informatie en voorkomen van onrust; (5)
- Bespreekbaar maken proces en coördinatierollen;
- Hoe zorgen we voor een heldere dossiervorming?
- Hoe kunnen patiënten/personeel ertoe gebracht worden om behandeling getrouw op te blijven volgen. (6)
Tijdens de expertmeeting werd duidelijk dat de punten ‘Bespreekbaar maken van het proces en de coördinatierollen’ en ‘het tijdig signaleren’ de meeste prioriteit hadden
Producten
Er zijn 2 tools ontwikkeld die gebruikt kunnen worden om het bestrijdingstraject beter te laten verlopen.De eerste tool is een stappenplan bestemd voor de melder van de uitbraak. Hierbij is een onderscheid gemaakt tussen scabiësuitbraken in extramurale zorgomgevingen (o.a. thuiszorg) en uitbraken onder studenten en in gezinnen. Er bestaat al een stappenplan voor uitbraken in zorginstellingen. De te nemen stappen worden aangegeven en de uitvoering wordt toegelicht.De tweede tool is een coördinatiekaart voor GGD’en om de rol van de melder te bespreken (zie PDF hiernaast). Het is een document met vragen aan de melder op basis waarvan de betrokken GGD de juiste coördinator voor de uitbraak kan aanwijzen. De vragen zijn bedoeld om de melder zich bewust te maken van de taken die bij het coördineren van een uitbraak horen.
Het stappenplan en de coördinatiekaart zijn ter beoordeling voorgelegd aan de expertgroep. Er zijn een paar aanpassingen gedaan in de uiteindelijke versies, bijvoorbeeld over de behandelkosten en de eigen bijdrage van de cliënten. Daar waar er verschillen tussen GGD’en waren, was de richtlijn Scabiës van de Landelijke Coördinatie Infectieziektebestrijding (LCI) van het RIVM leidend. Verder is op verzoek van meerdere GGD’en een stroomschema (zie PDF hiernaast) aan het stappenplan toegevoegd.
Het stappenplan en de coördinatiekaart zijn gepresenteerd aan het team infectieziektebestrijding van de GGD Haaglanden en aan de GGD’en in de regio tijdens het Provinciaal Overleg Infectieziekten (POI) Zuid-Holland. Het was de bedoeling om de tools in de periode juni 2016 tot en met oktober 2016 in de provincie te gebruiken en daarna te evalueren. Er waren echter geen uitbraken en daarom werd besloten om ze ook te verspreiden onder de GGD’en die in de expertgroep waren vertegenwoordigd. Hiermee zou de kans op ergens een uitbraak groter zijn en daarmee gelegenheid zijn om te testen en te evalueren. De testperiode werd verlengd tot eind februari 2017. De tools zijn uiteindelijk gebruikt bij 2 uitbraken in de extramurale zorg door een thuiszorginstelling en door de GGD verpleegkundige.
Uit de evaluatie bleek dat het stappenplan de meldende partijen goed had geholpen om alle taken die bij een uitbraak horen te overzien en uit te voeren. En aan de hand van de coördinatiekaart had de GGD de juiste vragen kunnen stellen aan genoemde partijen en kon bij allebei een coördinator aanwijzen.
Conclusie en aanbeveling
GGD Haaglanden kijkt terug op een interessant en leerzaam project waarin samen met de GGD’en in Zuid-Holland gestructureerd is gewerkt aan verbeteringen in de bestrijding van scabiës in de extramurale setting. De tools die zijn ontwikkeld kunnen zowel de GGD als de betrokken zorgomgeving helpen bij de bestrijding van scabiës. Door de coördinatiekaart is het voor de GGD makkelijker om de coördinatie met de medewerkers van de betrokken partij te bespreken en uiteindelijk de juiste persoon op de plek van ‘coördinator’ te krijgen. Het stappenplan geeft voor de betrokken partij kort en bondig de juiste informatie over de aanpak van een scabiësuitbraak.
De tools zijn er nu maar vragen om een blijvende kritische blik: Is de informatie die we hebben actueel? Passen de tools nog bij de huidige ontwikkelingen in de zorg? De GGD Haaglanden is daarom voornemens om op termijn de tools intern opnieuw te evalueren.
Dit onderzoek werd mede mogelijk gemaakt door financiële steun vanuit het programmabudget van het project Regionale Ondersteuning van het RIVM Centrum Infectieziektebestrijding. De tools zijn te vinden op https://lci.rivm.nl/richtlijnen/scabies.
Auteurs
C.Franchimon-Bremmer, W. Tas, D. van der Zande, GGD Haaglanden, afdeling infectieziektenbestrijding,
Correspondentie
dianne.vanderzande@ggdhaaglanden.nl
Literatuur
- LCI-richtlijn Scabiës http://www.rivm.nl/Onderwerpen/S/Scabies
- LCI-Draaiboek Scabiës – schurft – in zorginstellingen.
- Breemer J.N. , M.C. Trompenaars, H. Voeten, Evaluatie van nieuwe hulpmiddelen voor scabiësuitbraken in zorginstellingen. Waardevolle lessen voor praktijkonderzoek. Gepubliceerd op RIVM site RAC regionalisering.
- R Grol, M Wensing, M Eccles, D Davis - 2013van den Hoek JA, van de Weerd JA, Baayen TD, Molenaar PM, Sonder GJ, van Ouwerkerk IM Hardnekkig probleem met scabiës in Amsterdam: resistentie tegen lindaan en ivermectine? Infectieziektebulletin 2008;6:204-206
- W.Tas, GGD Haaglanden, Scabiës, Onbegrepen jeukklach-ten,https://link.springer.com/article/10.1007/s40884-015-0008-2, De Verpleegkundig Spe-cialist ,April 2015, Volume 10, Issue 1, pp 20–23
- R. Brugmans, GGD Haaglanden, Effectiever door Empathie, Betere bestrijding van scabiës door kennis over de beleving van de drager, Onderzoek in het kader van studie Master Public Health, 9 oktober 2015
Infectieziekten Bulletin, jaargang 29, nummer 9, November 2018
Aanpassing van de BEL-bemonsteringscriteria
De Bronopsporings Eenheid Legionellapneumonie (BEL) voert sinds 2002 brononderzoek uit voor de GGD’en bij potentiële bronnen van patiënten met een legionellapneumonie. Uit de resultaten van deze bemonsteringen blijkt dat sauna’s (in wellness centra, hierna sauna’s genoemd) en jacuzzi’s (privé en niet-privé, hierna jacuzzi’s genoemd) vaker dan andere potentiële bronnen positief zijn voor Legionella, en dat er geregeld een genotypische match kan worden gemaakt tussen patiëntisolaten en omgevingsstammen uit sauna- of jacuzzimonsters. Deze bevindingen waren de aanleiding om de criteria voor bemonstering aan te passen waardoor sauna’s en jacuzzi’s die door een patiënt als potentiele bron worden genoemd, vaker bemonsterd zullen worden.
Aanpassing van de BEL-bemonsteringscriteria
Hoe werkt de BEL?
Sinds 2002 bestaat er in Nederland een systematische registratie van potentiële besmettingsbronnen van patiënten met legionellapneumonie. De registratie wordt bijgehouden door de BEL vanuit het Streeklaboratorium voor de Volksgezondheid Kennemerland in Haarlem (SLH), het nationale referentielaboratorium voor Legionella. (1) De BEL voert sinds 2006 verschillende taken uit voor het RIVM/Centrum Infectieziektebestrijding (CIb) op het gebied van de legionellabestrijding in Nederland, en werkt samen met de GGD’en om besmettingsbronnen van legionella-pneumonie te identificeren en te elimineren met als doel om nieuwe ziektegevallen te voorkomen. De BEL bestaat uit een arts infectieziektebestrijding?, een klinisch epidemioloog, een medisch secretaresse en bemonsteraars. De BEL heeft de beschikking over een laboratorium waar omgevingsmonsters kunnen worden geanalyseerd op de aanwezigheid van Legionella. Klinische isolaten worden door de microbiologische laboratoria in Nederland ingestuurd naar het SLH en getypeerd bij het moleculaire laboratorium. Om genotypische matches tussen patiënt en bron te kunnen vaststellen, worden de klinische isolaten genotypisch vergeleken met omgevingsstammen (gevonden bij bemonsteringen van potentiele bronnen).
Het RIVM/CIb wordt wekelijks geïnformeerd over de resultaten van de bronopsporing, de klinisch epidemioloog overlegt wekelijks met contactpersonen van de RIVM/CIb-afdelingen Epidemiologie en Surveillance (EPI) en de Landelijke Coördinatie Infectieziektebestrijding (LCI), en iedere 6 weken wordt er een uitgebreide rapportage van de bevindingen van BEL besproken bij het LCI-casuïstiekoverleg.
De bronopsporing na een nieuwe melding van een patiënt met legionellapneumonie aan de GGD, bestaat uit 2 delen. Allereerst wordt de ’Vragenlijst Legionella-pneumonie’ door de GGD afgenomen bij de patiënt. De mogelijke besmettingsbronnen waaraan de patiënt tijdens de incubatietijd werd blootgesteld, worden door de GGD gemeld in Osiris, waarna deze door de BEL in een aparte bronnendatabase worden geregistreerd, ten behoeve van het opsporen van clusters. Vervolgens zal de BEL in opdracht van de GGD, potentiële besmettingsbronnen gaan bemonsteren als de melding aan 1 van de volgende voorwaarden voldoet:
- er is sprake van een locatiecluster van 2 of meer patiënten binnen 2 jaar gerelateerd aan dezelfde potentiele bron.
- er is sprake van een geografisch cluster van 3 of meer patiënten binnen een half jaar, woonachtig binnen een straal van 1 km van elkaar.
- er is een solitaire patiënt in een zorginstelling.
- er is een solitaire patiënt met een positieve sputumkweek, waarbij het woonhuis niet de enige potentiële besmettingsbron is
Aan de hand van de verkregen informatie uit de melding wordt door de GGD – eventueel in samenspraak met de BEL - een inventarisatie gemaakt van de potentiële bronnen van de infectie. Wanneer de casus binnen de BEL-bemonsteringscriteria valt, kan de GGD de bemonstering en het microbiologisch onderzoek van de bronnen in Nederland laten uitvoeren door de BEL. De (water)monsters, worden in het SLH verder gekweekt op Legionella. Waar mogelijk worden bovendien de legionella-isolaten van de patiënt en de bij bemonstering verkregen stammen genotypisch met elkaar vergeleken om een mogelijke match te ontdekken.
BEL-resultaten 2002-2012
De resultaten van de uitgevoerde bemonsteringen variëren per jaar, maar analyse van de BEL-resultaten in de periode augustus 2002- juli 2012 liet zien dat in ongeveer 25% van de bemonsteringen Legionella zat. (1) Deze percentages verschilden echter aanzienlijk tussen de verschillende bronnen. De bronnen die het vaakst (85%) positief waren voor Legionella waren sauna’s. (2) Verder werden in de periode 2002-2017, na bemonstering van sauna’s en jacuzzi’s, 9 genotypische matches gemaakt tussen patiëntisolaten en legionellastammen. Ter vergelijking: het totale aantal matches in deze periode was 50.
Sauna's en jacuzzi's
In de periode 2011-2016 werden door de BEL verschillende sauna’s en jacuzzi’s bemonsterd en onderzocht op de aanwezigheid van Legionella. In tabel 1 staan de resultaten weergegeven. De positieve bemonsteringsresultaten zijn onderverdeeld in bemonsteringen waarbij Legionella pneumophila werd aangetroffen in 1 of meer monsters, en bemonsteringen waarbij Legionella non-pneumophila werd aangetroffen. L. pneumophila is het type Legionella dat het vaakst werd gevonden bij patiënten met legionellapneumonie patiënten (>90%) en was meer pathogeen dan Legionella non-pneumophila. De betekenis van het aantonen van Legionella non-pneumophila in watermonsters is minder eenduidig. Legionella non-pneumophila wordt frequenter in watermonsters gevonden, maar leidt zelden tot ziekte. De aanwezigheid van Legionella non-pneumophila in het watersysteem is echter wel een signaal voor de beheerder dat er een verhoogd risico is op de groei van Legionella pneumophila in het systeem.
Tabel 1. Bemonsteringsresultaten 2011-2016 voor sauna’s en jacuzzi’s uitgevoerd door de BEL
| Sauna’s, n(%) | Jacuzzi’s, n(%) | ||||||
Jaar | L. pneumophila | L. non-pneumophila | Nega-tief | Totaal | L. pneumophila | L. non-pneumophila | Nega-tief | Totaal |
2011 | - | 1 | 1 | 2 | - | - | 3 | 3 |
2012 | - | - | - | - | 1 | - | 1 | 2 |
2013 | - | - | - | - | 2 | - | 1 | 3 |
2014 | 2 | - | - | 2 | - | - | - | - |
2015 | - | - | - | - | 1 | - | - | 1 |
2016 | 1 | 1 | - | 2 | 1 | - | 1 | 2 |
Tot | 3 (50) | 2 (33) | 1 (17) | 6 (100) | 5 (45) | - | 6 (55) | 11 (100) |
Gegevens zijn weergegeven als aantal (%)
Extra criterium voor bemonstering
Deze resultaten komen grotendeels overeen met de eerder gerapporteerde cijfers (1): meer dan 80% van de sauna’s, en bijna de helft van jacuzzi’s die waren bemonsterd, waren positief voor Legionella (met de aantekening dat de periodes enigszins overlappen). Dit percentage is aanzienlijk hoger dan bij de andere bronnen. Op basis van deze gegevens is eind 2017 een vijfde criterium toegevoegd aan de bemonsteringscriteria:
- er is een solitaire patiënt waarbij een sauna en/of een jacuzzi is/zijn geïdentificeerd als potentiële bron(nen).
In de periode 2011-2016 werden bij de 2212 gemelde patiënten met legionellapneumonie in totaal 3437 potentiële besmettingsbronnen gerapporteerd, waaronder 50 sauna’s of jacuzzi’s. Van deze 50 sauna’s en jacuzzi’s werden 37 niet bemonsterd omdat de gerelateerde patiënten niet voldeden aan de bemonsteringscriteria (n=32), na overleg met de GGD (n=4), of omdat bemonsteren niet meer mogelijk was (n=1).
De aanpassing van de bemonsteringscriteria zal waarschijnlijk leiden tot 5-6 extra bemonsteringen van sauna’s en/of jacuzzi’s per jaar. Als er een sauna of jacuzzi positief voor Legionella wordt bevonden, is het de GGD die besluit al dan niet in samenwerking met ILT of een andere toezichthouder welke maatregelen worden genomen om het risico op verdere besmetting te beperken. Voor eigenaren van privé jacuzzi’s zal dan het geven van voorlichting over het belang van onderhoud en desinfectie de belangrijkste maatregel zijn.
Conclusie
Uit de bemonsteringsresultaten van de BEL blijkt dat sauna’s en jacuzzi’s vaker positief zijn voor Legionella dan andere bronnen waarin Legionella voor kan komen. Ook is er regelmatig een genotypische match tussen patiëntisolaten en omgevingsstammen uit sauna- of jacuzzimonsters. Deze bevindingen hebben geleid tot het uitbreiden van de BEL-bemonsteringscriteria waardoor meer sauna’s en jacuzzi’s bemonsterd kunnen worden.
Auteurs
S. Euser1, P. Brandsema2, H. Ruijs2
- Stichting Streeklaboratorium voor de Volksgezondheid Kennemerland
- Centrum Infectieziektebestrijding, RIVM, Bilthoven
Correspondentie
Literatuur
- Results from the National Legionella Outbreak Detection Program, the Netherlands, 2002-2012. Den Boer JW, Euser SM, Brandsema P, Reijnen L, Bruin JP. Emerg Infect Dis 2015;21(7):1167-1173.
- Wellness centres: an important but overlooked source of Legionnaires’ disease. Eight years of source investigation in the Netherlands, 1 August 2002 to 1 August 2010. Euser SM, Bruin JP, Van der Hoek W, Schop WA, Den Boer JW. Eurosurveillance 2012;17 (8):pii=20097.
Infectieziekten Bulletin, jaargang 29, nummer 9, November 2018
Rabiëscasuïstiek in de GGD-regio Utrecht
Artsen en verpleegkundigen infectieziektebestrijding houden zich dagelijks bezig met reizigers die mogelijk zijn blootgesteld aan rabiës. Het is een redelijke verwachting dat de vraag naar rabiës- postexpositieprofylaxe (PEP) zal toenemen in de toekomst, aangezien steeds meer mensen naar verre gebieden reizen waar rabiës endemisch is en er meer awareness bestaat over de risico’s. (1,2,3) PEP bestaat uit vaccinaties en menselijke antirabiësimmunoglobulines (MARIG). Met name deze laatste zijn duur en schaars. (4) Bovendien kampten de leveranciers van vaccins die in Nederland geregistreerd zijn (Rabipur® en Rabies Merieux®) deze zomer nog met tekorten. De indicatiestelling en toediening van rabiës PEP vormt dus een steeds grotere belasting voor het zorgsysteem. Dit artikel beschrijft onderzoek naar andere preventiestrategieën die kosteneffectiever zijn.
Rabiëscasuïstiek in de GGD-regio Utrecht
Een mogelijke effectieve preventiestrategie is het voorkómen en verminderen van incidenten met dieren in het buitenland. Hiervoor is informatie over de risicofactoren voor blootstelling onontbeerlijk. Tot op heden zijn slechts enkele studies gedaan naar determinanten voor mogelijke blootstelling van reizigers aan rabiës. (5,6) In het kader van het ZonMw project: Predictors of rabiës exposure in travelers (website), waarin o.a. GGD regio Utrecht en het Centrum Infectieziektebestrijding (CIb) van het RIVM samenwerken is er binnen GGD regio Utrecht een vooronderzoek uitgevoerd. Het doel van dit kleinschalige dossieronderzoek was het in kaart brengen van de populatie reizigers die in 2016 de GGD regio Utrecht consulteerden na een mogelijk risicocontact met een rabide dier in het buitenland. Daarnaast is onderzocht wat voorspellers zijn voor overleg met de Landelijke Coördinatie Infectieziektebestrijding (LCI) van het CIb.
Methode
Voor dit retrospectieve dossieronderzoek, uitgevoerd door een student Geneeskunde (Universiteit Utrecht) in augustus 2017, zijn alle 114 casussen in HPZone waarbij sprake was van mogelijke blootstelling aan het rabiësvirus in het jaar 2016 geselecteerd. Inclusiecriteria voor dit onderzoek waren: 1. De mogelijke blootstelling heeft plaatsgevonden in een R1 land (enzoötische gebieden) (Figuur 1) en 2. verwonding betreft een type II of III blootstelling (Tabel 1). Uiteindelijk zijn 96 casussen geïncludeerd voor analyse op basis van bovenstaande criteria. Verschillende eigenschappen van elke casus zijn verzameld (zie Tabel 2). Vervolgens zijn met behulp van multivariabele logistische regressie (SPSS version 25) onafhankelijke voorspellers geïdentificeerd voor de uitkomstmaat ‘overleg met LCI’ (ja/nee).
Tabel 1. Typen blootstelling
Type I | Aanraken, voeren, likken op intacte huid. |
Type II | Knabbelen aan de intacte huid met als gevolg kleine krassen of ontvellingen zonder bloeden. |
Type III | Een of meer transdermale beten of krassen, lik op beschadigde huid, verontreiniging slijmvliesmembraan met speeksel. |
Tabel 2. Kenmerken van reizigers die mogelijk zijn blootgesteld aan rabiës, N=96
| Overleg met LCI | |
Ja (n=33) | Nee (n=63) | |
Geslacht: n (%) Man Vrouw |
13 (39) 20 (61) |
31 (49) 32 (51) |
Leeftijd: n Mediaan (range) |
25 (5-78) |
28 (4-65) |
Werelddeel: n (%) Zuidoost-Azië Afrika Zuid-Amerika Overig |
9 (27) 5 (15) 8 (24) 11 (33) |
44 (70) 5 (8) 4 (6) 10 (16) |
Dier: n (%) Hond Aap Kat Overig Onbekend |
17 (52) 4 (12) 8 (24) 4 (12) 0 (0) |
29 (46) 22 (35) 9 (14) 2 (3) 1 (2) |
Blootstelling: n (%) Type II Type III |
1 (3) 32 (97) |
36 (57) 27 (43) |
Plaats wond: n (%) Bovenste ledematen Onderste ledematen Hoofd borstkas/rug Onbekend |
16 (48) 11 (33) 1 (3) 2 (6) 3 (9) |
24 (38) 27 (43) 2 (3) 2 (3) 8 (13) |
Resultaten
Het totaal aantal geïncludeerde rabiëscases (n=96) liet een kleine meerderheid van vrouwen zien (54%). De mediane leeftijd bedroeg 26 jaar, met een range van 4 tot 74 jaar. In totaal bezochten zij 27 verschillende R1 landen (figuur 1). De top 3 landen - Thailand (27%), Indonesië (20%) en Marokko (5%) - vormden samen meer dan de helft van alle casuïstiek. Honden veroorzaakten het vaakst een verwonding (49%), gevolgd door apen (27%) en katten (18%). Een klein aantal diersoorten, waaronder vleermuizen, eekhoorns, varkens en wasberen vormden de restgroep. De meest voorkomende locaties voor beten en krabben waren de hand (24%) en de kuit (14%). Het merendeel van de blootstellingen was beoordeeld als type III (62%). In 49% van de gevallen ontbrak er specifieke informatie over de aanleiding tot het bijt- of krabincident in het registratiesysteem van de GGD (HPZone). Voorbeelden van incidenten die wel beschreven werden zijn: het aaien van een (slapend) dier, foto’s maken, het bezoeken van een Monkey Forest, dieren voeren, dieren wegduwen (van kinderen), spelen met dieren (met name puppy’s en kittens). 8 reizigers (8%) hadden zich voor de reis laten vaccineren tegen rabiës.
Figuur 1. Wereldkaart met R1-landen waar mogelijke blootstelling plaatsvond in 2016 bij bezoekers van GGD regio Utrecht. Een R1-land is een land met een hoog risico op transmissie volgens de classificatie van het Landelijk Coöordinatiecentrum Reizigersadvisering (LCR).
In totaal zijn 33 cases (34%) overlegd met de LCI, met als hoofdreden het bespreken van de indicatie voor immunoglobulinen. 17 hiervan hadden een indicatie en ontvingen de immunoglobulinen in Nederland. De overige 16 hadden geen indicatie voor immunoglobulinen. Het is aannemelijk dat in deze cases in ieder geval twijfel was over de indicatie voor immunoglobulinen. Daarnaast ontvingen in totaal 16 personen immunoglobulinen in het buitenland, waarvan 11 in Zuidoost-Azië. In 3 gevallen (3%) was repatriëring naar Nederland noodzakelijk omdat PEP lokaal niet beschikbaar was. Repatriëring betrof in alle 3 gevallen reizigers naar Zuid-Amerika (Nicaragua, Peru en Bolivia).
Met behulp van logistische regressieanalyse zijn onafhankelijke voorspellers geïdentificeerd voor de uitkomstmaat ‘overleg met LCI’ (ja/nee). De eigenschappen werelddeel, soort dier en type blootstelling waren significant geassocieerd met de uitkomstmaat in een univariaat model. Als grens voor inclusie in het multivariabele model is een p waarde van <0.20 gebruikt. In het multivariabele model waren de significante voorspellers voor de uitkomstmaat overleg met de LCI (Tabel 3), Zuid-Amerika, overig werelddeel, overig dier en type III-blootstelling. Hieruit kan worden afgeleid dat de kans op het plaatsvinden van overleg met de LCI door medewerkers van de GGD regio Utrecht toeneemt als een reiziger een type III-verwonding heeft opgelopen (OR 82,7), als het incident plaatsvond in Zuid-Amerika (OR 12,2) óf een land dat niet in Zuidoost-Azië of Afrika ligt (OR 4,9) en als het ging om een dier uit de categorie overig (OR 14,8).
Tabel 3. Logistische regressieanalyse ter identificatie van onafhankelijke voorspellers voor de uitkomstmaat ‘overleg met LCI’ (ja/nee)
Variabele | Significantie | Odds ratio |
Land Zuidoost-Azië Afrika Zuid-Amerika Overig |
Referentie 0,549 0,007 0,039 |
Referentie 1,7 12,2 4,9 |
Dier Hond Aap Kat Overig |
Referentie0,821 0,289 0,045 |
Referentie 1,2 2,4 14,8 |
Type blootstelling II III |
Referentie 0,001 |
Referentie 82,7 |
Conclusie/Discussie
Deze retrospectieve dossierstudie geeft een overzicht van de rabiëscasuïstiek in het jaar 2016 van de GGD regio Utrecht. Hieruit bleek dat de meeste krab- en bijtincidenten plaatsvonden in Thailand. Dit is in overeenstemming met de resultaten uit een recente Nederlandse studie die aantoont dat een reis naar Zuidoost-Azië een hogere kans op expositie met zich meebrengt dan een reis naar een andere bestemming. Dit beeld wordt vertekend door het feit dat er in absolute aantallen veel mensen naar Thailand op vakantie gaan. Welke andere factoren hierbij een rol spelen is niet onderzocht. (6) Daarnaast is er een analyse uitgevoerd om voorspellers te identificeren die de kans op overleg met de LCI doen toenemen.
Verder doet het oplopen van een type III-blootstelling de kans op een overlegsituatie met de LCI sterk toenemen. Dit is geheel in overeenkomst met de LCI-richtlijn, waarin wordt geadviseerd om contact te leggen met de LCI bij een indicatie voor MARIG, omdat dit alleen via de LCI verkrijgbaar is. Bij de GGD regio Utrecht wordt één derde van de rabiëscasuïstiek over PEP bij het LCI gemeld. Uit een oriënterend vervolgonderzoek van de LCI onder 20 GGD’en blijkt dat er gemiddeld 56% van de rabiëscases wordt overlegd met de LCI (range 13%-100%). Hoewel hierbij rekening gehouden moet worden met onjuiste of dubbele documentatie, geeft dit een redelijk beeld van de verschillen tussen GGD’en.
Daarnaast is het maken van een reis naar een land in Zuid-Amerika een significante voorspeller voor het plaatsvinden van overleg met de LCI. Ook deden alle gevallen van repatriëring zich in Zuid-Amerika voor. Mogelijk komt dit door de beperkte beschikbaarheid van immunoglobulinen in deze landen. (7) Verder onderzoek zal moeten uitwijzen of deze groep reizigers een specifieke doelgroep voor een interventie vormt.
Een knelpunt in de registratie van rabiëscasuïstiek bij de GGD regio Utrecht was het ontbreken van specifieke informatie over de aanleiding van het bijt- of krabincident in HP-Zone. Om in de toekomst beter en gericht onderzoek te kunnen doen, dienen gegevens over de toedracht van het incident zorgvuldig en volledig te worden gedocumenteerd.
Take home messages
- De meeste krab- en bijtincidenten van verdachte rabide dieren deden zich voor in Zuidoost-Azië.
- Het hebben van een type III-verwonding is de meest voorspellende eigenschap van reizigers die leidt tot overleg door de GGD met de LCI (ook indien de GGD zeker is van de indicatie is er altijd een kort overlegmoment).
- Andere voorspellers zijn reizen richting Zuid-Amerika en incidenten met dieren anders dan een aap, hond of kat.
- Reizigers richting Zuid-Amerika vormen mogelijk een nieuwe specifieke doelgroep voor interventie.
- Complete registratie in HP Zone is nodig om vervolgonderzoek naar de toedracht van incidenten mogelijk te maken.
Dit artikel is tot stand gekomen in samenwerking met het team Infectieziektebestrijding van de GGD regio Utrecht. Bijzondere dank gaat uit naar de alle verpleegkundigen infectieziektebestrijding voor de uitstekende hulp.
Auteurs
L. van Dee1, M. Dimmendaal2, S. Bantjes3, M. Haverkate3, R. van Kessel2
- Selective Utrecht Medical Master (SUMMA), Universitair Medisch Centrum Utrecht
- GGD regio Utrecht
- Centrum Infectieziektebestrijding, RIVM
Correspondentie
Literatuur
- Christiansen AH, Rodriguez AB, Nielsen J, Cowan SA. Should travellers to rabies-endemic countries be pre-exposure vaccinated? An assessment of post-exposure prophylaxis and pre-exposure prophylaxis given to Danes travelling to rabies-endemic countries 2000–12. J Travel Med 2016; 23(4): 1-6.
- Lankau EW, Cohen NJ, Jentes ES et al. Prevention and Control of Rabies in an Age of Global Travel: A Review of Travel‐and Trade‐Associated Rabies Events–United States 1986–2012. Zoonoses Public Health 2014; 61(5): 305-316.
- Freedman DO, Chen LH, & Kozarsky PE. Medical considerations before international travel. N Engl J Med 2016; 2016(375): 247-260.
- Bourhy H, Goudal M, Mailles A, Sadkowska-Todys M, Dacheux L, & Zeller H. Is there a need for anti-rabies vaccine and immunoglobulins rationing in Europe? Eurosurveillance 2009; 14(13).
- Shaw MT, Visser J, Edwards C. Rabies postexposure consultations in new zealand from 1998 to 2012. Journal of travel medicine 2014; 22(1): 31-38.
- Wieten RW, Tawil S, Van Vugt M, Goorhuis A, Grobusch, MP. Risk of rabies exposure among travellers. Neth J Med 2015; 73: 219-26.
- Jentes ES, Blanton, JD, Johnson, KJ et al. The global availability of rabies immune globulin and rabies vaccine in clinics providing direct care to travelers. Journal of travel medicine 2013; 20(3): 148-158.
Infectieziekten Bulletin, jaargang 29, nummer 9, November 2018
Meldingen van voedselgerelateerde infecties en vergiftigingen in 2017
Voedselgerelateerde infecties en vergiftigingen leiden wereldwijd tot aanzienlijke ziektelast. In Nederland is de schatting van deze ziektelast mede gebaseerd op het gemelde aantal zieken via de meldingsplicht en laboratoriumsurveillance. In 2017 waren er in Nederland naar schatting 629.000 aan voedsel gerelateerde infecties en vergiftigingen, waarbij Campylobacter de grootste ziektelast en meeste kosten veroorzaakte. (1) Door middel van surveillance en meldingsplicht van aan voedsel gerelateerde uitbraken en ziekte door specifieke micro-organismen, worden het vóórkomen van ziekteverwekkers, risicovolle omstandigheden en betrokken voedselproducten inzichtelijk. Ook worden zo eventuele trends gevolgd. Dit artikel is een samenvatting van het jaarrapport Registratie voedselgerelateerde uitbraken in Nederland, 2017. (2) Het jaarrapport geeft een overzicht van de in Osiris gemelde voedselgerelateerde uitbraken door de Nederlandse Voedsel- en Warenautoriteit (NVWA) en door de GGD’en. Osiris is een webgebaseerd registratiesysteem dat wordt beheerd door het Centrum Infectieziektebestrijding (CIb) van het RIVM. Verder geven wij in dit artikel een overzicht van de meldingen door de GGD van patiënten met mogelijk aan voedsel gerelateerde bacillaire dysenterie (shigellose), botulisme, brucellose, buiktyfus, cholera, hepatitis A en paratyfus A, B en C.
Meldingen van voedselgerelateerde infecties en vergiftigingen in 2017
Registratie in Osiris
De NVWA en GGD’en onderzoeken de oorzaken van vermoedelijke voedselgerelateerde infecties en - vergiftigingen (de besmettingsbron en de ziekteverwekker), elk vanuit hun eigen werkveld. De NVWA onderzoekt het besmette voedsel en de locatie waar het wordt verkocht en bereid. De GGD ondervraagt de personen die hebben blootgestaan aan besmet voedsel en voert eventueel fecesonderzoek uit. Deze gegevens vullen elkaar aan en bij een aantal uitbraken werken NVWA en GGD actief samen tijdens het onderzoek. In geval van een bovenregionale uitbraak is ook het Centrum Infectieziektebestrijding (CIb) van het RIVM betrokken.
Door de NVWA
De wijze waarop meldingen bij de NVWA worden behandeld, is al uitgebreid beschreven. (2, 3) In het kort: personen met ziekteverschijnselen die vermoeden dat deze veroorzaakt zijn door voedsel, kunnen telefonisch contact opnemen met het Klantcontactcentrum van de NVWA of het meldingenformulier via de website van de NVWA invullen (https://www.nvwa.nl/over-de-nvwa/inhoud/contact/klacht-indienen-bij-de-nvwa). Een binnengekomen melding wordt geregistreerd in een meldingssysteem en voorzien van een meldingsnummer. Bij meldingen waarbij er voldoende aanknopingspunten zijn om er directe opvolging aan te geven, voert een inspecteur een hygiëne-inspectie uit en neemt waar mogelijk voedsel- en/of omgevingsmonsters af voor laboratoriumonderzoek. De bevindingen van de inspecteur, de resultaten van het laboratoriumonderzoek en de eindconclusie worden terug gerapporteerd aan het Klantcontactcentrum die de melder over de uitkomsten informeert.
Het criterium voor registratie door de NVWA in Osiris is sinds 2015: alle niet-anonieme meldingen van voedselgerelateerde uitbraken met 2 of meer patiënten, ongeacht of er monsters genomen zijn of niet. Meldingen van 1 enkele patiënt en anonieme meldingen worden door de NVWA niet meer doorgegeven aan het CIb voor de jaarrapportage. Wel worden als daar aanleiding voor is inspecties uitgevoerd waarbij expliciet aandacht wordt gegeven aan de inhoud van de meldingen.
Door de GGD
Artsen en laboratoria melden aan de GGD in het kader van de meldingsplicht. De GGD onderzoekt de binnengekomen meldingen en registreert ze geanonimiseerd in Osiris. De registratiecriteria zijn: 2 of meer patiënten met dezelfde ziekteverschijnselen of bij wie dezelfde ziekteverwekker is aangetoond, en een onderlinge epidemiologische of microbiologische relatie wijzend op voedsel als besmettingsbron. De onderlinge relatie kan blijken uit een vergelijkbaar klinisch beeld, opvallende overeenkomst in tijdstip van ziekte, dezelfde ziekteverwekker of hetzelfde subtype. Ook individuele patiënten met specifieke infectieziekten moeten gemeld worden. Voor deze ziekten geldt een meldingsplicht vanwege de ernst van de ziekte of het risico voor besmetting van mens op mens. In dit artikel worden resultaten getoond van de volgende meldingsplichtige ziekten: bacillaire dysenterie (shigellose), botulisme, brucellose, buiktyfus, cholera, hepatitis A en paratyfus A, B en C.
Voedselgerelateerde uitbraken
Aantal meldingen
De NVWA registreerde 660 meldingen van voedselgerelateerde uitbraken in Osiris met 2957 patiënten. Door de GGD’en werden 28 meldingen gedaan van voedselgerelateerde uitbraken met 641 patiënten. In totaal werden in 2017 666 uitbraken gemeld met 2995 patiënten; hiervan werden 22 uitbraken door beide instanties gemeld.
Het aantal uitbraken en aantal patiënten is daarmee voor het tweede jaar op rij gestegen (2016: 594 uitbraken, 2731 patiënten; 2015: 406 uitbraken, 1850 patiënten). In de jaren daarvoor waren er meerdere fluctuaties, die deels veroorzaakt werden door wijzigingen in de meldingscriteria van de NVWA. In de periode 2015 tot en met 2017 waren er geen wijzigingen in de criteria. Er waren ook geen grote verschillen in grootte van de uitbraken in deze 3 jaren; dit is ook te zien aan het gemiddelde aantal zieken per uitbraak: 4,6 patiënten in 2015 en 2016 en 4,5 patiënten in 2017. 85% van de uitbraken bestonden uit 2 tot en met 4 patiënten en bij 11% van de uitbraken waren 5 tot en met 9 patiënten betrokken. De 9 grootste uitbraken hadden 45 tot en met 162 patiënten.
In vergelijking met de GGD, vormden de grotere uitbraken bij de NVWA met 10 of meer patiënten, maar een klein percentage van al hun meldingen (50%, n=14 versus 4%, n=29). Twaalf grote uitbraken werden door NVWA én GGD geregistreerd in Osiris.
Zowel bij uitbraken die door NVWA én GGD werden gemeld als bij uitbraken die door 1 van de 2 werden gemeld, was er contact en afstemming tussen beide partijen. In 2017 was dit het geval bij 40(6%) van de 666 uitbraken. Hoe groter de uitbraak hoe meer contact : bij uitbraken met minder dan 10 patiënten was dit 4% (23/635), bij uitbraken met 10 tot 19 patiënten (6/17) was dit 35% en bij uitbraken met 20 of meer patiënten 79% (11/14). Ook was er vaker contact bij uitbraken waarbij een ziekteverwekker was gevonden (64%) dan daar waar dat niet het geval was (2%).
Ziekteverwekkers
Bij 45 uitbraken (7%) werd melding gemaakt van een ziekteverwekker (Tabel 1). Bij 29 uitbraken (4%) werd een ziekteverwekker bij 1 of meer patiënten aangetroffen. Hiervan werden 22 gemeld via GGD (22/28 = 79%) en 7 door de NVWA.
Bij de patiënten werd voornamelijk Salmonella (in 15 uitbraken) aangetoond, gevolgd door norovirus (in 6 uitbraken) en Campylobacter (in 5 uitbraken).Verder werd bij 3 uitbraken respectievelijk Shigella flexneri, hepatitis A-virus en lintworm aangetoond. Bij 20 uitbraken (3%) gemeld door de NVWA werd een ziekteverwekker aangetoond in voedsel- of omgevingsmonsters (20/660 = 3%; meldingen met monstername: 20/200 = 10%). In 15 uitbraken werd norovirus aangetroffen: 14 keer in omgevingsmonsters en eenmaal in oesters. Verder werd 2 keer histamine aangetroffen, een eiwit dat in grote(re) hoeveelheden klachten kan veroorzaken, 1 keer Bacillus cereus en 1 keer Stafylococcus aureustoxine + Bacillus cereus.
Tabel 1. Uitbraken van voedselgerelateerde infecties en - vergiftigingen en de betrokken patiënten, naar gedetecteerde ziekteverwekker in voedsel en/of patiënten, 2017
Ziekteverwekker | Totaal | Ziekteverwekker aangetoond in | ||
voedsel* | humaan | |||
uitbraken(%) | zieken(%) | uitbraken(%) | uitbraken(%) | |
Salmonella spp | 15 (2,3) | 143 (4,8) | 1 (0,2) | 15 (2,3) |
Campylobacter spp | 5 (0,8) | 12 (0,4) | 0 | 5 (0,8) |
Shigella flexneri | 1 (0,2) | 162 (5,4) | 0 | 1 (0,2) |
Bacillus cereus | 1 (0,2) | 90 (3,1) | 1 (0,2) | 0 |
Staphylococcus aureus toxine & Bacillus cereus | 1 (0,2) | 47 (1,6) | 1 (0,2) | 0 |
Hepatitis A-virus | 1 (0,2) | 15 (0,5) | 0 | 1 (0,2) |
Norovirus | 18 (2,7) | 352 (11,8) | 15 (2,3) | 6 (0,9) |
Lintworm | 1 (0,2) | 2 (0,1) | 0 | 1 (0,2) |
Histamine-intoxicatie | 2 (0,3) | 9 (0,3) | 2 (0,3) | 0 |
Totaal bekend | 45 (6,8) | 832 (27,8) | 20 (3,0) | 29 (4,4) |
Onbekend | 621 (93,2) | 2163 (72,2) | 646 (97,0) | 637 (95,6) |
Totaal | 666 | 2995 | 666 | 666 |
Norovirus
In de periode 2009-2011 varieerde het aantal gerapporteerde uitbraken van norovirusinfecties tussen 3 en 6 per jaar. Hierbij moet opgemerkt worden dat ziekenhuizen buiten de registratie vallen omdat daar voedsel over het algemeen geen rol speelt bij uitbraken van norovirusinfecties; de transmissie verloopt met name van mens op mens. Sinds 2012 is er extra aandacht voor de invoer in Osiris van uitbraken waarbij norovirus aangetroffen is via positieve omgevingsmonsters, nadat geconstateerd was dat er sprake was van onderrapportage van deze uitslagen. (4) Sindsdien blijkt dat norovirus de belangrijkste veroorzaker bij de geregistreerde voedselgerelateerde uitbraken is. Positieve omgevingsmonsters zijn een indicatie dat voedsel tijdens de bereiding besmet is geraakt met norovirus. In de periode 2013-2017 werd 10 keer norovirus in schaal- en schelpdieren aangetroffen, voornamelijk in oesters, maar ook in mosselen en andere schelpdieren zoals kokkels. (2) In 2016 werden 4 uitbraken gelinkt aan norovirus in oesters (5), in 2017 1 uitbraak. De besmettingen hebben dan vrijwel altijd tijdens de primaire productiefase plaatsgevonden, waarin de schaal- en schelpdieren nog groeien in water waarin het virus, bijvoorbeeld doorhet lozen van rioolwater, terecht is gekomen.
Campylobacter en Salmonella
Over het algemeen werden tussen 2009 en 2016 evenveel uitbraken door Salmonella als door Campylobacter gemeld. Wel veroorzaakte Salmonella gemiddeld meer patiënten per uitbraak dan Campylobacter, met uitzondering van het jaar 2013 waarin slechts 3 salmonella-uitbraken met in totaal 7 patiënten werden gemeld. In 2017 werden meer uitbraken (15 versus 5) en meer zieken (143 versus 12)veroorzaakt door Salmonella gemeld, dan door Campylobacter.
In de laboratoriumsurveillance van het RIVM naar salmonellose is een stabilisatie te zien na een lange periode van geleidelijke afname met enkele piekjaren door grote(re) uitbraken. (6) Echter, het aantal diffuse en regionale salmonellose-uitbraken dat gedetecteerd is in de surveillance is wel gestegen van 17 in 2016 naar 23 in 2017. Het aantal isolaten binnen uitbraken is gedaald: in 2016 behoorde een kwart van de ingezonden isolaten tot een uitbraak, in 2017 was dat een vijfde van de isolaten.
Tot en met 2011 was er een toename van het aantal patiënten met campylobacteriose te zien in de laboratoriumsurveillance van het RIVM. Sindsdien is er sprake van een afname die ook doorzette in 2017. (6) Het aantal geregistreerde Campylobacter-uitbraken en de daarbij gemelde patiënten is laag in 2017 (5 uitbraken met 12 patiënten) en vergelijkbaar met 2014 (5 uitbraken met 11 patiënten). In de overige jaren sinds 2009 werden er jaarlijks 9 tot 18 uitbraken door Campylobacter geregistreerd met een oplopend gemiddeld aantal patiënten van 2,8 in 2009 naar 7,2 in 2016.
Inspecties en monstername
Bij 76% van de bij de NVWA binnengekomen meldingen werd vervolgonderzoek ingezet. In 40% van deze gevallen werden ook monsters genomen. In 10% van de monsternames werden ziekteverwekkers gevonden. Bij 216 van de 501 meldingen (43%) waarbij vervolgonderzoek werd uitgevoerd, bleek het betrokken bedrijf niet te voldoen aan de wettelijk vastgelegde hygiëneregels en - richtlijnen. Dit leidde tot de volgende maatregelen: aan 23% van de bedrijven werd een Schriftelijke Waarschuwing (SW) gegeven, aan 14% een Rapport van Bevindingen (RvB; boete) en aan 6% beide. Het percentage meldingen met een opgelegde maatregel (43%) was vergelijkbaar met 2015 (42%) en 2016 (41%). Wel lijken er meer RvB en juist minder SW te zijn opgemaakt in 2017 dan in 2015 en 2016.
Meldingsplichtige ziekten veroorzaakt door specifieke micro-organismen
Bacillaire dysenterie (shigellose), botulisme, brucellose, buiktyfus, cholera en hepatitis A en paratyfus A, B en C kunnen door voedsel veroorzaakt worden en zijn meldingsplichtig. Van deze ziekten kwam shigellose het meest voor (Tabel 2). De meeste shigella-infecties worden veroorzaakt door S. sonnei (58%) en S. flexneri (34%). Het aantal meldingen van hepatitis A is na jaren van daling sterk gestegen in 2017. De stijging is toe te schrijven aan een uitbraak met 3 verschillende hepatitis A-virusstammen onder mannen die seks hebben met mannen (MSM), waarbij de uitbraak zich ook verspreidde buiten deze risicogroep. (7) Paratyfus B (n=32) lijkt voor het derde jaar op rij licht te stijgen. Er werden in 2017 geen meldingen van botulisme en cholera gedaan.
Tabel 2. Aantal aangiftes van patiënten besmet met meldingsplichtige micro-organismen, mogelijk aan voedsel gerelateerd, 2008-2017
| 2017 | 2016 | 2015 | 2014 | 2013 | 2012 | 2011 | 2010 | 2009 | 2008 |
Shigellose | 428 | 445 | 479 | 360 | 432 | 498 | 435 | 454 | 385 | 433 |
Botulisme | 0 | 2 | 0 | 0 | 0 | 2 | 0 | 0 | 0 | 7 |
Brucellose | 2 | 4 | 9 | 2 | 5 | 2 | 1 | 6 | 3 | 7 |
Buiktyfus | 20 | 18 | 17 | 20 | 25 | 18 | 18 | 26 | 25 | 28 |
Cholera | 0 | 1 | 1 | 3 | 0 | 3 | 3 | 0 | 4 | 5 |
Hepatitis A | 374 | 81 | 80 | 105 | 110 | 121 | 125 | 262 | 176 | 189 |
Paratyfus A | 11 | 11 | 6 | 9 | 22 | 24 | 13 | 20 | 16 | 10 |
Paratyfus B | 32 | 29 | 23 | 8 | 14 | 18 | 27 | 15 | 16 | 26 |
Paratyfus C | 3 | 0 | 4 | 0 | 2 | 3 | 1 | 0 | 3 | 1 |
Veel van de infecties veroorzaakt door deze meldingsplichtige micro-organismen werden in het buitenland opgelopen (Tabel 3). Van de reisgerelateerde shigellose (63%) werd 43% opgelopen in 1 van de volgende landen: Indonesië (10%), Marokko (9%), India (7%), Kaapverdië en Egypte (elk 5%) en Cuba en Tanzania (elk 4%). Hepatitis A werd in 2017 minder vaak in het buitenland opgelopen dan in voorgaande jaren, dit komt voor een groot deel door de uitbraak onder MSM die de infectie voornamelijk in Nederland opliepen. Marokko werd het vaakst genoemd (22/103; 21%), gevolgd door Spanje (21/103; 20%; voornamelijk gerelateerd aan de uitbraak onder MSM). Van de reisgerelateerde infecties werd 90% (paratyfus A; 9/10), 88% (paratyfus B; 23/26) en 74% (buiktyfus; 13/18) in Azië opgelopen. Patiënten met buiktyfus noemden India (n=6) het vaakst als land van besmetting, en patiënten met paratyfus B noemden vooral Indonesië als land van besmetting (n=13). Paratyfus C werd opgelopen in de Dominicaanse Republiek, Marokko en Zuid-Afrika.
Meestal was de bron van de infectie niet duidelijk. Vooral als de patiënt in het buitenland is geweest, is het lastig nagaan of de infectie voedsel- of watergerelateerd was. Niettemin was een deel van de infecties met een zekere waarschijnlijkheid toe te schrijven aan aan voedsel- of waterconsumptie (Tabel 3). In 2017 was dit het hoogste voor paratyfus C (67%), paratyfus B (56%) en paratyfus A (55%). Hepatitis A werd vooral verspreid van mens op mens, slechts 11% werd veroorzaakt door water/voedselconsumptie. In 2017 was 47% van de hepatitis A-patiënten MSM en binnen de hepatitis A-uitbraak was dit zelfs 65%. In de periode 2005-2015 was er een toename van shigellose onder MSM . (8) In 2017 was 17% van de patiënten met shigellose MSM.
Tabel 3. Percentage van de meldingsplichtige aangiftes (GGD) van infectieziekten opgelopen in het buitenland en veroorzaakt door voedsel of water, indien bekend, 2014-2017
| % opgelopen in buitenland | % opgelopen door voedsel of water | ||||||
| 2017 | 2016 | 2015 | 2014 | 2017 | 2016 | 2015 | 2014 |
Shigellose | 63 | 59 | 61 | 56 | 36 | 29 | 30 | 26 |
Botulisme | - | 0 | - | - | - | 50 | - | - |
Brucellose | 100 | 50 | 100 | 100 | 50 | 25 | 44 | 50 |
Buiktyfus | 90 | 89 | 88 | 85 | 50 | 17 | 24 | 30 |
Cholera | - | 100 | 100 | 100 | - | 100 | - | 67 |
Hepatitis A | 28 | 58 | 59 | 53 | 11 | 28 | 36 | 32 |
Paratyfus A | 91 | 82 | 83 | 100 | 55 | 64 | 67 | 78 |
Paratyfus B | 81 | 86 | 78 | 63 | 56 | 41 | 52 | 38 |
Paratyfus C | 100 | - | 75 | - | 67 | - | 50 | - |
Discussie en conclusie
Dit artikel geeft een overzicht van het aantal door de NVWA en GGD’en in Osiris gemelde voedsel- gerelateerde uitbraken en patiënten die ziek werden door meldingsplichtige micro-organismen die deels aan voedsel gerelateerd kunnen zijn. De toename van het aantal gemelde uitbraken en patiënten is volledig toe te schrijven aan de stijging van de meldingen door de NVWA. Dit kan veroorzaakt zijn door een hoger aantal voedselgerelateerde uitbraken in Nederland en/of omdat er meer uitbraken gemeld werden bij de NVWA.
- De belangrijkste verwekker van voedselgerelateerde uitbraken was wederom norovirus, zowel in het aantal uitbraken als in het aantal patiënten.
- Van de meldingsplichtige micro-organismen besproken in dit artikel, leidden Shigella en het hepatitis A-virus tot het grootste aantal patiënten.
- Het aantal patiënten met shigellose per jaar is relatief stabiel, maar binnen deze groep stijgt het aantal MSM. (8)
- Het aantal meldingen van hepatitis A-infecties is in 2017, na jaren van daling, sterk gestegen als gevolg van de uitbraak onder MSM. (7, 9)
- Er bestaan meer ziekteverwekkers die via voedsel overgedragen kunnen worden met bijbehorende ziektespecifieke registraties. Als deze ziekteverwekkers daarnaast ook een zoönotische oorsprong kunnen hebben, zoals Campylobacter, Salmonella, STEC en Listeria, dan wordt het vóórkomen jaarlijks beschreven in het rapport Staat van Zoönosen. (6)
- Listeriose en STEC-infecties worden daarnaast ook in aparte artikelen besproken. (10, 11)
Het jaarlijkse rapport Disease burden of food-related pathogens in the Netherlands geeft een schatting van het aantal voedselgerelateerde infecties en - vergiftigingen. (1) In 2017 waren er naar schatting 629.000 infecties en vergiftigingen. Dit komt neer op ongeveer 163 miljoen euro aan kosten (o.a. direct medische kosten, kosten voor de patiënt en/of zijn familie, ziekteverzuim).
Rond 95% van de infecties verloopt asymptomatisch of mild. Vanuit de gedachte dat asymptomatische en milde infecties nauwelijks effect hebben op de volksgezondheid, lijkt registratie minder van belang. Toch kunnen deze infecties wel een aanwijzing zijn dat er levensmiddelen op de markt zijn gebracht die mogelijk een risico voor de volksgezondheid vormen. Zicht op deze infecties, inclusief de vraag of voedsel consumptie leidde tot ziekte, draagt bij aan een betere risicoschatting voor het doen van onderzoek en meer toezicht op voedselveiligheid. (12, 13) De moeilijkheid is echter dat niet iedere patiënt met een symptomatische dan wel asymptomatische infectie naar de huisarts gaat of contact opneemt met de NVWA. Daarnaast variëert de transmissie per ziekteverwekker: naast via voedsel lopen de routes van mens op mens, van dier op mens en via het milieu. (14)
De huidige meldingen zijn echter wel geschikt voor het geven van inzicht in de circulerende aan voedsel gerelateerde bacteriële en virale infecties en voor het volgen van veranderingen en trends in de tijd, wat behulpzaam kan zijn bij de prioritering van het toezicht van de NVWA.
Auteurs
I.H.M. Friesema1, I.A. Slegers-Fitz-James2, B. Wit2, E. Franz1
- Centrum Infectieziektebestrijding RIVM, Bilthoven
- Expertisecentrum Voedselvergiftiging, Nederlandse Voedsel- en Warenautoriteit (NVWA), Utrecht
Correspondentie
Literatuur
- Mangen M.J., Friesema I.H.M., Pijnacker R., Mughini Gras L., Van Pelt W. Disease burden of food-related pathogens in the Netherlands, 2017. Bilthoven: RIVM, 2018.
- Friesema I.H.M., Slegers-Fitz-James I.A., Wit B., Franz E. Registratie voedselgerelateerde uitbraken in Nederland, 2017. Bilthoven: RIVM, 2018.
- Aalten M., De Jong A., Stenvers O., et al. Staat van zoönosen 2010. Bilthoven / Den Haag: RIVM / nVWA, 2011.
- Friesema I.H.M., Boxman I.L.A., De Jong A.E.I., Van Pelt W. Registratie voedselinfecties en -vergiftigingen bij de NVWA en het CIb, 2012. Bilthoven: RIVM, 2013.
- Friesema I.H.M., Tijsma A.S.L., Slegers-Fitz-James I., Van Pelt W. Registratie voedselgerelateerde uitbraken in Nederland, 2016. Bilthoven: RIVM, 2017.
- Uiterwijk M., De Rosa M., Friesema I., et al. Staat van Zoönosen 2017. Bilthoven: RIVM, 2018.
- Friesema I.H., Sonder G.J., Petrignani M.W., et al. Spillover of a hepatitis A outbreak among men who have sex with men (MSM) to the general population, the Netherlands, 2017. Euro Surveill 2018; 23: pii=1800265.
- Pijnacker R., Friesema I.H.M., Franz E., Van Pelt W. Trends van shigellosemeldingen in Nederland, 1988-2015. Infectieziekte Bulletin 2017; 28: 121-8.
- Friesema I.H.M., Sonder G.J.B., Petrignani M.W.F., et al. Het effect van de wereldwijde uitbraak van hepatitis A onder MSM op de hepatitis A-epidemiologie in Nederland. Infectieziekte Bulletin 2018; 29.
- Friesema I.H.M., Kuiling S., van der Voort M., in 't Veld P.H., Heck M.E.O.C., Franz E. Surveillance van STEC in Nederland in 2017. Infectieziekte Bulletin 2018; 29.
- Friesema I.H.M., Kuiling S., Heck M.E.O.C., et al. Surveillance van Listeria monocytogenes in Nederland, 2017. Infectieziekte Bulletin 2018; 29.
- Batz M.B., Doyle M.P., Morris G., Jr., et al. Attributing illness to food. Emerg Infect Dis 2005; 11: 993-9.
- Painter J.A., Hoekstra R.M., Ayers T., et al. Attribution of Foodborne Illnesses, Hospitalizations, and Deaths to Food Commodities by using Outbreak Data, United States, 1998-2008. Emerg Infect Dis 2013; 19: 407-15.
- Havelaar A.H., Galindo A.V., Kurowicka D., Cooke R.M. Attribution of foodborne pathogens using structured expert elicitation. Foodborne Pathog Dis 2008; 5: 649-59.
Infectieziekten Bulletin, jaargang 29, nummer 9, November 2018