Infectieziekten Bulletin
December 2018 | Jaargang 29, nummer 10
https://magazines.rivm.nl/2018/04/infectieziekten-bulletin-0
Gesignaleerd
Buitenlandse signalen
Aanhoudende uitbraak van Salmonella Enteritidis gerelateerd aan Poolse eieren
De salmonella-enteritidisuitbraak in Europa gerelateerd aan Poolse eieren houdt aan. Sinds 2012 zijn 1412 patiënten gemeld. De meeste patiënten werden gerapporteerd tijdens de zomermaanden (Figuur 1). Uit gezamenlijke epidemiologische, microbiologische, omgevings- en traceringsonderzoeken uitgevoerd in 2016, bleek dat eieren afkomstig uit Polen de bron zijn van deze uitbraak. De controlemaatregelen die eind 2016 werden geïmplementeerd lijken ontoereikend. Het aantal nieuwe patiënten in 2017 en in 2018 was vergelijkbaar en ook het meldpatroon over de seizoenen kwam overeen. Sinds 1 februari 2017 zijn 532 patiënten met een bevestigde Salmonella Enteriditis en 166 met een vermoedelijke besmetting gemeld in 15 Europese landen, voornamelijk in het Verenigd Koninkrijk (412 bevestigde - en 3 vermoedelijke patiënten). Omdat er landen zijn waar moleculaire typering niet routinematig wordt uitgevoerd voor humane salmonella-enteritidisisolaten, zijn er waarschijnlijk meer landen betrokken bij deze uitbraak, bijvoorbeeld Bulgarije, Cyprus en Portugal. Een aantal patiënten heeft namelijk gemeld dat zij in deze landen waren geweest. In Nederland zijn slechts enkele patiënten gemeld in 2017 en 2018. Blijkbaar worden in Nederland geen tafeleieren meer afgenomen van het betrokken Poolse bedrijf. (Bronnen: ECDC (epidemiologische update), ECDC RRA )
Figuur 1. Aantal patiënten met Salmonella Enteritidis per eerste ziektemaand* en classificatie (bevestigde patiënten behoren tot 4 verschillende WGS-clusters) (n=1 412), EU/EEA, januari 2012-oktober 2018*maand van bemonstering of maand van ontvangst van monsters door het referentielaboratorium is gebruikt als gegevens over de eerste ziektemaand ontbreken. (Bron: ECDC)
Tularemie onder jagers in Beieren, Duitsland
In de gemeente Schwandorf in de Duitse deelstaat Beieren hebben 11 mensen vermoedelijk tularemie opgelopen. Het zijn 9 jagers die hebben meegedaan aan een hazenjacht op 27 oktober, en 2 medewerkers van een verwerkingsbedrijf voor wildvlees die ook contact hebben gehad met de tijdens de jacht gedode hazen. Zij werden van 4 tot 8 november met griepachtige symptomen opgenomen in het ziekenhuis. Het Robert Koch Instituut geeft aan dat op basis van de eerste serologische uitslagen van 2 patiënten en 3 jachthonden zeer waarschijnlijk sprake is van een infectie met Fransicella tularensis. Met PCR (polymerase chain reaction) is ook tularemie vastgesteld bij tenminste bij 1 van de hazen. Jagers worden geadviseerd om voorzorgsmaatregelen zoals het dragen van wegwerphandschoenen en een masker tijdens het bereiden van wildvlees. Wandelaars in de omgeving worden geadviseerd om dode en zieke dieren of dieren die abnormaal gedrag vertonen niet aan te raken. Wildvlees moet eerst goed worden gekookt of doorbakken voordat het geconsumeerd wordt. (Bronnen: Schwandorf Landratsambt, Gezondheidsautoriteiten Beieren, ProMed)
Patiënt met autochtone dengue in Catalonië, Spanje
De Catalaanse volksgezondheidsautoriteiten meldden het eerste geval van autochtone dengue in Catalonië. De patiënt is een jonge man uit Barcelona die niet recent buiten Catalonië was geweest. De eerste symptomen begonnen tussen 16 en 18 oktober 2018. Dit is de zesde patiënt in Spanje met autochtone dengue. De patiënt in Barcelona heeft geen bekende relatie met de 5 andere patiënten met autochtone dengue, waarvan 3 binnen 1 familie, die in oktober en begin november 2018 werden gemeld in Cadiz en Murcia. Het denguevirus wordt overgedragen door muggen, waaronder de Aziatische tijgermug Aedes albopictus. Omdat deze mug voorkomt in het zuiden en oosten van Spanje, is het voorkomen van enkele patiënten of kleine clusters van patiënten met autochtone dengue in die gebieden niet onverwacht. Op basis van de meest recente gegevens hebben de muggen zich gevestigd in de provincie Barcelona en in de regio Murcia, en zijn ze voor het eerst gesignaleerd in de provincie Cádiz. Het risico van verdere overdracht wordt als laag beschouwd vanwege de weersomstandigheden in de komende weken. (Bronnen: ECDC RRA, Catalaanse volksgezondheidsautoriteiten (ASPCAT)
Autochtone malaria in Griekenland
Griekse gezondheidsautoriteiten hebben sinds augustus van dit jaar 9 patiënten gemeld met autochtone malaria in het noordoosten van Griekenland. Twee patiënten waren besmet met Plasmodium vivax, vermoedelijk in de regio Oost-Macedonië/Thracië. Verder is een cluster van 7 patiënten gemeld, waarbij 6 besmet waren met Plasmodium vivax en bij 1 patiënt kon het type niet worden vastgesteld, maar wel dat het een P. non-falciparum was. Deze patiënten waren waarschijnlijk besmet geraakt in Echedoros in de regio Centraal-Macedonië. De eerste ziektedag van deze patiënten was tussen half september en begin oktober. Alle patiënten hebben zeer waarschijnlijk malaria opgelopen door een mug die besmet werd via een besmet persoon uit een malaria-endemisch gebied. De malaraisurveillance is verscherpt en er zijn veiligheidsmaatregelen genomen ten aanzien van bloedtransfusies. Griekenland werd in 1974 malariavrij verklaard. Autochtone transmissie is sinds 2009 incidenteel vastgesteld, vooral in landelijke waterrijke gebieden met relatief veel inwoners die afkomstig zijn uit gebieden waar Plasmodium vivax voorkomt. In 2011– 2012 werden in het zuiden van Griekenland enkele clusters gemeld van patiënten met autochtone malaria veroorzaakt door Plasmodium vivax. (Bronnen: Media, Keelpno)
Rabiës na een kattenbeet in Marokko
Op 12 november 2018 meldde Public Health England (PHE) een patiënt met rabiës die uit Marokko was teruggekeerd. De patiënt was daar besmet door een kat. Rabiës is een dodelijke ziekte. Hoewel het risico van mens-op-mensoverdracht verwaarloosbaar klein is, kregen de familie van de patiënt en het betrokken medisch personeel vaccinatie aangeboden. Volgens PHE hebben in de periode 2000 – 2017, 5 patiënten in het Verenigd Koninkrijk rabiës opgelopen na verblijf in het buitenland. Deze gebeurtenis onderstreept het belang van het informeren van reizigers over het risico van hondsdolheid in landen waar rabiës voorkomt. Niet alleen honden en katten, maar ook andere dieren zoals apen, vleermuizen en vossen kunnen rabiësvirus overbrengen door bijten, krabben of likken. Verder moeten zorgverleners alert blijven op rabiës om een mogelijk besmette patiënt tijdig postexpositieprofylaxe toe te dienen. (Bronnen: PHE, media)
World Malaria Report 2018
In november publiceerde de World Health Organization (WHO) het World Malaria Report. In 2017 werden wereldwijd de meeste malariapatiënten gediagnosticeerd op het Afrikaanse continent (200 miljoen patiënten; 92% van alle patiënten, gevolgd door Zuidoost-Azië (5%) en het oostelijke Middellandse Zeegebied (2%). In de periode 2010-2014 daalde het aantal patiënten wereldwijd van 72 naar 59 per 1000 mensen behorend tot de risicopopulatie. Sindsdien stagneert het aantal op 59 per 1.000. In Zuidoost-Azië bleef de incidentie dalen, terwijl andere WHO-regio’s weinig vooruitgang boekten. Er was zelfs sprake van een toename in Midden-en Zuid-Amerika, voornamelijk in Brazilië, Nicaragua en Venezuela.
De introductie van artemisinine gebaseerde combinatietherapie (ACT's) is een integraal onderdeel van de wereldwijde malariacontroleprogramma’s. Het is een wereldwijde prioriteit om de effectiviteit van deze antimalariamiddelen te waarborgen. Hoewel in Thailand, Cambodja, Vietnam en Laos resistentie is gemeld tegen een aantal geneesmiddelen, waaronder artemisinine (gedeeltelijke resistentie) en tegen partnergeneesmiddelen, is in deze landen het aantal malariapatiënten en patiënten die daaraan overlijden enorme gedaald. Tot nu toe is er in Afrika geen resistentie tegen artemisinine gemeld. (Bron: WHO)
Auteur
S. Mooij, Centrum Infectieziektebestrijding, RIVM
Correspondentie
Infectieziekten Bulletin, jaargang 29, nummer 11, december 2018
Antibioticaresistentie in de thuiszorg
Met dit onderzoek hebben we in kaart gebracht welke ervaringen thuiszorgorganisaties hebben met antibioticaresistantie, welke knelpunten zij zien, welke handvatten zij nodig hebben om op de juiste manier met antibioticaresistentie om te gaan en welke instanties/organisaties hen hierbij kunnen helpen.
Antibioticasresistentie in de thuiszorg
Wereldwijd groeit het probleem van antibioticaresistentie. Steeds meer bacteriën - bijzonder resistente micro-organismen (BRMO) genoemd - zijn resistent tegen meerdere soorten antibiotica. (1) Antibioticaresistentie is een risico voor de volksgezondheid, omdat infecties door resistente bacteriën lastig of soms niet te behandelen zijn. In Nederland komen deze infecties nog relatief weinig voor. Uit onderzoek is gebleken dat het aantal infecties door BRMO de afgelopen jaren ongeveer stabiel is gebleven. (2) Toch is in zorginstellingen het aantal uitbraken van infectieziekten door BRMO die resistent zijn voor ‘laatste-redmiddel-antibiotica’ (i.e. carbapenems) toegenomen. (2)
Om een landelijke aanpak van antibioticaresistentie mogelijk te maken heeft het ministerie van Volksgezondheid, Welzijn en Sport (VWS) Nederland opgedeeld in 10 regio’s, met elk een antibioticaresistentiezorgnetwerk. (3) Mensen uit verschillende disciplines en vakgebieden werken in deze zorgnetwerken samen. De GGD vertegenwoordigt in het netwerk de sector publieke gezondheidszorg. Een belangrijke taak van de GGD is het geven van voorlichting/scholing en advies aan onder andere thuiszorgorganisaties. (4)
Hoewel de GGD advies en ondersteuning kan bieden aan thuiszorgorganisaties bij vragen over gezondheid in het algemeen, blijkt uit de praktijk dat de GGD maar weinig door deze organisaties geconsulteerd wordt, terwijl andere zorginstellingen – zoals verpleeghuizen – de GGD hier vaker voor benaderen. (5) Uit een eerder onderzoek uitgevoerd door GGD West-Brabant blijkt dat veel thuiszorgmedewerkers niet goed weten dat de GGD hen kan ondersteunen en/of ervaren de drempel om contact op te nemen als te hoog. (6)
Het is niet bekend of thuiszorgorganisaties bij vragen over infectiepreventie en –bestrijding wel andere organisaties of experts inschakelen. Er zijn aanwijzingen dat er binnen thuiszorgorganisaties veel vragen en onduidelijkheden zijn over hoe om te gaan met antibioticaresistentie. Dit is vooral het gevolg van richtlijnen die soms tegenstrijdige adviezen geven en de verouderde richtlijnen van de Werkgroep Infectiepreventie (WIP). (7,8)
Methode
Wij hebben semigestructureerde diepte-interviews afgenomen. Deze methode van kwalitatief onderzoek doen wordt gebruikt wanneer men vooral inzicht wil krijgen in de ervaringen en meningen van mensen met een bepaald fenomeen en niet zozeer in het aantal keren dat een fenomeen voorkomt. De onderzoeksopzet werd beoordeeld door de Commissie Mensgebonden Onderzoek van het Radboudumc en werd vrijgesteld van de verplichtingen van de Wet medisch wetenschappelijk onderzoek (WMO).
Studiepopulatie
De studiepopulatie bestond uit medewerkers van 13 thuiszorgorganisaties uit gemeenten in de GGD regio’s Gelderland-Zuid en Gelderland-Midden. Er werd een lijst met thuiszorgorganisaties opgesteld door de GGD op basis van informatie van het internet.
Wij hebben de secretariaten en/of leidinggevenden van de thuiszorgorganisaties op de lijst telefonisch of per e-mail benaderd. De medewerkers die uiteindelijk meededen waren door hun leidinggevende gevraagd om mee te doen aan het onderzoek. Voorwaarde hierbij was dat zij op de hoogte moesten zijn van de manier waarop binnen de eigen organisatie wordt omgegaan met antibioticaresistentie. Hierna hebben wij telefonisch of per e-mail afspraken gemaakt voor de interviews waarbij tenslotte maximaal 2 medewerkers per organisatie werden geïnterviewd in 1 interview. Organisaties werden geïncludeerd totdat datasaturatie werd bereikt. Men spreekt van datasaturatie wanneer geen nieuwe informatie zich meer aandient en inclusie van meer respondenten dus niet meer leidt tot nieuwe inzichten. We hebben voor het samenstellen van onze sample rekening gehouden met grootte, ligging en specifieke kenmerken van de organisaties die geselecteerd werden (zoals een religieuze overtuiging of culturele achtergrond), om een zo groot mogelijke diversiteit en geografisch verspreiding te krijgen.
Dataverzameling
In de interviews kwamen de volgende onderwerpen aan bod:
- ervaring met antibioticaresistentie;
- omgang met antibioticaresistentie, waaronder
- betrokken personen/instanties
- protocollen
- persoonlijke beschermingsmiddelen
- mogelijke verbeterpunten
- scholing/voorlichting over antibioticaresistentie;
- contact met instanties/organisaties over antibioticaresistentie.
De interviews werden gehouden op de locaties van de thuiszorgorganisaties. De deelnemers waren vooraf geïnformeerd over het onderzoek en hadden schriftelijk toestemming gegeven om de gesprekken op te nemen en te verwerken in een rapportage. De interviews werden afgenomen door een onderzoeker en een deskundige infectiepreventie van 1 van beide GGD’en. De laatste was aanwezig om aanvullende vragen in kader van het onderzoek te kunnen stellen en eventuele inhoudelijke vragen van de deelnemers achteraf te kunnen beantwoorden. De interviews duurden 45-60 minuten.
Data-analyse
Interviews werden opgenomen en volledig uitgeschreven. Wij hebben de gegevens geanalyseerd aan de hand van een combinatie van comparative analysis en thematic analysis (9) door open codering (10) met Atlas.Ti version 7.1.5.
Om de betrouwbaarheid van de analyses te borgen hebben wij de eerste 2 interviews opgedeeld in 4 delen die werden gecodeerd door onderzoeker A en 1 van de andere onderzoekers B, C, D of E. Daarna werden de opkomende thema’s en toegewezen codes geanalyseerd binnen het onderzoeksteam totdat consensus werd bereikt. Op deze manier werden later nog 2 interviews geanalyseerd. Alle andere interviews werden alleen door onderzoeker A gecodeerd.
Resultaten
In de periode van september-december 2017 hebben wij interviews afgenomen bij 13 organisaties uit 10 verschillende gemeenten.
Onder de deelnemende thuiszorgorganisaties was er 1 organisatie met een multiculturele achtergrond, leverde er 1 zorg vanuit een bepaalde religieuze overtuiging, en leverde 1 specialistische thuiszorg. De organisaties varieerden in grootte van 12 tot 10.000 medewerkers, en sommige grote organisaties hadden ook een verpleeghuis. De karakteristieken van de organisaties en geïnterviewden zijn weergegeven in Tabel 1.
Er is geen duidelijke relatie gevonden tussen de karakteristieken van de thuiszorgorganisaties en de manieren van omgaan met antibioticaresistentie.
Tabel 1. Karakteristieken van de deelnemende organisaties
| Gegevens deelnemde organisaties | Gegevens deelnemende medewerkers | |||||
| Organisatie | Totaal aantal medewerkers | DI* werkzaam | Infectie-commissie aanwezig | Functie(s) respondent(en) | Één of beide respondenten ervaring met ABR binnen organisatie | Contact GGD ABR |
| 1 | 550 | Ja | Ja | 1.Wijkvpk** 2.Voorzitter infectiecommissie | Ja | Ja |
| 2 | ~60 | Nee | Nee | 1.Zorgcoördinator/ wijkvpk* | Ja | Ja |
| 3 | ~30 | Nee | Nee | 1.Directeur zorg/ vpk | Ja | Ja |
| 2.Teamcoach/ vpk | ||||||
| 4 | 25 | Nee | Nee | 1.Algemene directeur | Ja | Ja |
| 5 | 12 | Nee | Nee | 1.Directie manager | Ja | Ja |
| 6 | 10.000 | Nee | Nee | 1.Wijkvpk | Ja | Nee |
| 2.Wijkvpk | ||||||
| 7 | 2000 | Nee | Nee | 1.Wijkvpk | Ja | Nee |
| 2.Basis verpleegkundige | ||||||
| 8 | 1600 | Ja | Nee | 1.Wijkvpk | Ja | Nee |
| 2.Wijkvpk | ||||||
| 9 | 914 | Nee | Ja | 1.Wijkvpk | Ja | Nee |
| 10 | 873 | Nee | Nee | 1.Wijkvpk | Ja | Nee |
| 11 | 639 | Nee | Nee | 1.Wijkvpk | Ja | Nee |
| 12 | 53 | Nee | Nee | 1.Bestuurder | Ja | Nee |
| 13 | 800 | Ja | Ja | 1.Wijkvpk | Nee | Nee |
| 2.VIG’er*** | ||||||
* DI = deskundige infectieziektepreventie; **vpk = verpleegkundige; *** VIG = verzorgende individuele gezondheidszorg
Thema’s uit de interviews
Ervaring met antibioticaresistentie
Slechts 1 van de organisaties heeft nog geen ervaring met cliënten met infecties door resistente bacteriën. De meeste organisaties hebben ervaring met de zorg voor cliënten met Meticillineresistente Staphylococcus aureus (MRSA). En een aantal organisaties heeft ervaring met cliënten met een andere BRMO, zoals Vancomycineresistente enterokok (VRE) of Extended Spectrum Beta-Lactamase (ESBL). Het aantal clienten met een infectie door een resistente bacterie varieert van zeer zelden tot vaak, met een maximum van 5-6 keer per jaar.
Protocol voor antibioticaresistentie
De meeste organisaties hebben een protocol voor antibioticaresistentie. Meestal is dit het protocol van Vilans, een kenniscentrum voor langdurige zorg (11); enkele organisaties hanteren de richtlijnen van de Landelijke Coördinatie Infectieziektebestrijding (LCI) van het RIVM, de richtlijnen van het ziekenhuis of hebben ze zelf opgesteld, waarbij een aantal organisaties de WIP-richtlijnen als basis heeft gebruikt.
De meeste medewerkers gebruiken het beschikbare protocol en vinden ook dat het duidelijk is opgesteld. Een aantal gaf echter aan dat hun protocol niet specifiek voor de thuiszorg is of niet (goed) toepasbaar in de thuiszorg.
“En ik vind het soms lastig, zeg maar, wij hebben hier wel protocollen, die geven niet altijd heel erg specifiek aan – en die zijn ook vaak heel erg intramuraal geënt.”
Beschermingsmiddelen
Alle medewerkers gebruiken beschermingsmiddelen als zij naar (mogelijk) besmette cliënten gaan. Bij de meeste organisaties zijn beschermingsmiddelen altijd op voorraad. Bij een aantal organisaties moeten ze besteld worden. In de meeste organisaties is de werkgever verantwoordelijk voor de aanschaf en kosten van beschermingsmiddelen.
“Ja, ik denk dat wij als thuiszorg verantwoordelijk zijn dat er natuurlijk wel de benodigde materialen liggen, hè, zodat wij in ieder geval ons kunnen beschermen daartegen. Omdat [....] wij wel verantwoordelijk zijn ook voor andere cliënten.”
Sommige medewerkers stoppen - conform het protocol - met het gebruiken van persoonlijke beschermingsmiddelen, als de uitslag van het kweekonderzoek bij hun client een aantal keren achter elkaar negatief is. Één medewerker geeft aan soms ook op eigen initiatief te stoppen als de kweekuitslagen te lang op zich laten wachten. Hij/zij vindt het gebruik van beschermingsmiddelen in zo’n situatie nutteloos.
“En we doen het [gebruik beschermingsmiddelen] allemaal meestal braaf, tot we soms denken van ‘jeetje, we doen het nou zo lang, we krijgen van geen enkele kweek een reactie terug’.”
Zorgoverdracht
Bijna alle thuiszorgorganisaties hebben te maken met besmette clienten die na verblijf in het ziekenhuis aan hun zorg worden toevertrouwd. De meeste medewerkers vinden de communicatie met het ziekenhuis of met de huisarts rondom de zorgoverdracht slecht, omdat de besmetting of andere informatie niet (op tijd) wordt doorgegeven, waardoor beschermende maatregelen te laat worden toegepast. Slechts enkele respondenten hebben wel goede ervaringen met de zorgoverdracht.
“Dus dan heb je ze eigenlijk al heel lang onbeschermd verzorgd, en toen ineens werd bekend dat ze de VRE-bacterie hadden.”
Alle medewerkers vinden dat de zorgoverdracht verbeterd kan worden. Ze zouden graag een duidelijke zorgoverdracht krijgen, telefonisch of op papier, voordat de cliënt in zorg komt. Er wordt nu erg wisselend mee omgegaan. Het komt regelmatig voor dat de thuiszorg geen informatie over de aanwezigheid van een BRMO ontvangt of deze te laat ontvangt. Daarnaast geven een paar medewerkersaan behoefte te hebben aan een kort protocol bij de overdracht.
“Dat dat er gelijk bijstaat [....]van ‘goh mevrouw is bekend met een BRMO, hij zit daar en daar, en deze maatregelen dien je te nemen’. Dat zou het meest praktische zijn.”
Als er vragen zijn over antibioticaresistentie met betrekking tot een cliënt nemen veel medewerkers contact op met de huisarts van de betreffende client. Medewerkers geven aan wisselende ervaringen te hebben met contact met de huisarts in geval van vragen.
“Nou, ik heb heel veel problemen met de huisarts qua terugkoppeling. Er moet gewoon heel wat veranderen [....] de communicatie is gewoon dermate slecht, met de huisartsen.”
Als er vragen zijn over cliënten die vanuit een ziekenhuis zijn overgedragen nemen de meeste medewerkers contact op met het betreffende ziekenhuis. Ook hier zijn de ervaringen wisselend en meerdere medewerkers geven aan dat ze zouden willen dat het ziekenhuis beter communiceert.
“Ik heb alleen die ervaring dat ik daar zelf iedere keer achteraan moest bellen en voordat ik dan weer iemand aan de lijn had die daar dan weer iets van wist [....]”
Hoewel een aantal medewerkers wel contact heeft gehad met de GGD over antibioticaresistentie, weten de meesten niet dat ze de GGD kunnen inschakelen. Een aantal medewerkers geeft aan in de toekomst contact op te zullen nemen met de GGD als er behoefte is aan ondersteuning of informatie op dit gebied.
Er zijn ook medewerkers die hun vragen over antibioticaresistentie voorleggen aan een interne of externe deskundige infectiepreventie, een interne infectiepreventiecommissie of een ARBO-arts.
Informatiebehoefte
Een aantal medewerkers geeft aan dat ze onvoldoende weten over antibioticaresistentie. Verder geven de meesten aan dat hun collega’s hier ook vragen over hebben. Slechts 1 medewerker meldt dat zijn/haar collega’s, voorzover hij/zij weet, geen vragen hebben over antibioticaresistentie.
“Ik denk wel dat het belangrijk is dat mensen meer informatie krijgen over die resistentie, van hoe zit het nou, hoe kan het gebeuren en waardoor gebeurt het.”
Binnen een aantal organisaties is wel scholing over MRSA georganiseerd. Daar was positief op gereageerd. Andere medewerkers geven aan dat zij behoefte hebben aan informatie in de vorm van scholing. Er zijn ook medewerkers die informatie over antibioticaresistentie willen krijgen, maar alleen op het moment dat het speelt, en het hoeft niet in de vorm van een scholing.
Discussie
Met dit onderzoek hebben wij in kaart gebracht hoe thuiszorgorganisaties omgaan met antibioticaresistentie en welke problemen zij ervaren met betrekking tot protocollen, beschermingsmiddelen en de communicatie met andere zorgprofessionals. Uit het onderzoek blijkt dat veel thuiszorgmedewerkers behoefte hebben aan meer informatie over antibioticaresistentie, duidelijke protocollen specifiek voor de thuiszorg, betere communicatie met de huisarts en het ziekenhuis en een betere zorgoverdracht van cliënten met een infectie veroorzaakt door een resistente bacterie.
Voor zover bekend is dit onderzoek onder thuiszorgorganisaties niet eerder uitgevoerd. Er werd datasaturatie bereikt na gesproken te hebben met 13 organisaties, die heel verschillend waren, waardoor we een diversiteit aan ideëen en denkbeelden naar boven konden halen. Het bleek dat veel organisaties, ongeacht grootte, specifieke achtergrond en geografische ligging, tegen dezelfde problemen aanliepen. Een ander sterk punt is dat sommige interviews werden afgenomen bij 2 medewerkers met verschillende functies uit 1 organisatie, die allebei vanuit hun eigen functie kennis hadden over het omgaan met antibioticaresistentie binnen hun organisatie.
We hebben ongeveer 60 thuiszorgorganisaties moeten benaderen voordat we voldoende deelnemers hadden geïncludeerd om datasaturatie te bereiken. Veel organisaties gaven aan dat zij met name door tijdgebrek niet mee konden doen. Dit zou wellicht een indicatie kunnen zijn dat thuiszorgorganisaties antibioticaresistentie nog niet hoog op hun prioriteitenlijst hebben staan.
Protocollen
Uit ons onderzoek blijkt dat de medewerkers van de meeste aan het onderzoek deelnemende thuiszorgorganisaties een protocol voor antibioticaresistentie kunnen vinden wanneer dit nodig is en dat zij maatregelen treffen in geval van besmette cliënten. Dit komt overeen met resultaten van een eerder onderzoek (12) onder medewerkers van Nederlandse ziekenhuizen die, wanneer het nodig is, ook het MRSA-protocol kunnen vinden en maatregelen nemen bij patiënten met MRSA.
Thuiszorgmedewerkers hebben echter wel problemen met het uitvoeren van de protocollen. Ze zijn lang/uitgebreid - de benodigde beschermingsmiddelen zijn wel snel beschikbaar - maar vooral ze zijn niet specifiek geschikt voor de thuiszorg. Ook is het niet duidelijk waarom er in een ziekenhuis andere maatregelen nodig zijn voor dezelfde patiënt dan in de thuiszorgsituatie.
Uit het eerder genoemde onderzoek in de ziekenhuizen bleek dat ziekenhuismedewerkers ook problemen ondervinden met de lengte van de protocollen en dat er sprake is van onwil in gebruik van beschermingsmiddelen, bijvoorbeeld wanneer deze de uitvoering van het werk hinderen, en dat er problemen zijn met toepasbaarheid van protocol door problemen met de infrastructuur en geld- of personeeltekort. (12)
Zorgoverdracht
De overdracht van besmette cliënten vanuit verschillende zorginstellingen naar thuiszorgorganisaties verloopt niet altijd optimaal. Uit eerder onderzoek is gebleken dat de regelmatige patiëntenstroom tussen verschillende Nederlandse zorginstellingen bijdraagt aan de verspreiding van resistente microrganismen. (13) Uit een onderzoek in Californië (USA) blijkt zelfs dat het verplaatsen van patiënten van ziekenhuizen naar verpleeghuizen en terug, kan leiden tot meer verspreiding van MRSA, zelfs wanneer een patiënt tussendoor nog een periode thuis is en eventueel thuiszorg krijgt. (14) Om het probleem van antibioticaresistentie aan te pakken is het daarom van belang dat verschillende partijen samen de verspreiding van resistente micro-organismen tegengaan door allen de benodigde maatregelen te treffen. (13)
Informatiebehoefte
Thuiszorgmedewerkers hebben veel vragen over antibioticaresistentie en willen graag meer informatie over het onderwerp ontvangen. De meeste thuiszorgmedewerkers hebben nooit scholing over antibioticaresistentie gehad. Uit het onderzoek onder ziekenhuismedewerkers blijkt dat zij hierover vaak wel een scholing hebben gehad. (12) Ziekenhuismedewerkers waren dan ook veel positiever over hun kennis, houding en gedrag met betrekking tot antibioticaresistentie, dan de medewerkers in ons onderzoek.
Aanbevelingen
- Het is zinvol om aanvullend kwantitatief onderzoek te doen om de omvang van het probleem en de behoeftes van thuiszorgorganisaties in de GGD regio’s Gelderland-Zuid en Gelderland-Midden nog beter in kaart te brengen.
- Uit dit onderzoek blijkt dat thuiszorgorganisaties problemen ervaren met de communicatie met en de zorgoverdracht vanuit huisartsen en het ziekenhuis. Om te bepalen of huisartsen en ziekenhuizen ook deze problemen ervaren, is aanvullend onderzoek nodig vanuit het perspectief van de huisarts en het ziekenhuis. De Zorgnetwerken Antibioticaresistentie zijn in diverse regio’s bezig met projecten om de zorgoverdracht te verbeteren. Het is belangrijk dat ook de thuiszorg hierin wordt meegnomen.
- Omdat de protocollen over antibioticaresistentie die in de thuiszorg gebruikt worden niet specifiek voor de thuiszorg zijn, is het belangrijk dat er landelijke protocollen specifiek voor de thuiszorg worden ontwikkeld.
- Thuiszorgmedewerkers hebben behoefte aan meer kennis over antibioticaresistentie. Ook hierbij kunnen de regionale zorgnetwerken, waarin multidisciplinair wordt samengewerkt, een rol spelen. Aangezien de GGD een belangrijke rol heeft in het bieden van informatie en ondersteuning over antibioticaresistentie buiten zorginstellingen, ligt het voor de hand dat de GGD hierbij het voortouw neemt. Het Gelders Antibioticaresistentie en Infectiepreventie Netwerk (GAIN) en het Zorgnetwerk Antibioticaresistentie voor Zuidwest-Nederland (ZWN) hebben inmiddels hun krachten gebundeld en gaan eind 2018 een scholingsprogramma ontwikkelen voor beide regio’s dat later ook beschikbaar zal worden gemaakt voor andere zorgregio’s. Naast scholing zal netwerkvorming en het op de managementagenda plaatsen van antibioticaresistentie en infectiepreventie, onderdeel uitmaken van dit programma.
Auteurs
D.J.J. van Nimwegen1, M.J.W. van Mourik1, M. Terwee2, H. Beks2, C.H.M. van Jaarsveld3, J.L.A. Hautvast1,3, S.G. Feenstra1
- GGD Gelderland-Zuid, Nijmegen,
- GGD Gelderland-Midden, Arnhem,
- Academische werkplaats AMPHI, Afdeling Eerstelijnsgeneeskunde, Radboudumc, Nijmegen
Correspondentie
sfeenstra@ggdgelderlandzuid.nl,
Literatuur
- WHO. Global action plan on antimicrobial resistance. 2015 [Beschikbaar via: http://apps.who.int/iris/bitstream/10665/193736/1/9789241509763_eng.pdf?... Geraadpleegd 1 augustus 2018.
- de Greeff SC, Mouton JW. NethMap 2017: Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands/MARAN 2017: Monitoring of antimicrobial resistance and antibiotic usage in animals in the Netherlands in 2016. RIVM; 2017. Contract No.: 2017-0056.
- Schippers EI. Kamerbrief over voortgang aanpak antibioticaresistentie. Den Haag: Ministerie van Volksgezondheid, Welzijn en Sport; 2016. Contract No.: 988034-152874-PG.
- GGD Nederland. Rol van de GGD bij ABR. 2015.
- Kusters T, Raven S, Jansen L, Nadi S, Hautvast J, Tostmann A. BRMO-casuïstiek in 2015: omvang en werkinzet bij 8 GGD'en. Infectieziekten Bulletin. 2017;28(9):347-52.
- van Leeuwen SM. Grenzeloos samenwerken, daar wordt iedereen beter van. Deventer: Hogeschool Saxion; 2015. Moons C. Andere BRMO-maatregelen in de thuiszorg? 2016 [Beschikbaar via: http://www.zorgvoorbeter.nl/ouderenzorg/BRMO-thuiszorg.html] Geraadpleegd 1 augustus 2018.
- Zorg voor Beter. Richtlijnen infectiepreventie voor thuiszorg ontbreken. 2016 [Beschikbaar via: https://www.zorgvoorbeter.nl/nieuws/richtlijnen-infectiepreventie-thuisz... Geraadpleegd 28 september 2018.
- Dawson C. Introduction to research methods. 4th ed. Oxford, United Kingdom: How to books Ltd; 2009.
- Boeije H. Analysis in qualitative research. 1st ed. London, United Kingdom: Sage publications Ltd; 2010.
- Vilans. KICK-protocollen. 2018 [Beschikbaar via: https://www.vilans.nl/themas/kick-protocollen] Geraadpleegd 1 augustus 2018.
- van Gemert-Pijnen J, Hendrix MG, van der Palen J, Schellens PJ. Performance of methicillin-resistant Staphylococcus aureus protocols in Dutch hospitals. American journal of infection control. 2005;33(7):377-84.
- Donker T, Ciccolini M, Wallinga J, Kluytmans JA, Grundmann H, Friedrich AW. Analyse van patiëntstromen: de basis voor regionale bestrijding van gevaarlijke infecties. Nederlands tijdschrift voor geneeskunde. 2015;159:A8468.
- Lee BY, Bartsch SM, Wong KF, Singh A, Avery TR, Kim DS, et al. The importance of nursing homes in the spread of methicillin-resistant Staphylococcus aureus (MRSA) among hospitals. Medical care. 2013;51(3):205-15.
Infectieziekten Bulletin, jaargang 29, nummer 11, december 2018
OneHealth Hub
In het kader van het One Health eZoonproject heeft het Centre for eHealth & Wellbeing Research van de Universiteit Twente de OneHealth Hub ontwikkeld. Dit is een platform dat samenwerking stimuleert tussen professionals uit de humane en veterinaire gezondheidzorg ter voorkoming en bestrijding van zoönosen.
OneHealth Hub
Waarom een OneHealth Hub?
Verschillende professionals van de NVWA, GGD, UMC en KNMvD werden geïnterviewd om de behoefte aan een OneHealth Hub na te gaan. Tijdens deze interviews bleek dat er behoefte is aan een OneHealth Hub waarin samenwerking en communicatie tussen de betrokken sectoren wordt gefaciliteerd (bijvoorbeeld door weergave van contactgegevens van betrokkenen). De OneHealth Hub richt zich nu op interactie.
De geïnterviewden waren ook op zoek naar een manier om adequate en accurate informatie over zoönosen op te kunnen vragen. Uit de interviews met professionals werkzaam in de publieke gezondheid blijkt dat zij bijvoorbeeld graag gebruik zouden willen maken van een website zoals MRSA-net, die ook toepasbaar is voor professionals werkzaam buiten het ziekenhuis:
"Wij willen MRSA-net heel graag gebruiken, een platform waarop alles te vinden is over zoönosen zou door ons zeker gebruikt worden, alleen nu is die puur gericht op het ziekenhuis en niet op de publieke gezondheid. Wij kunnen het niet gebruiken zoals die nu is." professional publieke gezondheidzorg
OneHealth Hub
Vanuit bovenstaande behoeftes is de interactieve OneHealth Hub ontwikkeld. Het verschil met bestaande OneHealth-platforms is de combinatie van informatie-, educatie- en communicatievoorziening voor de 2 sectoren en een afzonderlijke informatievoorziening voor het algemeen publiek. We willen ook het OneHealth-netwerk versterken, door van de OneHealth Hub een letterlijke informatie- en datahub te maken, waardoor professionals uit verschillende sectoren elkaar kunnen vinden.
Platform
De OneHealth Hub is een online platform gericht op risicopreventie voor besmettingen en voor de training van management bij zoönoseuitbraken. Het bestaat uit een Vraag&Antwoord (Q&A)-systeem (voor algemeen publiek en professionals) met vragen over risico’s en het voorkomen ervan. Daarnaast biedt de hub een serious game die professionals traint voor een gezamenlijke aanpak van zoönosen.
Doelgroepen
De doelgroepen van de Hub zijn:
- professionals werkzaam in de humane gezondheidszorg (curatieve en publieke gezondheidszorg),
- professionals werkzaam in de veterinaire gezondheidszorg,
- algemene publiek.
OneHealth Q&A-systeem voor publiek en professionals
Twee jaar geleden beschreven we in het Infectieziekten Bulletin in het artikel De mythes en missers over MRSA de start van het eZoon-project dat als doel heeft om de publieke communicatie en informatievoorziening over zoönosen te verbeteren en de samenwerking te versterken tussen humane en veterinaire gezondheidszorg (One Health). Binnen het project was gestart met de actualisatie en uitbreiding van MRSA-net. (1) MRSA-net is een online-informatieplatform over MRSA voor (zorg-)professionals en het algemeen publiek in de vorm van een Q&A systeem. Het MRSA-net wordt veel gebruikt (in het afgelopen jaar circa 2 miljoen pageviews en meer dan 500.000 sessies) en gebruikers beoordelen het systeem als goed.
MRSA-net heeft als voorbeeld gediend voor de OneHealth Hub. De Hub Q&A’s leveren al informatie over MRSA in de samenleving en in ziekenhuizen. Na een doorontwikkeling van de Hub, wordt deze uitgebreid met informatie over meerdere zoönosen. Het systeem is in staat om op basis van een gestelde vraag snel relevante antwoorden te tonen, dankzij het gebruik van een chatbotzoekfunctie (een digitale assistent die de meeste vragen kan beantwoorden). De inhoud van de Hub is nu gebaseerd op protocollen en behoeftes van eindgebruikers.
Informatiestructuur
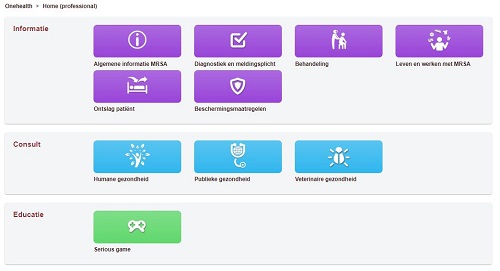
De informatiestructuur voor de OneHealth Hub is bepaald met behulp van een online card sort-studie onder het algemeen publiek (n=23) en professionals (n=18). Met een online card sort kun je de structuur van een website bepalen en afstemmen op de eindgebruikers. (2) Behalve de structuur zijn verschillende OneHealth gerelateerde onderwerpen geïdentificeerd voor beide groepen. Met de resultaten ontwikkelden we een digitaal prototype van de Hub (Figuur 1).
Figuur 1. Een weergave van het platform prototype.
Het digitale prototype hebben we getest met professionals, het algemene publiek en met experts. De resultaten verwerken we in het eerste werkende prototype van de OneHealth Hub.
Game-based elearning
In het 2 jaar geleden geschreven artikel in het Infectieziekten Bulletin Van ‘vreemde vogels’ en vogelgriep bespraken we de ontwikkeling en het doel van een serious game. (3) Met een serious game kun je vaardigheden voor risico- en crisiscommunicatie en interdisciplinaire samenwerking rondom een zoönose-uitbraak trainen (casus: vogelgriep). De verhaallijn van de game is inmiddels gevalideerd door professionals uit het veld, werkzaam bij de NVWA en de GGD. Experts en eindgebruikers evalueerden een tweede versie van de game op design en vormgeving. (4) De deelnemers waren zeer positief over de game. Ze gaven onder andere relevante suggesties ten aanzien van het design. Maar ze gaven bijvoorbeeld ook aan feedback te willen ontvangen die is afgestemd op hun daadwerkelijk speelgedrag. De game zal als educatievoorziening voor professionals geïntegreerd worden in de OneHealth Hub.
Implementatie
Het implementatietraject van de OneHealth Hub geven we momenteel vorm. Hierbij komen factoren aan de orde als verantwoordelijkheid, eigenaarschap, inbedding landelijk/regionaal, trainingsmodel en een verdienmodel voor duurzame implementatie, dit wordt gedaan door middel van scenario-based interviews met stakeholders.(5)
Conclusie
De OneHealth Hub is ontworpen vanuit een interactieve en participerende ontwerpaanpak. (6) We hebben relevante stakeholders betrokken uit de humane gezondheidszorg (inclusief de publieke gezondheidszorg) en de veterinaire gezondheidszorg. (5)
De inhoud van de OneHealth Hub is gebaseerd op protocollen, informatiebehoeften en op risicopreventies, gemeten onder de bevolking en professionals. De inhoud is vertaald in een menu-structuur via card sort. Verder zijn de functionaliteiten gedefinieerd op basis van gebruikerstesten met eindgebruikers. Daarnaast zijn scenario’s voor implementatie opgesteld op basis van interviews met stakeholders.
Het is belangrijk om de communicatie, educatie en informatie over zoönosen vanuit OneHealth perspectief te verhelderen en beter te structureren. Hier is een duidelijke behoefte aan en we willen dat op een centraal punt gaan aanbieden. Doel is dat relevante stakeholders beter samenwerken en communiceren met elkaar en dat de informatievoorziening voor professionals en algemeen publiek adequaat en accuraat is.
In het themanummer Antibioticaresistentie van Infectieziekten Bulletin (Jaargang 18, nr. 9) is het eZoon-project geïntroduceerd vanuit het Centre for eHealth and Wellbeing Research van de Universiteit Twente. Dit project is gefinancierd door ZonMw en wordt vanuit onderzoekservaring met risicocommunicatie en eHealth-implementatie uitgevoerd door de Universiteit Twente. In dit project wordt vanuit het OneHealth-perspectief gewerkt aan het ontwikkelen van een eHealth-applicatie: de OneHealth Hub
Auteurs
M.F. ter Horst, N. Köhle, L.M.A. Braakman-Jansen, N. Beerlage-de Jong, A. Snoep, J.E.W.C. Van Gemert Pijnen, Centre for eHealth, Wellbeing and Research, afdeling Psychologie, Gezondheid en Technologie, Universiteit Twente
Correspondentie
m.f.terhorst@utwente.nl
Literatuur
- Jong NB, Siemons L, Köhle N. De mythes en missers over MRSA. Infect Bull. 2017;28(9):359–61.
- Wentzel J, Müller F, Beerlage-de Jong N, van Gemert-Pijnen J. Card sorting to evaluate the robustness of the information architecture of a protocol website. Int J Med Inform. Elsevier Ireland Ltd; 2016;86:71–81.
- Jong NB, Köhle N, Siemons L. Van ‘ vreemde vogels ’ en vogelgriep. Infect Bull. 2017;28(9):362–5.
- Kiili K. Digital game-based learning: Towards an experiential gaming model. Internet High Educ. 2005;8(1):13–24.
- van Woezik AF, Braakman-Jansen LM, Kulyk O, Siemons L, van Gemert-Pijnen JE. Tackling wicked problems in infection prevention and control: a guideline for co-creation with stakeholders. Antimicrob Resist Infect Control. 2016;5(1).
- van Gemert-Pijnen JEWC, Nijland N, van Limburg M, Ossebaard HC, Kelders SM, Eysenbach G, et al. A holistic framework to improve the uptake and impact of eHealth technologies. J Med Internet Res. 2011;13(4).
Infectieziekten Bulletin, jaargang 29, nummer 11, december 2018
Surveillance van Listeria in Nederland in 2017
De surveillance van listeriose in Nederland is gestart in 2005 met een laboratoriumsurveillance. Sinds december 2008 is de ziekte meldingsplichtig. In 2017 werden 115 patiënten met listeriose geregistreerd, waaronder 3 zwangere vrouwen (3%). Tien volwassenen zijn overleden (9%).
Surveillance van Listeria in Nederland in 2017
Listeria monocytogenes is een bacterie die overal in het milieu voorkomt en daarbij ook onder ongunstige omstandigheden, zoals droogte en lage temperaturen, kan overleven en zelfs kan groeien. Infectie bij de mens gebeurt voornamelijk via voedsel dat besmet wordt vanuit de productieomgeving. Het aantal mensen dat (ernstig) ziek wordt van Listeria is niet heel groot, maar de ziektelast is hoog door de ernst van de ziekte. (1, 2) In Nederland bestaat er sinds 2005 een laboratoriumsurveillance voor L. monocytogenes en een meldingsplicht sinds 2008. Daarnaast worden door de Nederlandse Voedsel en Waren Autoriteit (NVWA) jaarlijks diverse soorten risicovolle voedingsmiddelen op L. monocytogenes onderzocht. In deze rapportage presenteren we de resultaten van 2017 van beide surveillances en vergelijken die met elkaar en ten opzichte van voorgaande jaren.
Methode
Volgens de Wet Publieke Gezondheid (Wpg) (2008) is listeriose meldingsplichtig wanneer L. monocytogenes is geïsoleerd uit feces, bloed of liquor of (in geval van een zwangerschap) uit materiaal van een foetus, doodgeboren kind, pasgeboren kind of de moeder. Medisch microbiologische laboratoria dienen elke positieve kweek van L. monocytogenes te melden aan de GGD. De GGD neemt vervolgens contact op met de patiënt of naasten van de patiënt en neemt een korte vragenlijst af over medische achtergrond, klinisch beloop en blootstelling aan mogelijke risicofactoren in de 30 dagen voor het begin van de klachten. Deze gegevens worden via de webapplicatie Osiris geregistreerd bij het RIVM.
Daarnaast wordt de laboratoria gevraagd Listeria-isolaten van patiënten met meningitis of sepsis naar het Nederlands Referentielaboratorium voor Bacteriële Meningitis (NRBM) te sturen waar de isolaten getypeerd worden met serotypering. Er zijn meer dan 14 verschillende serotypes bekend voor L. monocytogenes. Slechts 4 serotypes, namelijk 1/2a, 1/2b, 1/2c en 4b, zijn verantwoordelijk voor >95% van alle humane infecties.
Het NRBM stuurt vervolgens de stammen door naar het RIVM die de isolaten typeert met whole-genome sequencing (WGS). De WGS-data worden gebruikt voor clusterdetectie (2 of meer (vrijwel) identieke stammen uit verschillende bronnen/patiënten) met core-genome multi-locus sequence typing (cgMLST). Bij een cluster is er alleen sprake van (vrijwel) identieke stammen. Als er daarnaast aanwijzingen zijn dat er een epidemiologische link is tussen patiënten, al dan niet met een link naar een voedselproduct, wordt gesproken van een uitbraak. De cgMLST-clusterdetectie vervangt de PFGE-analyse die tot 2017 werd gedaan.
De NVWA onderzoekt jaarlijks diverse soorten risicovolle voedingsmiddelen op aanwezigheid van L. monocytogenes in het kader van haar toezichtstaak. Hieronder valt ook het brononderzoek naar aanleiding van meldingen van voedselinfecties. Het surveillanceonderzoek van L. monocytogenes door de NVWA richt zich vooral op kant-en-klare levensmiddelen. Volgens Verordening (EG) nr. 2073/2005 mogen er in kant-en-klare levensmiddelen die in de handel zijn gebracht niet meer dan 100 kolonievormende eenheden (kve) L. monocytogenes per gram voorkomen gedurende de houdbaarheidstermijn. Kant-en-klare zuigelingenvoeding en kant-en-klare voeding voor medisch gebruik, zoals drinkvoeding, mogen in het geheel geen L. monocytogenes bevatten (afwezigheid in 25 g). De door de NVWA onderzochte monsters zijn kwalitatief (detectie in 25 g) en/of kwantitatief (telling met detectielimiet 10 kve/g) onderzocht op aanwezigheid van L. monocytogenes (ISO 11290-1 en -2). Bij een geconstateerde afwijking van de norm zal de NVWA de verkoper en/of de producent op de hoogte brengen opdat deze een interventie kan plegen. Tevens voert de NVWA in het kader van haar bronopsporingstaak nader typeringsonderzoek uit op de door haar verkregen voedselisolaten. De door de NVWA verkregen voedselisolaten zijn getypeerd met behulp van moleculaire ‘serotypering’, op basis van WGS-data (genoserotypering). Het verschil tussen klassieke serotypering (door het NRBM) en genoserotypering (door de NVWA) is dat genoserotypering alleen discrimineert tussen 5 gedefinieerde genoserogroepen; IIa (=1/2a en 3a), IIb (=1/2b, 3b en 7), IIc (=1/2c en 3c), IVa (=4a en 4c) en IVb (=4b, 4d en 4e). (3, 4) Ondanks dit minder discriminerend vermogen van de genoserotypering geeft deze methode toch een voldoende karakterisering. Dit komt doordat de meest voorkomende serotypes 1/2a, 1/2b, 1/2c en 4b elk in een andere genoserogroep vallen en dus van elkaar te onderscheiden zijn.
Resultaten
Aantal gerapporteerde ziektegevallen en klinisch beeld
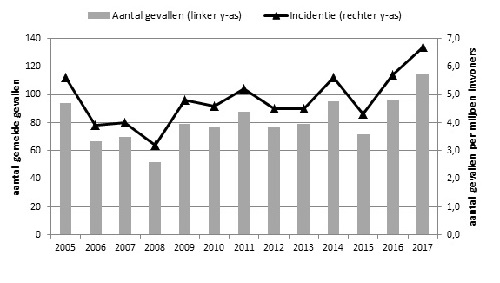
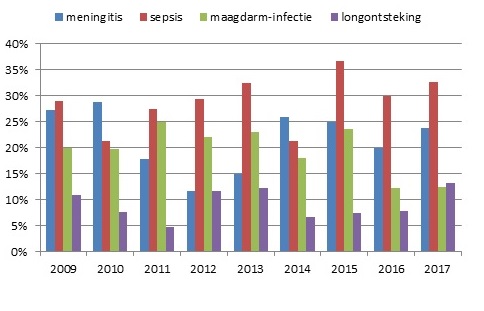
In 2017 werden 115 patiënten gerapporteerd met een infectie met L. monocytogenes. Dit komt overeen met een incidentie van 6,7 patiënten per miljoen inwoners (Figuur 1). Elf patiënten vormden samen met 1 patiënt uit 2016 en 1 uit 2018 het eerste landelijke uitbraakcluster sinds de start van de surveillance in 2005. Via Osiris werden 113 patiënten gemeld (van 101 werd ook een isolaat naar het NRBM en/of RIVM gestuurd) en van 2 patiënten was alleen een isolaat ingestuurd. De mediane leeftijd van alle patiënten was 74 jaar (range 19-94 jaar) en 60% van de patiënten was man. De meest voorkomende ziektebeelden waren sepsis, meningitis, longontsteking en maagdarminfectie (Figuur 2). Sepsis werd het meest gemeld (37 patiënten), gevolgd door meningitis (27 patiënten). De zeldzamere ziektebeelden encefalitis en endocarditis werden respectievelijk bij 4 en 3 patiënten gediagnosticeerd. Van 113 patiënten van wie het beloop van de infectie bekend was, zijn er 10 overleden (9%) met een mediane leeftijd van 81 jaar (range 70-93 jaar). Drie patiënten (3%) waren zwanger toen zij listeriose hadden, waarbij 2 kindjes doodgeboren werden, en 1 kindje voor zover bekend geen symptomen had.
Figuur 1. Aantal patiënten met een L. monocytogenes infectie met bijbehorende incidentie, 2005-2017
Figuur 2. Verdeling van 4 belangrijkste ziektebeelden van listeriose, 2009-2017
Gegevens over risicofactoren
Mensen met onderliggend lijden en/of medicijngebruik hebben een verhoogd risico op listeriose. Twee vrouwen en 5 mannen in de leeftijd 63-88 jaar hadden geen onderliggend lijden en gebruikten geen maagzuurremmers of immunosuppressiva. Maagzuurremmers werden door 57% van de listeriosepatiënten gebruikt en bijna de helft (46%) slikte immunosuppressiva (Tabel 1); een kwart van de patiënten slikte beide. De 3 meest genoemde onderliggende ziekten in 2017 waren kanker, hart- en vaatziekten en longziekten. Vooral het aantal patiënten met een longziekte (18%) valt daarbij op; in voorgaande jaren had maximaal 10% van de patiënten een longziekte. Patiënten met een longziekte werden daarbij 2 keer vaker met een listerioselongontsteking gemeld dan de overige patiënten. Hetzelfde werd ook gezien voor maagdarminfectie bij patiënten met een maagdarmaandoening. In tabel 2 staan de meest geconsumeerde risicoproducten. Twee producten vallen voornamelijk op: 60% van de patiënten heeft worst/worstjes gegeten, terwijl dit in de voorgaande jaren onder de helft (39-48%) bleef. Ook haring is in 2017 meer gegeten met 43% ten opzichte van 27-36% in voorgaande jaren. Binnen het landelijke cluster werd een sterke associatie met haring gezien (8/13; 62%), ten opzichte van 40% van de patiënten in 2017 buiten het cluster.
Tabel 1. Osirisgegevens over onderliggend lijden en medicijngebruik bij patiënten met een L. monocytogenesinfectie, 2013-2017
Onderliggende condities en medicijngebruik | 2017 n / N (%) | 2016 n / N (%) | 2015 n / N (%) | 2014 n / N (%) | 2013 n / N (%) |
Diabetes | 17 / 111 (15) | 18 / 88 (20) | 14 / 68 (21) | 13 / 88 (15) | 17 / 71 (24) |
Leverziekte | 9 / 111 (8) | 10 / 88 (11) | 3 / 68 (4) | 3 / 88 (3) | 4 / 71 (6) |
Nierziekte | 14 / 111 (13) | 11 / 88 (13) | 10 / 68 (15) | 11 / 88 (13) | 13 / 71 (18) |
Hart- en vaatziekten | 30 / 111 (27) | 21 / 88 (24) | 16 / 68 (24) | 17 / 88 (19) | 16 / 71 (23) |
Kanker | 39 / 111 (35) | 26 / 88 (30) | 20 / 68 (29) | 30 / 88 (34) | 20 / 71 (28) |
Immuunstoornis | 3 / 111 (3) | 7 / 88 (8) | 5 / 68 (7) | 11 / 88 (13) | 3 / 71 (4) |
Longziekte | 20 / 111 (18) | 4 / 88 (5) | 3 / 68 (4) | 9 / 88 (10) | 5 / 71 (7) |
Maagdarmziekte | 10 / 111 (9) | 5 / 88 (6) | 5 / 68 (7) | 7 / 88 (8) | 5 / 71 (7) |
Transplantatie-orgaan | 4 / 111 (4) | 3 / 88 (3) | 2 / 68 (3) | 4 / 88 (5) | 4 / 71 (6) |
Reuma | 7 / 111 (6) | 6 / 88 (7) | 6 / 68 (9) | 13 / 88 (15) | 6 / 71 (8) |
Alcoholmisbruik | 3 / 111 (3) | 7 / 88 (8) | 4 / 68 (6) | 3 / 88 (3) | 2 / 71 (3) |
Andere ziekte | 14 / 111 (13) | 10 / 88 (11) | 7 / 68 (10) | 7 / 88 (8) | 12 / 71 (17) |
Medicijngebruik: Immunosuppressiva Maagzuurremmers |
46 / 99 (46) 50 / 87 (57) |
39 / 82 (48) 42 / 71 (59) |
26 / 58 (45) 34 / 47 (72) |
50 / 84 (60) 38 / 67 (57) |
35 / 62 (56) 24 / 55 (44) |
Geen onderliggend condities | 7 / 111 (6) | 3 / 88 (3) | 4 / 67 (6) | 6 / 88 (7) | 1 / 72 (1) |
Tabel 2. Osirisgegevens over activiteiten en voedselconsumptie* in de 30 dagen vóór de klachten bij patiënten met een L. monocytogenesinfectie, 2013-2017
Risicofactoren | 2017 n / N (%) | 2016 n / N (%) | 2015 n / N (%) | 2014 n / N (%) | 2013 n / N (%) | |
Activiteiten | ||||||
Reis buitenland | 5 / 109 (5) | 1 / 85 (1) | 2 / 66 (3) | 3 / 85 (4) | 2 / 68 (3) | |
Voedselconsumptie | ||||||
Worst/worstjes | 54 / 90 (60) | 24 / 62 (39) | 19 / 41 (46) | 32 / 67 (48) | 20 / 48 (42) | |
Rosbief | 18 / 90 (20) | 22 / 62 (35) | 7 / 41 (17) | 13 / 67 (19) | 9 / 48 (19) | |
Rauwe ham | 19 / 90 (21) | 12 / 62 (19) | 8 / 41 (20) | 9 / 67 (13) | 7 / 48 (15) | |
Gekookte/gerookte ham | 38 / 90 (42) | 26 / 62 (42) | 19 / 41 (46) | 32 / 67 (48) | 20 / 48 (42) | |
Kip/kalkoen vleeswaren | 34 / 90 (38) | 23 / 62 (37) | 16 / 41 (39) | 31 / 67 (46) | 18 / 48 (38) | |
Gerookte zalm | 30 / 92 (33) | 23 / 62 (37) | 11 / 44 (25) | 12 / 69 (17) | 16 / 51 (31) | |
Gerookte makreel | 24 / 92 (26) | 12 / 62 (19) | 6 / 44 (14) | 13 / 69 (19) | 12 / 51 (24) | |
Haring | 40 / 92 (43) | 17 / 62 (27) | 16 / 44 (36) | 19 / 69 (28) | 16 / 51 (31) | |
Kibbeling/lekkerbek | 24 / 92 (26) | 16 / 62 (26) | 13 / 44 (30) | 17 / 69 (25) | 14 / 51 (28) | |
Totaal zachte kazen | 35 / 93 (38) | 34 / 63 (54) | 17 / 46 (37) | 31 / 72 (43) | 28 / 54 (52) | |
* Consumptie van voedsel alleen weergegeven indien door tenminste 20% van de patiënten in 2016 genoemd
Onderzoek levensmiddelen
In 2017 onderzocht de NVWA circa 4900 (partijen van) levensmiddelen op aanwezigheid (kwalitatief en/of kwantitatief) van L. monocytogenes. Hieruit zijn 227 isolaten verkregen. 95% van de isolaten is verkregen uit de kwalitatieve methode, waarbij het besmettingsniveau onder de 100 kve/gram ligt. De isolaten zijn verkregen uit: 38 visproducten (15 zalm, 12 haring), 55 vers pluimveevlees (47 kip, 8 kalkoen), 74 bereid pluimveevlees (71 kip, 3 kalkoen), 28 rundvlees, 15 vleesproducten rauw te consumeren (9 filet américain), 9 lamsvlees, 5 varkensvlees en elk 1 in partij tahin, tapas, en 1 maaltijdsalade.
Serotypering van patiënt- en voedselisolaten
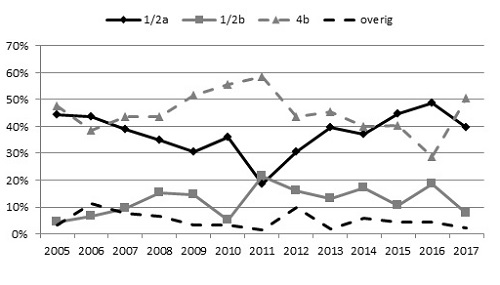
Van 102 patiënten was een isolaat beschikbaar voor serotypering en/of sequencing en van 1 patiënt ontvingen we de sequencegegevens van een regionaal laboratorium. De meeste isolaten waren afkomstig uit bloed (72%), liquor (9%) en bloed en liquor (11%). De 9 overige isolaten waren afkomstig uit ascites (2), pleuravocht (2), weefsel/vocht knie (2), galvocht (1), en overig niet gespecificeerd (2). Van 93 patiënten is het isolaat door het NRBM geserotypeerd. L. monocytogenes serotype 4b werd bij 51% van de patiënten geïsoleerd en is daarmee, evenals in de periode 2007-2014, het meest gevonden serotype, gevolgd door 1/2a (40%) en 1/2b (8%) (Figuur 3). Serotype 1/2c werd 1 keer aangetoond en ten slotte eenmaal 1/2.
Op basis van genoserotypering konden de isolaten uit voedsel worden ingedeeld in verschillende groepen. Van de isolaten waar een genoserotype van bepaald kon worden waren 129 stammen genoserogroep IIa (60%), 58 stammen genoserogroep IIc (27%), 11 stammen genoserogroep IIb (5%) en 16 stammen genoserogroep IVb (7%). Voor 13 isolaten kon het genoserotype niet bepaald worden. Alle geïdentificeerde genoserotypes kwamen in de verschillende geteste voedsel categorieën voor.
Figuur 3. Serotypering van de humane isolaten, 2005-2017
Clusteranalyse
In 2017 werden voor het eerst standaard WGS-data gebruikt voor clusterdetectie. Van de isolaten van 97 patiënten waren WGS-data beschikbaar. Voor het eerder genoemde cluster met 11 patiënten in 2017 en elk 1 patiënt in 2016 en 2018 lagen de eerste ziektedagen tussen 9 december 2016 en 7 januari 2018. De patiënten waren in de leeftijd 51-89 jaar (mediaan 78 jaar) en 62% was man. Analyse van de voedselconsumptie opgegeven in Osiris leidde naar haring (8/13; 62%) als meest waarschijnlijke bron. De NVWA heeft aan de hand van detailgegevens van de aankoopplekken van de haring een trace-back uitgevoerd, wat niet naar een gezamenlijke leverancier of locatie heeft geleid.
Er werden nog 11 andere, kleinere patiëntclusters geïdentificeerd met in totaal 30 patiënten (6 clusters van 2 patiënten, 4 clusters van 3 en een cluster van 6 patiënten). Echter, deze clusters waren dermate klein dat op basis van de beschikbare gegevens geen gezamenlijke bron aangewezen kan worden en verder onderzoek weinig zou toevoegen.
Geen van de in 2017 gevonden patiëntclusters clusterde op basis van WGS met voedselisolaten. Alleen 4 ongelinkte patiëntisolaten clusterden ieder met een voedselisolaat uit 2016 (1), 2017 (2) of 2018 (1). In 3 van de 4 clusters werd het voedselisolaat enkele maanden tot 1 jaar eerder gevonden dan de patiënt, in het vierde geval werd het voedselisolaat ongeveer 1 maand later gedetecteerd.
Discussie
Het tweede jaar op rij is het aantal listeriosemeldingen toegenomen en lag in 2017 voor het eerst boven de 100 met 115 patiënten (incidentie 6,7 patiënten per miljoen inwoners). Sinds de invoering van de meldingsplicht eind 2008 lag de incidentie van gerapporteerde listeriose tussen 4,3 en 5,7 patiënten per miljoen inwoners. In de Europese Unie (EU) lag de gemiddelde incidentie in 2017 op 4,8 patiënten per miljoen inwoners, met 8,0 en 8,8 patiënten per miljoen inwoners in respectievelijk België en Duitsland (3). Elf patiënten in 2017 waren gerelateerd aan de eerste landelijke uitbraak van listeriose in Nederland sinds de start van de surveillance in 2005. De bron van de uitbraak is niet gevonden. Er was een sterke epidemiologische associatie met haring. De grote spreiding van de patiënten over de tijd (14 maanden) bemoeilijkte het onderzoek. Daarnaast maakt de lange incubatietijd tot ongeveer 4 weken bij Listeria het voor de patiënten lastig om zich te herinneren wat ze precies hebben gegeten tijdens de voor de besmetting relevante periode.
Van 90% van de patiënten was een stam beschikbaar, terwijl dit in 2013-2016 tussen 65% en 74% lag. Er waren in 2017 maar 2 stammen (2%) die niet vergezeld gingen van een officiële melding, wat lager is dan de 6% in de 4 voorgaande jaren (2016: 6/96; 2015: 4/72; 2014: 6/95; 2013: 5/79). Dit is in ieder geval deels te verklaren door de uitbraak, waardoor er extra aandacht en inspanningen waren om zoveel mogelijk informatie te verzamelen.
In 2016 werden 7 zwangere vrouwen met listeriose gemeld, wat vergelijkbaar was met 2012 (n=6) en 2011 (n=9). In 2017 werden, evenals in 2013-2015, 3 zwangere vrouwen in een jaar gemeld. Twee van de 3 zwangerschappen eindigden in een doodgeboorte. Van de volwassenen overleden 10 personen (9%), vergelijkbaar met 2016 (9%) en 2013-2014 (10%), maar lager dan in 2015 (15/68 (22%)).
Vooral mensen met onderliggend lijden zijn gevoelig voor infecties met L. monocytogenes en hebben een grotere kans op een ernstig beloop van de infectie. (4, 5) Maagzuurremmers worden gezien als veilige medicatie en ook door mensen zonder ernstig onderliggend lijden gebruikt. De meerderheid van de listeriosepatiënten slikt maagzuurremmers. Een eerdere patiëntcontrolestudie uitgevoerd op de Nederlandse data liet zien dat dit mogelijk het risico op listeriose verhoogt. (6) In een groot patiëntcontroleonderzoek in Denemarken met 721 patiënten en 34844 gematchte controles, werd een onderscheid gevonden naar type maagzuurremmers (7). Gebruik van protonpompremmers in de 90 dagen ervoor was significant geassocieerd met listeriose, terwijl dit niet werd gevonden voor H-2- antagonisten. Mogelijke verklaring voor het verhoogde risico is de verminderde productie van maagzuur, waardoor bacteriën een grotere kans hebben om de passage door de maag te overleven.
Sinds 2017 is typering van de humane isolaten door PFGE vervangen door WGS. Ook de voedselisolaten worden sinds 2017 standaard gesequenced. WGS heeft een beter onderscheidend vermogen, geeft beter inzicht in stammen die maar iets van elkaar verschillen en is over het algemeen sneller beschikbaar dan PFGE. (8, 9) Deze wijziging in clusterdetectie heeft in dit eerste jaar niet geleid tot het vinden van meer of minder clusters dan bij gebruik van PFGE. De data van 1 jaar leveren echter weinig vergelijkingsmateriaal op. Via een Europese studie, ELiTE, zijn de humane isolaten uit de periode 2010-2016 gesequenced. Ook de voedselisolaten van 2016 en een deel van 2014-2015 zijn ondertussen gesequenced. Er is een start gemaakt om alle Nederlandse data van zowel voedsel als patiënten samen te voegen om retrospectief een vergelijking over meerdere jaren te maken. Voornaamste doel hierbij is om typen te identificeren die over de jaren terugkomen en matchen tussen humaan en voedsel. Dit zou indicatief zijn voor langdurige (industriële) bronnen van besmetting. WGS data van het RIVM en de NVWA worden real-time bijeen gebracht in een database waardoor in het geval van verheffingen wellicht sneller naar een bron is toe te werken.
Wij bedanken alle GGD’en en medisch microbiologische laboratoria hartelijk voor hun medewerking bij de verzameling van de patiëntengegevens en het insturen van isolaten. Verder gaat onze dank uit naar alle patiënten voor hun medewerking bij het beantwoorden van de vragen onder vaak moeilijke omstandigheden. Tenslotte bedanken we de personen binnen het RIVM (met name Ramon Noomen) voor hun werk aan de isolatie en typering van Listeria monocytogenes, de onderzoeksondersteuners van het laboratorium Voeder- en Voedselveiligheid van de NVWA voor het onderzoeken van de monsters en Redmar van den Berg voor de WGS-data-analyse van voedselisolaten.
Auteurs
I.H.M. Friesema1, S. Kuiling1, M.E.O.C. Heck1, M. van der Voort2, E.G. Biesta-Peters, W. Freudenburg-de Graaf3, A. van der Ende3, E. Franz1
- Centrum Infectieziektebestrijding, RIVM, Bilthoven
- Nederlandse Voedsel en Waren Autoriteit (NVWA), Divisie Handhaving
- Afdeling Medische Microbiologie, Nederlands Referentielaboratorium voor Bacteriële Meningitis, Amsterdam UMC, Universiteit Amsterdam
Correspondentie
Literatuur
- Maertens de Noordhout C., Devleesschauwer B., Angulo F.J., et al. The global burden of listeriosis: a systematic review and meta-analysis. The Lancet Infectious diseases 2014; 14: 1073-82.
- Chlebicz A., Slizewska K. Campylobacteriosis, Salmonellosis, Yersiniosis, and Listeriosis as Zoonotic Foodborne Diseases: A Review. International Journal of Environmental Research and Public Health 2018; 15.
- ECDC. Disease data from ECDC Surveillance Atlas - listeriosis. 2017. (Accessed 2018).
- Ramaswamy V., Cresence V.M., Rejitha J.S., et al. Listeria - Review of epidemiology and pathogenesis. J Microbiol Immunol Infect 2007; 40: 4-13.
- Drevets D.A., Bronze M.S. Listeria monocytogenes : Epidemiology, human disease, and mechanisms of brain invasion. FEMS Immunol Med Microbiol 2008; 53: 151-65.
- Friesema I.H., Kuiling S., van der Ende A., Heck M.E., Spanjaard L., van Pelt W. Risk factors for sporadic listeriosis in the Netherlands, 2008 to 2013. Euro Surveill 2015; 20: pii: 21199.
- Kvistholm Jensen A., Simonsen J., Ethelberg S. Use of Proton Pump Inhibitors and the Risk of Listeriosis: A Nationwide Registry-based Case-Control Study. Clin Infect Dis 2017; 64: 845-51.
- Moura A., Tourdjman M., Leclercq A., et al. Real-Time Whole-Genome Sequencing for Surveillance of Listeria monocytogenes, France. Emerg Infect Dis 2017; 23: 1462-70.
- Lüth S., Kleta S., Al Dahouk S. Whole genome sequencing as a typing tool for foodborne pathogens like Listeria monocytogenes - The way towards global harmonisation and data exchange. Trends in Food Science & Technology 2018; 73: 67-75.
Infectieziekten Bulletin, jaargang 29, nummer 11, december 2018
De LCI in 2017
De Landelijke Coördinatie Infectieziektebestrijding (LCI) van het Centrum Infectieziektebestrijding (CIb) van het RIVM is 24/7 bereikbaar voor professionals betrokken bij infectieziektebestrijding. De LCI wordt over uiteenlopende casuïstiek geconsulteerd door onder andere GGD’en, microbiologische laboratoria, ziekenhuizen, alarmcentrales en huisartsen. Daarnaast ontwikkelt de LCI richtlijnen en coördineert zij de respons bij uitbraken van infectieziekten en groep A-meldingsplichtige ziekten. Ook worden adviezen over infectieziekten aan het ministerie van Volksgezondheid, Welzijn en Sport (VWS) gegeven.
De LCI in 2017
Dagelijkse advisering en opschaling in 2017
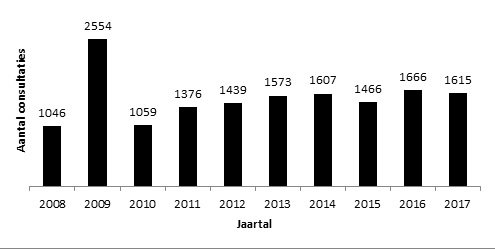
In 2017 is de LCI 1615 keer geconsulteerd (zie figuur 1); dit is iets minder ten opzichte van het jaar 2016 (1666). De meeste vragen gingen, net als in voorgaande jaren, over rabiës (n=591; 36,6% van het totaal aantal vragen, zie tabel 1). Daarnaast werden veel vragen gesteld over vaccinaties tegen onder andere influenza, difterie, tetanus en polio, kinkhoest, pneumokokken, meningokokken en hepatitis B (n=125; 7,7%). De meeste vragen gingen over casuïstiek (84%), maar er werden ook vragen gesteld over richtlijnen (6%), beleid (9%) en onderzoek (1%).
Figuur 1. Het aantal gestelde vragen aan de LCI van 2008 tot en met 2017
Net als in voorgaande jaren werden de meeste vragen gesteld door GGD’en (figuur 2). Daarna volgden zorgprofessionals uit de tweede lijn (zoals microbiologen en infectiologen) en internationale organisaties zoals de World Health Organization (WHO) en het European Centre for Disease Prevention and Control (ECDC). Ook in 2017 was er steeg aantal vragen van alarmcentrales/repatriëringsorganisaties. Zij hebben vaak het eerste contact met de patiënt in het buitenland. Het aantal consultaties van huisartsen aan de LCI is stabiel. Tijdens het griepseizoen is de LCI voor huisartsen eerste aanspreekpunt als zij vragen hebben over de influenzavaccinatie die ieder najaar wordt aangeboden aan kwetsbare patiënten en ouderen. Overige vragen van huisartsen over infectieziekten worden doorgaans in de eigen regio aan de GGD gesteld of aan artsen in het regionale ziekenhuis.
Figuur 2. Het aandeel in de gestelde vragen (% van totaal) aan de LCI in 2015, 2016 en 2017 per type organisatie
Omdat de Werkgroep Infectie Preventie (WIP) per 1 juni 2017 is opgeheven, is ook de helpdesk komen te vervallen. Er blijkt echter wel behoefte te zijn aan een helpdesk voor vragen over WIP-richtlijnen. Het ministerie van Volksgezondheid, Welzijn en Sport (VWS) heeft daarom de LCI gevraagd om deze dienstverlening tijdelijk over te nemen. Vanaf september 2017 kreeg de LCI 68 uiteenlopende vragen over de WIP-richtlijnen. Verderop in dit artikel wordt verslag gedaan van de werkwijze en de diversiteit aan vragen die de LCI, samen met casuïstiek (n= 283) die het Landelijk Centrum Hygiëne en Veiligheid (LCHV), in 2017 ontving.
Naast het geven van dagelijks advies is de LCI verantwoordelijk voor de coördinatie bij ingewikkelde infectieziekteproblematiek en voor het operationele crisismanagement tijdens een (dreigende) regio-overschrijdende uitbraak. In 2017 werden er 36 afstemmingsoverleggen (AO), 3 responsteams (RT), 5 deskundigenberaden (DB) en 1 expertmeeting georganiseerd.
- AO’s worden georganiseerd als er een signaal is (bijvoorbeeld verhoogde surveillance) of als er een risicobeoordeling moet worden gemaakt, waarbij het nog niet altijd nodig is om ook externe partijen te betrekken.
- Bij een RT wordt verwacht dat er langdurige inzet nodig is van diverse (in- en externe) partijen ten behoeve van de uitbraakbestrijding.
- Bij een DB is het de bedoeling dat er een advies over een bepaald onderwerp tot stand komt dat door diverse partijen ondersteund wordt en uiteindelijk leidt tot een advies aan het ministerie van VWS.
Meer informatie is te vinden in de folder Landelijke advisering bij infectieziektedreiging- en crisis: https://www.rivm.nl/documenten/folder-landelijke-advisering-bij-infectie...
Een belangrijk onderwerp in 2017 was de uitbraak van hepatitis A onder Mannen die Seks hebben met Mannen (MSM). Ook was er een kleinere hepatitis A-uitbraak gerelateerd aan bevroren rood fruit. Tegelijkertijd bleken er vaccintekorten voor zowel hepatitis A en hepatitis B. Alle onderwerpen werden besproken in 1 of meerdere AO’s. Vanwege een poliobesmettingsgeval bij een vaccinproductiefaciliteit werden RT’s georganiseerd (zie verderop in dit artikel). Begin 2017 kwam er een einde aan de in 2016 begonnen uitbraak van Salmonella Enteritis, maar volgde er meteen weer een andere landelijke salmonella-uitbraak ( S. Bovismorbificans, zie ook verderop). AO’s werden ook georganiseerd ten behoeve van de risico-inschatting en maatregelen naar aanleiding van ratten met seoulvirus waarbij mensen besmet waren. Voor deze zoönose, alsmede voor brucellose, werden deskundigenberaden (DB-Z’s) georganiseerd. Ook werden DB’s georganiserd voor azolenresistente Aspergillus, meningokokken W en ESBL/CPE. Tenslotte werden AO’s georganiseerd over listeriose- en legionellacasuïstiek. Afhankelijk van het type overleg en besluit wordt de uitkomst gecommuniceerd via bijvoorbeeld een (lab)Inf@ct, een nieuwsbericht, een persbericht of een adviesbrief aan het ministerie.
Top 10-onderwerpen van LCI-consultaties
De meestgestelde vragen aan de LCI in 2017 gingen, net als in voorgaande jaren, over rabiës (n=519; 36,3%, zie tabel 1). De meeste vragen zijn afkomstig van GGD’en en van alarmcentrales en repatriëringsorganisaties. Een enkele keer belt een tropencentrum met de LCI. De vragen gaan bijna altijd over de indicatiestelling voor postexpositieprofylaxe voor het dure en schaarse middel humaan anti-rabiës immunoglobulinen (MARIG). In 2016 was er een flinke stijging van het aantal meldingen te zien (618), in 2017 ligt het aantal iets lager (591), maar nog steeds hoog ten opzichte van de afgelopen 10 jaar. In 2017 is de LCI een door ZonMW gesubsidieerd onderzoek gestart naar de determinanten van reizigers die blootgesteld worden aan potentieel rabide dieren tijdens hun vakantie. Deze determinanten zullen input vormen voor het rabiësprotocol van de LCR om personen die een verhoogd risico lopen gericht pre-expositieprofylaxe of voorlichting aan te bevelen. Dit onderzoek wordt uitgevoerd in samenwerking met de LCR, LUMC, GGD Amsterdam, GGD regio Utrecht, GGD Hart voor Brabant en GGD West-Brabant . (3)
De vaccinatievragen (n=125) staan op de tweede plaats in de top 10. Twintig procent ging over influenzavaccinatie. Daarnaast werden vragen gesteld over vaccinatie tegen difterie, tetanus en polio (10%), hepatitis B (10%), kinkhoest (10%), pneumokokken (10%) en meningokokken ACWY (6%). De vragen over vaccinatie staan al 5 jaar in de top 3.
De derde plek wordt ingenomen door het onderwerp Mers-coronavirus (MERS-CoV). Met name rondom de Hadj neemt het aantal vragen aan de LCI rond dit onderwerp toe. Een infectie met Mers-CoV bij een patiënt in een ziekenhuis moet gemeld worden. Zodra er een verdenking is van een patiënt, dient de behandelend arts contact op te nemen met de LCI zodat beoordeeld kan worden of de patiënt aan de casusdefinitie voldoet, waarna laboratoriumdiagnostiek ingezet kan worden. In 2017 is de diagnose bij niemand in Nederland bevestigd.
Op nummer 4 staat het onderwerp Zika. In 2016 was dit een nieuwkomer. In Brazilië werd een uitbraak ontdekt nadat er ongewone stijging bleek te zijn van het aantal pasgeboren baby’s met microcefalie en een gelijktijdige toename van het aantal patiënten met het syndroom van Guillain-Barré. In 2016 werden er 129 vragen aan de LCI gesteld en in 2017 daalde het aantal (n=42) doordat de uitbraak in Brazilië in omvang afnam en de afspraken voor Nederland rond diagnostiek en beleid meer bekend waren bij GGD’en en andere zorgprofessionals.
Opvallend in de top 10 is de terugkeer van de onderwerpen Mazelen op nummer 5 en Hepatitis A op nummer 7. Salmonella en Groep A-streptokokken zijn geheel nieuw in de top 10.
Mazelen stond voor het laatst in 2014 in de top 10 nadat in 2013 in Nederland een grote mazelenuitbraak was. (4) Sinds 2017 is in diverse landen in Europa een toename te zien van het aantal patiënten met mazelen en daardoor werden in Nederland ook enkele importpatiënten met mazelen (of verdenking) gerapporteerd. Omdat mazelen zeer besmettelijk is en een nieuwe melding het begin van een uitbraak kan zijn, neemt de LCI bij een nieuwe mazelencasus altijd op korte termijn contact op met de GGD. Ook wordt aan de GGD gevraagd om met het regionaal laboratorium contact op te nemen zodat klinisch materiaal doorgestuurd wordt voor typering en clusteranalyse door het nationaal referentielaboratorium voor mazelen . In Nederland is dat ondergebracht bij het RIVM en het ErasmusMC.
Het aantal hepatitis A-vragen nam toe door de uitbraak onder MSM. (5,6) Ook werd er een uitbraak gemeld waarbij bevroren rood fruit als bron werd aangewezen. (7)Salmonella is geheel nieuw in de top 10, nadat in 2016 een verheffing te zien was van het aantal patiënten besmet met een specifiek type Salmonella enteritidis in Nederland en in Europa. Na intensieve samenwerking tussen NVWA, GGD, CIb, het ECDC en andere Europese overheidsinstanties en laboratoria, bleek de uitbraak terug te voeren naar Poolse eieren. (8) De uitbraak was begin 2017 ten einde, maar werd meteen gevolgd door een verheffing van de Salmonella bovismorbificans, wat gerelateerd bleek aan ham. (9,10)Het aantal vragen over Groep A- streptokokken (GAS) nam toe en dat is ook terug te zien in het aantal meldingen van (meldingsplichtige) GAS-infecties dat het RIVM ontving : fasciitis necroticans, septische shock en puerperale sepsis [https://www.rivm.nl/groep-a-streptokokkeninfecties-gas]. De vragen die gesteld werden aan de LCI gingen voornamelijk over het beleid van antibioticaprofylaxe voor contacten.
Tabel 1. Overzicht top 10 consultatieonderwerpen in 2017 naast die van 2013-2016
| 2013 | N (%) | 2014 | N (%) | 2015 | N (%) | |
|---|---|---|---|---|---|---|
| 1. | Rabiës | 485 (30,8) | Rabiës | 451 (28,0) | Rabiës | 526 (35,9) |
| 2. | Mazelen | 207 (13,2) | Ebola | 301 (18,7) | Vaccinatieadvies | 90 (6,1) |
| 3. | Vaccinatieadvies | 141 (9,0) | Vaccinatieadvies | 139 (8,6) | Ebola | 81 (5,5) |
| 4. | MERS-CoV | 69 (4,4) | MERS-CoV | 129 (8,0) | MERS-CoV | 62 (4,2) |
| 5. | Influenza | 37 (2,4) | Aviaire influenza | 39 (2,4) | Scabiës | 32 (2,2) |
| 6. | Hepatitis B | 36 (2,3) | Kinkhoest | 36 (2,2) | Hepatitis B | 30 (2,0) |
| 7. | MRSA | 36 (2,3) | Mazelen | 35 (2,2) | Influenza | 30 (2,0) |
| 8. | Tuberculose | 29 (1,8) | Varicella | 26 (1,6) | Kinkhoest | 29 (2,0) |
| 9. | Legionellose | 27 (1,7) | Legionellose | 23 (1,4) | Legionellose | 28 (1,9) |
| 10. | Tetanus | 27 (1,7) | Hepatitis B | 22 (1,4) | Asielzoekers-gerelateerde vragen | 27 (1,8) |
| Anders | 620 (39,4) | Anders | 430 (26,7) | Anders | 531 (36,2) | |
| Totaal | 1573 | Totaal | 1609 | Totaal | 1466 |
| 2016 | N (%) | 2017 | N (%) | |
|---|---|---|---|---|
| 1. | Rabiës | 618 (37,1) | Rabiës | 591 (36,6) |
| 2. | Zika | 129 (7,7) | Vaccinatieadvies | 125 (7,7) |
| 3. | Vaccinatieadvies | 113 (6,8) | MERS-CoV | 58 (3,6) |
| 4. | Meningokokken-infectie | 51 (3,1) | Zika | 42 (2,6) |
| 5. | MERS-CoV | 46 (2,8) | Mazelen | 37 (2,3) |
| 6. | Aviaire influenza | 29 (1,7) | Meningokokken-infectie | 34 (2,1) |
| 7. | Tuberculose | 28 (1,7) | Hepatitis A | 30 (1,9) |
| 8. | Influenza | 25 (1,5) | Salmonella | 28 (1,7) |
| 9. | Legionellose | 25 (1,5) | Influenza | 26 (1,6) |
| 10. | Varicella | 25 (1,5) | Streptokokkeninfecties-groep-A | 24 (1,5) |
| Anders | 577 (34,6) | Anders | 620 (38,4) | |
| Totaal | 1666 | Totaal | 1615 |
Bijzondere casuïstiek
Wildpoliovirustype 2-besmetting in een vaccinproductiefaciliteit
Begin april 2017 is er een incident geweest bij een vaccinproductiefaciliteit. Twee volledig gevaccineerde medewerkers werden blootgesteld aan wildpoliovirustype 2 (WPV2), een poliovirustype dat wereldwijd uitgeroeid is. (11) Conform het protocol werd meteen gestart met het monitoren van beide medewerkers door het afnemen en onderzoeken van keel- en fecesmonsters. Binnen een dag nadat bekend werd dat 1 van de medewerkers positief was voor WPV2. Er werd een responsteam gevormd om de vervolgstappen te bespreken. Dit responsteam bestond uit artsen infectieziektebestrijding van de LCI en GGD’en, een bedrijfsarts, een viroloog, een deskundige infectiepreventie, een epidemioloog, een beleidsadviseur, veiligheidsfunctionarissen van de productiefaciliteit en een communicatiespecialist.
Het responsteam was verantwoordelijk voor het maken van een gestructureerde inschatting van de volksgezondheidsrisico’s. Verder werden er afspraken gemaakt voor de verdere monitoring van de besmette medewerker en zijn contacten. Ook was het responsteam verantwoordelijk voor de meldingen en informatievoorziening aan media, zorgprofessionals en internationale contacten als de WHO en het ECDC, die op de hoogte gehouden wilden worden van de situatie.Binnen het responsteam vond afstemming plaats tussen de verschillende partijen en werd gezocht naar oplossingen voor problemen die zich voordeden in de praktijk. Zo moest er een balans worden gevonden tussen de strenge eisen die gesteld werden in het GAPIII-document van de WHO (12) waarin staat dat volledige inperking van WPV2 noodzakelijk is en er geen WPV2 in het milieu mag komen en de haalbaarheid en leefbaarheid voor de betrokken medewerker beschrijft.
De besmette medewerker werd in vrijwillige thuisisolatie geplaatst waarbij hij dagelijks contact had met de GGD. Om de verdere verspreiding van het poliovirus zo goed mogelijk in te perken werden zeer strikte hygiënemaatregelen opgelegd: er werd een speciaal toilet geïnstalleerd, naar analogie met het Ebolaprotocol, om de besmette ontlasting apart af te kunnen voeren; ook moest aan het einde van de isolatieperiode het huis compleet gedesinfecteerd met waterstofperoxidefogging.Tot 29 dagen na blootstelling kon WPV2 worden aangetoond in de feces van de besmette medewerker.
In totaal zijn er 7 overleggen georganiseerd door de LCI. Nadien heeft een evaluatie van het incident plaatsgevonden met alle betrokken partijen. Momenteel wordt gewerkt aan een mogelijke aanpassing van de meldingsplicht voor dergelijk incidenten met A-ziekten en aan een draaiboek voor incidenten met WPV.
Hygiëneadviezen
283 vragen hadden betrekking op hygiëne en werden beantwoord door de medewerkers van het Landelijk Centrum Hygiëne en Veiligheid (LCHV) van het RIVM/CIb, samen met deskundigen infectiepreventie-adviseurs (DI-a) die vanuit een aantal GGD’en bij de LCI zijn gedetacheerd. De meeste vragen werd gesteld door GGD-collega’s (n=157) en hadden betrekking op situaties die de GGD tegenkomt bij toezicht- en inspectietaken zoals tatoeage en piercing, sanitaire certificatie van schepen en bezoeken aan festivals en seksbedrijven. Veel vragen gingen over de juiste wijze van desinfectie, waarover door met name de Nederlandse regels verwarring ontstaat. Ook had men vaak behoefte aan overleg over een hygiënerisicobeoordeling, bijvoorbeeld bij evenementen met een groot aantal bezoekers of bij een gecombineerde kappers/piercingstudio. Verder gingen de vragen over hygiëne in de zorg, in met name de thuiszorg, waar actuele hygiënerichtlijnen niet voorhanden zijn. Er werden meer vragen gesteld over mud races, obstacle runs en evenementen met dieren.
Voor de beantwoording van die vragen maakt de LCHV ook gebruik van kennis bij collega’s binnen en buiten RIVM. Ook adviseerde het LCHV vaker terug aan deze collega’s over hygiënemaatregelen bij specifieke casuïstiek, evenals over maatregelen bij legionellapreventie.
De LCHV, vlnr: Marloes Bongers, Leo van der Laan, Saskia Tejland, Hella Kok, Alvin Bartels, Janneke Broekhuijsen, Peter Molenaar, Petri Kuijlaars, Thijs Veenstra
De helpdesk voor hygiënevragen die voorheen door de WIP werden behandeld is in september 2017 bij de LCI ondergebracht. In de maanden die volgden werden 68 vragen gesteld. Voor de behandeling van die vragen werd gebruik gemaakt van kennis van een externe deskundige infectiepreventie en van kennis bij het LCHV. De meeste vragen (n=30) werden gesteld door deskundigen infectiepreventie en kwaliteits- en arbomedewerkers die zich bezighouden met het beleid dat op het gebied van infectiepreventie in de zorginstellingen wordt gevoerd. De overige vragen werden door verschillende andere professionals gesteld, regelmatig waren dat verpleegkundigen, maar varieert verder van ok-assistenten tot laboratoriummedewerkers. De meeste vragen gingen over persoonlijke beschermingsmiddelen en persoonlijke hygiëne en over de interpretatie van de bestaande richtlijnen in specifieke situaties. Een vraag die gesteld werd ging bijvoorbeeld over het dragen van laboratoriumjassen door laboratoriumpersoneel tijdens prikrondes op een verpleegafdeling, en of een medewerker op de intensive care een elastische kous over hand en arm mag dragen. Verder werden veel vragen gesteld over reiniging en desinfectie. In veel gevallen werden deze vragen gesteld in relatie tot Bijzonder Resistente Micro-organismen. Ook waren er in relatie daarmee vragen over barrière en isolatie.
Deze helpdesk voor de intramurale zorg wordt voortgezet, in afwachting van ontwikkelingen ter opvolging van de WIP.
Wie staat u te woord als u de LCI consulteert?
Het LCI-responsteam bestaat uit 9 beleidsadviseurs (voorwachten) en 7 artsen infectieziektebestrijding (achterwachten) en 2 artsen in opleiding (tussenwachten).
Van maandag tot en met vrijdag van 8:30 tot 17:00 uur worden infectieziekteprofessionals door het LCI- secretariaat doorverbonden met de voorwacht. De voorwacht neemt de vraag of het signaal in behandeling, daarbij is het van belang dat er snel een zo compleet mogelijk beeld wordt verkregen van de situatie. De voorwacht gaat op zoek naar het antwoord en raadpleegt (nationale en internationale) richtlijnen, vergelijkbare casuïstiek en/of literatuur. Er wordt, zo nodig, overlegd met LCI-collega’s met een specifieke deskundigheid (huisarts, infectioloog, bedrijfsarts, arbeidshygiënist etc.) en/of deskundigen van andere centra binnen het CIb (Epidemiologie en Surveillance van Infectieziekten, Infectieziekteonderzoek, Diagnostiek en laboratoriumSurveillance, Zoönosen en Omgevingsmicrobiologie, Immunologie van Infectieziekten en Vaccins). Ook worden experts buiten het RIVM/CIb of GGD’en die te maken hebben gehad met vergelijkbare casuïstiek, geconsulteerd. Uiteindelijk wordt het antwoord besproken met de tussen- of achterwacht van het LCI-responsteam en pas daarna wordt de vraagsteller teruggebeld om het antwoord te bespreken.
Alle vragen of signalen, dus ook e-mails of berichten die internationaal bij de LCI (als National Focal Point) terechtkomen, worden vastgelegd. Buiten kantoortijden is de LCI bereikbaar voor spoedoverleg, de vraagsteller wordt dan via de meldkamer in contact gebracht met de dienstdoende arts infectieziektebestrijding van de LCI. Zowel binnen als buiten kantoortijden is de LCI bereikbaar via 030-2747000.
Het voorwachtteam bestaat uit beleidsadviseurs met een verpleegkundige-, biomedische- of gezondheidswetenschappelijke achtergrond. Iedere adviseur heeft zijn/haar eigen aandachtsgebied(en), is inzetbaar voor de voorwachtdienst en voor het coördineren en organiseren van afstemmingsoverleggen, deskundigenberaden of andere overleggen bij crises. Er wordt daarin samengewerkt met de artsen Maatschappij en Gezondheid, profiel Infectieziektebestrijding.
Het responsteam, vlnr: Hans van den Kerkhof, Ton Oomen, Sabine Bantjes, Suzanne Kliffen, Marijke van Cooten, Helma Ruijs, Manon Haverkate, Margreet te Wierik, Madelief Mollers, Imke Schreuder, Peter Molenaar, Annemarie Meiberg, Corien Swaan, Rosa Joosten en Gini van Rijckevorsel.Niet op de foto: Aura Timen, Sabiena Feenstra, Willemijn Marsman, en de regionaal consulenten die het responsteam buiten kantooruren versterken: Ariene Rietveld, Peter Jacobs, Rob van Kessel en Toos Waegemaekers.
De auteurs danken Helma Ruijs, Erwin Duizer en Petri Kuijlaars voor het meelezen en bewerken van de bijzondere casuïstiek in dit artikel.
Auteurs
A.E. Meiberg, M.R. Haverkate, T.Veenstra, C.M. Swaan, Centrum Infectieziektebestrijding, RIVM, Bilthoven
Correspondentie
Literatuur
- Haverkate MR, Jacobi A,Oomen T, Swaan CM. De LCI in 2016. Infectieziekten Bulletin 2017: 28(8);273-8
- Haverkate MR, Mollers M, Swaan CM. De LCI in 2015. Infectieziekten Bulletin, 2016,26(10)
- Zon Mw-project Predictors of rabies exposure in travelers
- Woudenberg T, van Binnendijk RS, Sanders EA, Wallinga J, de Melker HE, Ruijs WL, Hahné SJ. Euro Surveillance. Large measles epidemic in the Netherlands, May 2013 to March 2014: changing epidemiology. 2017 Jan 19;22(3)
- Freidl GS, Sonder GJ, Bovée LP, Friesema IH, van Rijckevorsel GG, Ruijs WL, van Schie F, Siedenburg EC, Yang JY, Vennema H. Hepatitis A outbreak among men who have sex with men (MSM) predominantly linked with the EuroPride, the Netherlands, July 2016 to February 2017. Euro Surveill. 2017 Feb 23;22(8). pii: 30468. doi: 10.2807/1560-7917.ES.2017.22.8.30468.
- Friesema IHM, Sonder GJB, Petrignani MFW, Meiberg AE, van Rijckevorsel GGC, Ruijs WLM, Vennema H. Hepatitis A onder MSM. Infectieziekten Bulletin, 2018, 29(10)
- Mollers M, Boxman ILA, Vennema H, Slegers-Fitz-James IA, Brandwagt D, Friesema IH, Batstra JS, Te Wierik MJM. Successful Use of Advertisement Pictures to Assist Recall in a Food-Borne Hepatitis A Outbreak in The Netherlands, 2017. Food Environ Virol. 2018 Sep;10(3):272-277. doi: 10.1007/s12560-018-9347-3. Epub 2018 May 4.
- Pijnacker R, Tijsma ASL, Friesema IHM, Voort van der M, Nijs de R, Slegers-Fitz-James IA, Heck MEOC, Kuiling S, Kerkhof van den JHCT, Leblanc JMJ, Franz E. Bronopsporing bij een langdurige internationale uitbraak van Salmonella Enteritidis. Infectieziekten Bulletin, 2017, 28(6): 181-187
- Brandwagt D, Wijngaard van den C, Tulen AD, Mulder AC, Hofhuis A, Jacobs R, Heck M, Verbruggen A, Kerkhof van den H, Slegers-Fitz-James I, Mughini-Gras L, Franz E. Outbreak of Salmonella Bovismorbificans associated with the consumption of uncooked ham roducts, the Netherlands, 2016 to 2017. Euro Surveill. 2018;23(1):pii=17-00335.
- W. van Pelt, M. van der Voort, M-J. Mangen, K. Veldman, B. Wit, E. Franz, M. Heck, R. Pijnacker, I. Friesema, L. Mughini-Gras. Salmonella in Nederland in 2017. Infectieziekten Bulletin, 2018, 29(7)
- Duizer E, Ruijs WL, van der Weijden CP, Timen A. Response to a wild poliovirus type 2 (WPV2)-shedding event following accidental exposure to WPV2, the Netherlands, April 2017. Euro Surveill 2017; 22 (21): pii: 30542
- WHO. WHO Global Action Plan to minimize poliovirus facility-associated risk after type-specific eradication of wild poliovirusses en sequential cessation of oral polio vaccine use. Geneva: WHO; 2015.
Infectieziekten Bulletin, jaargang 29, nummer 11, december 2018
Aankondigingen
Mazelenvirus en schade afweersysteem
Het mazelenvirus infecteert en doodt de geheugencellen van ons afweersysteem. Dat is de conclusie van een studie van onderzoekers van het Erasmus MC in Rotterdam, die deze week wordt gepubliceerd in het tijdschrift Nature Communications. Mazelen verzwakt het afweersysteem, waardoor kinderen na herstel van mazelen vatbaarder zijn voor andere infectieziekten. In een recent in BMJ Open gepubliceerde epidemiologische studie liet dezelfde onderzoeksgroep zien dat kinderen tot enkele jaren na mazelen gemiddeld meer infecties doormaken dan kinderen die geen mazelen hadden gehad.
Naar artikel
Registratie infectieziekten
Wet publieke gezondheid
De meldingen Wet publieke gezondheid tot en met week 48, 2018
Virologische weekstaten
De meldingen in de virologische weekstaten tot en met week 48, 2018