Gesignaleerd
Overzicht van bijzondere meldingen, clusters en epidemieën van infectieziekten in binnen- en buitenland tot en met 31 januari 2019.
Binnenlandse signalen
Griepseizoen in Nederland
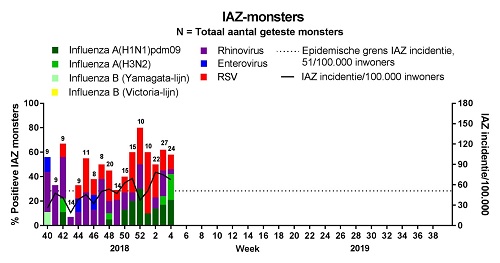
In week 4 van 2019 rapporteerden de peilstations participerend in Nivel Zorgregistraties eerste lijn 68 mensen met influenza-achtig ziektebeeld (IAZ) op de 100.000 inwoners (figuur 1), boven de epidemische grens van 51 per 100.000 inwoners. Dit is daarmee de zevende week van deze griepepidemie. De griepepidemie zet echter nog niet erg door, want de incidentie is lager dan in de voorgaande 2 weken (79 en 75/100.000 inwoners in week 2 en 3 respectievelijk). In het begin van de epidemie bleek een groot deel van de IAZ-gevallen in huisartspraktijken niet het gevolg van influenzavirussen, maar voornamelijk van RSV en rhinovirussen. Vanaf week 2 namen influenzavirusinfecties toe, al was de proportie RSV- en rhinovirusinfecties samen genomen hoger dan dat van de influenzavirusinfecties. In week 4 leek het tij te keren doordat 42% van de IAZ-patiënten waarbij onderzoek was gedaan positief testten voor influenzavirus en slechts 17% voor RSV in combinatie met rhinovirus. Echter, dit heeft zich nog niet vertaald in een toename van de incidentie van patiënten met IAZ.Het begin van dit griepseizoen werd gedomineerd door influenza A-virussen van het A(H1N1)pdm09 subtype, maar de laatste weken neemt de proportie van het subtype A(H3N2) toe.De Nederlandse A(H3N2)-virussen behoren vooral tot clade 3C.2a1b, en in mindere mate tot clades 3C.2a1, 3C.2a2 en 3C.3a. De vaccinstam behoort tot clade 3C.2a1 die aan de voet staat van clade 3C.2a1b maar er genetisch van verschilt. Ondanks dat verschil geeft de WHO aan dat de virussen van clade 3C.2a1 en 3C.2a1b antigeen goed matchen met cel-gebaseerde vaccins maar minder goed met ei-gebaseerde vaccins. De andere clades matchen antigeen niet goed met de vaccinstam. De vaccins die we in Nederland gebruiken zijn op eieren geproduceerd en daardoor is de verwachting dat de vaccineffectiviteit tegen de nu circulerende A(H3N2)-virussen niet optimaal zal zijn. Alle A(H1N1)pdm09-virussen in Nederland vallen in clade 6B.1 net als de vaccinstam, al is enige genetische diversiteit zichtbaar. De WHO geeft aan dat de overgrote meerderheid van de huidig circulerende A(H1N1)pdm09-virussen ondanks de genetische diversiteit antigeen goed matchen met de stam in het vaccin. Dat is ook de bevinding van de karakteriseringen van A(H1N1)pdm09-virussen die in Nederland zijn gedaan. Daardoor is de verwachting dat de vaccineffectiviteit tegen de huidig circulerende A(H1N1)pdm09-virussen goed zal zijn. Berekening van de interim vaccineffectiviteit volgt later in januari uit de Europese I-MOVE- studie. In Europa neemt over het algemeen de influenza-activiteit toe, waarbij influenza A- virussen domineren: A(H1N1)pdm09 wordt iets vaker aangetoond dan A(H3N2). (Bronnen: Nivel, RIVM, ErasmusMC, WHO, Flu news Europe)
Figuur 1. Incidentie van influenza-achtig ziektebeeld (IAZ) en laboratoriumuitslagen van monsters van patiënten met IAZ bij de huisarts, Nederland, week 40 2018 – week 4 2019
Therapieresistente scabiës bij een zorgverlener
In het noorden van het land is scabiës (schurft) vastgesteld die klinisch resistent leek tegen de gebruikte scabicide middelen. De jongvolwassen patiënt meldde zich eind september bij de huisarts met jeukklachten en bultjes op de pols. Hij/zij werkte in de gezondheidszorg en was verder gezond. Na vaststelling van de diagnose door de huisarts en dermatoloog werd hij/zij 2 keer behandeld met permetrine en vervolgens 2 keer met ivermectine in combinatie met permetrine. Eind november werd hij/zij nogmaals onderzocht door een dermatoloog en arts-microbioloog; toen werden gangetjes in de huid aangetroffen. Na multidisciplinair overleg werd besloten om hem/haar te behandelen met 3 maal ivermectine (dag 1, 8 en 15) en 3 maal permetrine. Medio december werden door de dermatoloog geen mijten (Sarcoptes scabiei) meer aangetroffen. Ook bij de directe contacten van de patiënt (ouders en vriend) die waren meebehandeld, werden geen mijten aangetroffen. Het onderzoek van de GGD leverde een paar mogelijke besmettingsbronnen op waaronder een hostel waar de patiënt anderhalve week voor aanvang van de klachten verbleef. Ook is gedacht aan het paard van de patiënt als mogelijke bron van besmetting, maar dit bleek toch zeer onwaarschijnlijk. Varianten van sarcoptes komen in Nederland namelijk niet bij paarden voor. Scabiës bij dieren kan bij de mens jeukklachten, puistjes en blaasjes veroorzaken, maar de mijten graven zich niet in in de menselijke huid.Bij scabiës is het niet alleen belangrijk om de patiënt en zijn huishoudcontacten gelijktijdig te behandelen. Ook hun kleding en beddengoed moet worden gewassen en gelucht. Verder moet gedacht worden aan het reinigen van bijvoorbeeld banken, autostoelen, etc. Ondanks de zeer zorgvuldige behandeling van de patiënt en de andere maatregelen conform de richtlijn, kwam de scabiës telkens terug. Er was zeer waarschijnlijk sprake van therapieresistente scabiës. Dit is vaker beschreven in de literatuur. Behandeling met benzylbenzoaat is een alternatief, maar dit middel is in Nederland moeilijk verkrijgbaar. (Bronnen: GGD Groningen, UMCG, Khalil et al., PLoS Negl Trop Dis 2017, Aussy et al., Br J Dermatol 2018)
Toename para-influenzavirus type 2 in de Virologische Weekstaten
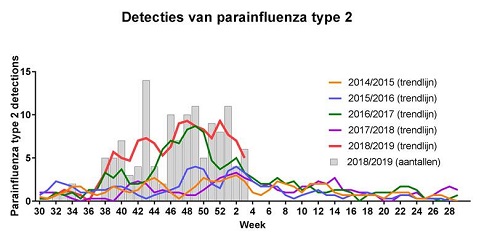
In de Virologische Weekstaten is sinds oktober 2018 een toename van para-influenzavirus type 2 (PIV-2) te zien (zie Figuur 2). In week 40 tot en met 3 van 2019 waren er 115 meldingen, ten opzichte van gemiddeld 44 in dezelfde periode in 2014 tot en met 2017 (spreiding: 29 - 79). De meldingen worden gedaan door meerdere laboratoria, waarbij er voor zover bekend geen sprake is van veranderingen in diagnostiek of testbeleid. PIV-2 kan pseudokroep veroorzaken en bovenste- en ondersteluchtweginfecties met griepachtige symptomen. Er is weinig bekend over de epidemiologie van PIV-2. De enkele studies geven aan dat er een cyclus van om de 2 jaar verheffing voor kan komen. In Nederland was er 2 jaar geleden (seizoen 2016/2017) ook een (iets minder hoge) verheffing met 79 meldingen in de periode van week 40- week 3. Er kunnen lokaal diverse varianten circuleren zonder snelle wereldwijde spreiding. De oorzaak van de cyclus is niet duidelijk. Het ontstaan van antigene varianten en een niet volledige immuniteit na infectie op jonge leeftijd kunnen hierbij een rol spelen. (Bronnen: RIVM, Virologische Weekstaten, Branche et al, Semin Respir Crit Care Med 2016)
Figuur 2. Aantal meldingen van para-influenzavirus type 2 in de Virologische Weekstaten. In week 3 van 2019 hebben mogelijk nog niet alle laboratoria gemeld. Absoluut aantal meldingen per week in 2018-2019. De trendlijnen zijn een 3-weeks gemiddelde
Buitenlandse signalen
Toename van acute slappe verlamming in het Verenigd Koninkrijk
Public Health England rapporteerde eind december 2018 een toename van patiënten met acute slappe verlamming (AFP). In 2018 werden 28 AFP patiënten gemeld, aanzienlijk meer dan voorgaande jaren. De ziektegevallen deden zich voornamelijk voor vanaf september. Bij 12 patiënten is een enterovirus gevonden. Bij 8 van hen werd het enterovirus-D68 (EV-D68)gevonden. Dit is één van de enterovirussen waarvan bekend is dat het AFP kan veroorzaken. Eerder in 2018 meldde Public Health Wales een toename van EV-D68-infecties met een piek in oktober. Van de 220 gemelde patiënten met een EV-D68-infectie in Wales tussen september 2015 en 5 november 2018 hadden 2 patienten (1%) AFP. In de Verenigde Staten wordt al sinds 2014 een toename gerapporteerd van het aantal patiënten met AFP, met elke 2 jaar een piek, ook in 2018. Deze toenames worden vooral geassocieerd met EV-D68- en EV-A71-infecties.In Nederland wordt EV-D68 sinds 1997 sporadisch gezien in de peilstations van het Nivel/RIVM. In het najaar van 2010 was de eerste verheffing van EV-D68-infecties te zien, in zowel de Nivel/RIVM als de Type-Ned enterovirussurveillance, met vervolgens iedere 2 jaar een verheffing in de nazomer/herfst. In beide surveillancebronnen was de verheffing in 2018 lager dan in 2016. Wel waren er 2 patiënten - in 2016 en 2018 - met AFP en EV-D68-infectie. Of dit alle patiënten zijn geweest, is niet duidelijk; sinds 2003 is er in Nederland geen AFP-surveillance meer. (Bronnen: Helfferich J et al. NTvG 2017, Knoester M. et al. Pediatr Infect Dis J 2019, PHE, PHW, CDC, RIVM)
Uitbraken van polio wereldwijd
Uit de registratiegegevens van de WHO van 2 januari 2019 blijkt dat in 2018 in Afghanistan en Pakistan respectievelijk 21 en 8 patiënten met polio door wildpoliovirustype 1 (WPV1) zijn gemeld. Dit is een toename van 7 patiënten periode ten opzichte van 2017. In beide landen wordt regelmatig WPV1 gevonden in rioolwater in regio’s waar geen patiënten worden gemeld. In 2018 hebben 5 landen in totaal 100 patiënten met polio gemeld veroorzaakt door circulating vaccine derived poliovirustype (cVDPV). Dit aantal ligt iets hoger dan het aantal patiënten door cVDPV in 2 landen in 2017. In Papoea-Nieuw-Guinea werden 26 patiënten gemeld met polio veroorzaakt door cVDPV1 , in Nigeria 33 patiënten door cVDPV2, in, de Democratische Republiek Congo (DRC) 20 patiënten door 3 verschillende typen cVDPV2,, in Niger 9 patiënten door cVDPV2 uit Nigeria en 5 poliopatiënten in Somalië. Daarnaast rapporteerde Somalië 6 poliopatiënten veroorzaakt door cVDPV3, en in 1 patiënt werd zowel cVDPV2 als cVDPV3 geïsoleerd. Voor Nigeria en DRC geldt wel dat in verschillende regio’s voor het eerst sinds jaren weer surveillance wordt uitgevoerd en vaccinaties gegeven. De WHO geeft aan dat de polio-uitbraak in Syrië die werd veroorzaakt door cVDPV2 en in 2017 werd vastgesteld, nu over is. (Bronnen: EMRO, GPE)
Opnieuw uitbraak van pest op Madagaskar
In 2017 was er een uitbraak van (long)pest in Madagaskar die duurde van augustus tot en met november. Ook in 2018 was er weer sprake van een uitbraak. Tussen tussen 1 augustus en 18 november, werden 36 patiënten met builenpest en 10 patiënten met longpest gemeld. 5 patiënten met builenpest en 9 patiënten met longpest zijn overleden. De patiënten kwamen uit 13 van de 114 districten, waaronder districten dicht bij de hoofdstad gelegen. Pest wordt veroorzaakt door Yersinia pestis en wordt overgebracht op mensen door beten van besmette vlooien van ratten of andere (knaag)dieren. Longpest is de meest virulente vorm en kan van mens-op-mens worden overgedragen via hoesten. Sinds de jaren ‘90 worden in rurale gebieden in Madagaskar jaarlijks rond de 200 patiënten met builenpest gezien. Het is echter uitzonderlijk dat er zoals in 2017 niet alleen longpest voorkomt maar dat er ook longpestpatiënten worden gemeld in steden.. Besmetting is te voorkomen door het contact met patiënten en met dode dieren te vermijden. Verder is het belangrijk om antimuggenmiddelen te gebruiken, zoals bijvoorbeeld DEET. Deze middelen zijn ook effectief tegen vlooien. (Bronnen: Ministère de la Santé Publique Madagascar, CDC, UNOCHA)
Chikungunya in het zuiden van Thailand
De gezondheidsautoriteiten van Thailand melden een toename van het aantal patiënten met chikungunya in het zuiden van het land. Tussen 17 oktober en 10 december 2018 werden 1.690 patiënten gemeld, waarvan 1.132 in november. Het totale aantal patiënten in 2018 is 2.143 (peildatum 10 december) in 13 provincies, ten opzichte van 10 patiënten in heel 2017. Er zijn geen sterfgevallen bekend. De meeste patiënten werden gemeld vanuit Zuid-Thailand, voornamelijk uit de provincies Songkhla, Satun, Narathiwat, Phuket en Pattani. Uitbraken van chikungunya komen vaker voor in Thailand en de omringende landen: in 2008/2009 was er een grote uitbraak in Thailand met 22.000 patiënten. De Landelijke Coördinatie Reizigersadvisering (LCR) adviseert reizigers naar risicogebieden voor chikungunya om zich overdag goed te beschermen tegen muggenbeten. (Bronnen: MoPH Thailand, LCR, Suwanmanee et al., Acta Trop 2018)
Auteur
S. Raven, Centrum Infectieziektebestrijding, RIVM
Correspondentie
Infectieziekten Bulletin, jaargang 30, nummer 1, februari 2019